Clear Sky Science · pl
Usuwanie glikanów wywołuje nową dystalną konformację receptora mannozowego CD206
Dlaczego powłoki cukrowe na czujnikach immunologicznych mają znaczenie
Nasze komórki odpornościowe polegają na molekularnych „antenach”, by wykrywać zagrożenia, takie jak drobnoustroje czy komórki nowotworowe. Jedną z tych anten jest receptor mannozowy CD206, który pomaga komórkom odpornościowym chwytać cząsteczki ozdobione cukrami, a nawet kierować się ku nowotworom. Podobnie jak wiele białek, CD206 sam jest pokryty krótkimi łańcuchami cukrowymi. W badaniu postawiono pozornie proste pytanie o daleko idących implikacjach: co dzieje się z kształtem i funkcją CD206, gdy te cukry zostaną usunięte?
Elastyczne ramię czytające sygnały cukrowe
CD206 znajduje się na powierzchni wybranych komórek odpornościowych, zwłaszcza makrofagów patrolujących tkanki i guzy. Ma długą, stawową strukturę sięgającą od błony komórkowej i kończącą się kilkoma domenami lektynowymi, które rozpoznają cukry na napotykanych cząsteczkach. CD206 może też być odcinany do krwiobiegu, gdzie jego stężenia korelują z chorobami zapalnymi i włóknieniowymi, co czyni go potencjalnym markerem schorzeń. Białko jest silnie glikozylowane wiązaniami N, a wcześniejsze prace wykazały, że te modyfikacje mogą wpływać na zdolność poszczególnych segmentów receptora do rozpoznawania cukrów. Wiele miejsc glikozylacji leży daleko od głównych kieszeni wiążących, co sugeruje, że mogą one działać raczej jak odległe przełączniki niż proste blokery.
Modele komputerowe ujawniają ukryte zgięcie
Ponieważ pełna trójwymiarowa struktura CD206 nie została jeszcze odtworzona eksperymentalnie, autorzy sięgnęli po współczesne narzędzia obliczeniowe. Najpierw użyli AlphaFold do zbudowania modeli pełnej długości receptora, a następnie przeprowadzili długie, szczegółowe symulacje dynamiki molekularnej CD206 z przyłączonymi cukrami i bez nich. Obie wersje zachowywały się jak wydłużone molekularne ramię, ale forma „bezcukrowa” wykazała uderzającą nową ruchomość na swoim końcu. Dwie ostatnie domeny lektynowe (oznaczone CTLD7 i CTLD8) mogły kołysać się do wnętrza, tworząc wklęsły, zgięty koniec — kształt nieobserwowany w formie z glikanami, która pozostawała bardziej wypukła i odgięta na zewnątrz.
Jak mała zmiana przeprojektowuje ruch
Aby zrozumieć tę różnicę, zespół przeanalizował dominujące ruchy w swoich symulacjach. Stwierdzili, że główny ruch rozróżniający obie formy to właśnie zgięcie dystalnego końca i że pojawia się ono wyłącznie przy braku cukrów. Usunięcie glikanów ogólnie zwiększało elastyczność receptora, szczególnie w odległych domenach lektynowych, a w mniejszym stopniu w okolicy końca N‑terminalnego. Mapy korelacji wspólnych ruchów różnych części białka pokazały, że bez cukrów ostatnie dwie domeny lektynowe poruszają się bardziej skoordynowanie i są mocniej sprzężone z innymi regionami. W istocie, glikany nie tylko siedzą na powierzchni — pomagają regulować, jak całe ramię się zgina i przekazuje sygnały wzdłuż swojej długości.
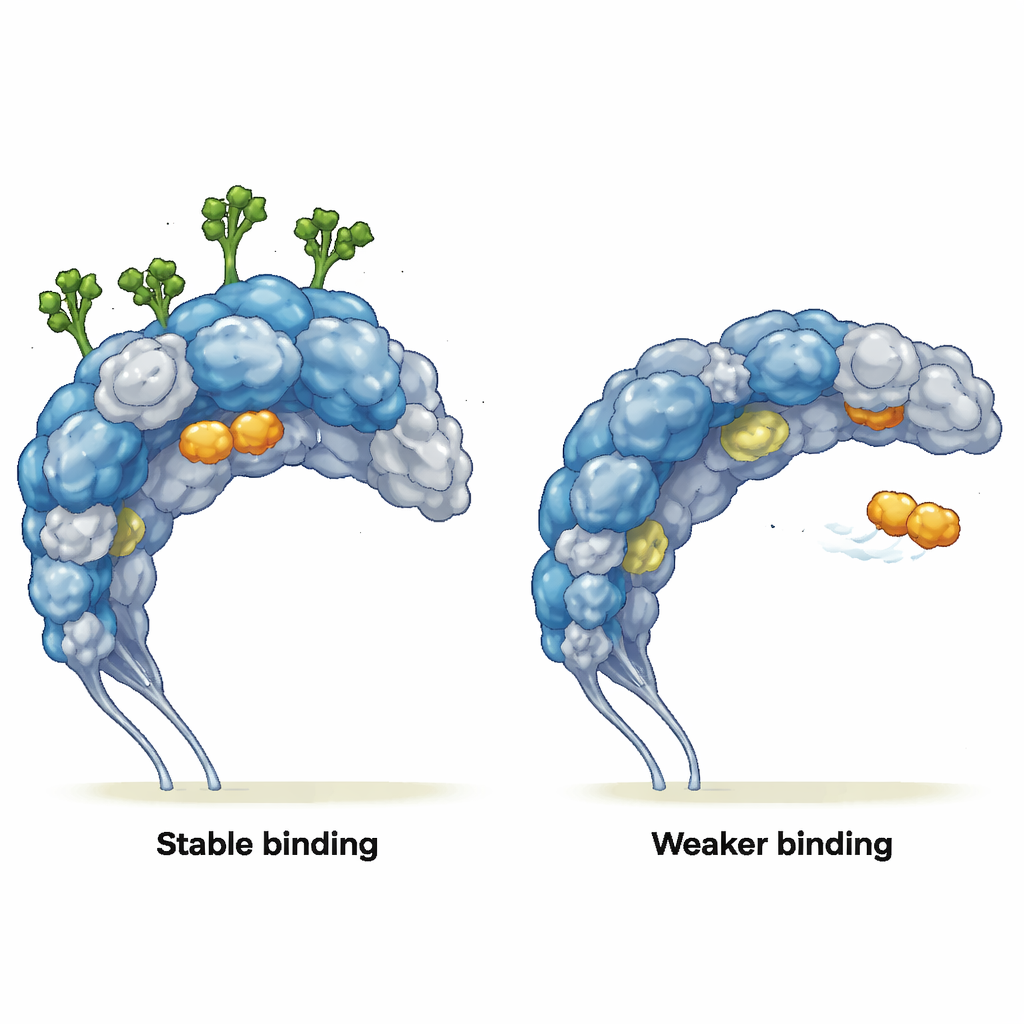
Zmiana sposobu wiązania partnerów
Następnie autorzy sprawdzili, jak zmieniona dynamika wpływa na rzeczywistych partnerów wiążących. Symulowali interakcje z dwoma ligandami: prostym cukrem podobnym do mannozy (MMA), który mieści się w dobrze określonej kieszeni, oraz peptydem o tropie nowotworowym nazwanym mUNO, który celuje w CD206-dodatnie makrofagi związane z guzem. Gdy glikany były obecne, MMA pozostawał ciasno w swojej kieszeni przez całą symulację, utrzymując kluczowe kontakty, mimo że pobliska struktura białka prawie się nie zmieniała. Bez cukrów MMA uciekł z kieszeni, przesuwając się po powierzchni białka i nawiązując tylko krótkie, powierzchowne kontakty. W przypadku mUNO glikozylowany receptor wykazywał kilka stabilnych poz wiążących z częstymi, długotrwałymi kontaktami. W zdeglikozylowanej formie wiązanie mUNO było słabsze i bardziej rozproszone, a peptyd zaczął eksplorować rejony normalnie blokowane przez łańcuchy cukrowe, ujawniając nowe, wcześniej ukryte miejsca interakcji.
Co to oznacza dla chorób i terapii
Podsumowując, wyniki pokazują, że cukry przyłączone do CD206 działają jako zdalni regulatorzy jego kształtu i „lepkości” wobec ligandów. Ograniczając pewne zgięcia i organizując wspólne ruchy segmentów, glikozylacja pomaga receptorowi silniej utrzymywać niektóre ligandy i kierować inne do preferowanych miejsc dokowania, jednocześnie osłaniając część jego powierzchni. W chorobach, takich jak nowotwory, gdzie wzorce glikozylacji białek ulegają zmianom, CD206 może przyjmować odmienne kształty i zachowania wiążące, zmieniając sposób, w jaki komórki odpornościowe wyczuwają środowisko. Zrozumienie tego zależnego od cukrów „przełącznika konformacyjnego” nie tylko wyjaśnia działanie CD206, ale też sugeruje nowe strategie projektowania leków lub znaczników obrazujących, które wykorzystują zmieniający się pejzaż receptora w guzach i innych stanach patologicznych.
Cytowanie: Alvarez, G., Di Lella, S., Pickholz, M. et al. Deglycosylation induces a novel distal conformation in the mannose receptor CD206. Sci Rep 16, 5239 (2026). https://doi.org/10.1038/s41598-026-35240-y
Słowa kluczowe: receptor mannozowy, glikozylacja białek, rozpoznawanie immunologiczne, makrofagi związane z guzem, dynamika molekularna