Clear Sky Science · pl
Nanoskapsułki z chitozanu i siarczanu dekstranu zwiększające skuteczność tigecykliny wobec pozatyfoidalnego Salmonella enterica
Dlaczego to ma znaczenie dla bezpieczeństwa żywności
Większość osób kojarzy Salmonellę z uciążliwym zatruciem pokarmowym, często związanym z niedogotowanym drobiem. Mniej osób zdaje sobie sprawę, że niektóre szczepy stały się tak oporne na antybiotyki, że nawet silne leki „ostatniej szansy” zawodzą. Badanie to bada podejście oparte na nanotechnologii, które może ocalić jeden z takich leków — tigecyklinę — poprzez zamknięcie go w maleńkich kapsułkach na bazie cukrów, które pomagają mu dostać się do zakażonych komórek i wyciszyć kluczowe mechanizmy oporności u Salmonelli.
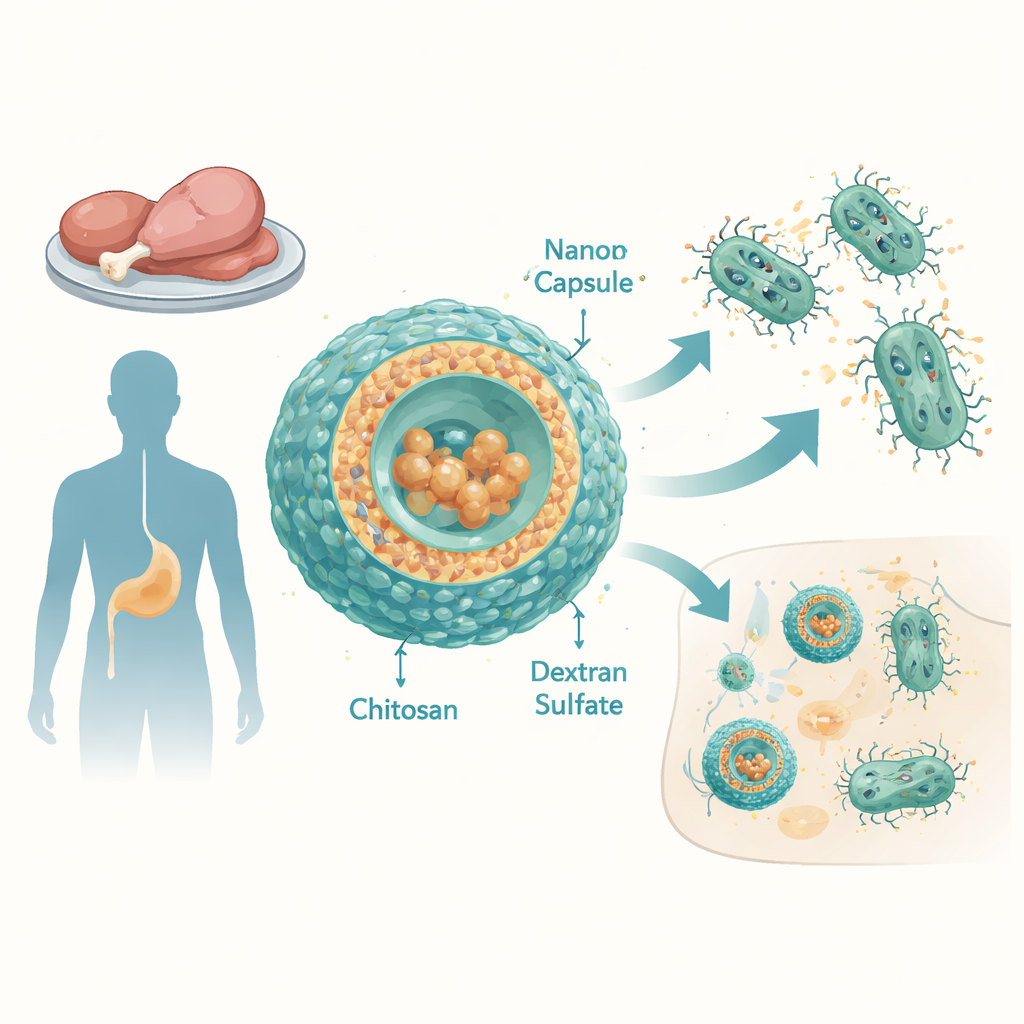
Rosnące zagrożenie ze strony opornych Salmonella
Pozatyfoidalne serowary Salmonella (NTS) są jedną z głównych przyczyn biegunek i zakażeń krwi na świecie, szczególnie w krajach o niskich i średnich dochodach. Badacze przeanalizowali 12 szczepów Salmonella enterica pobranych z mięsa kurcząt i kaczek w Egipcie. Szczepy te były oporne na wiele powszechnie stosowanych antybiotyków, w tym penicyliny, cefalosporyny, tetracykliny i inne, i wykazywały wysokie wskaźniki wielolekowej oporności. Nawet tigecyklina, lek o szerokim spektrum stosowany w trudnych przypadkach, działała słabo: bakterie tolerowały bardzo wysokie jej stężenia. Główną przyczyną były nadaktywne „pompy wypompowujące” — struktury w błonie bakteryjnej, które stale wypompowują antybiotyki na zewnątrz komórki.
Budowa inteligentnej kapsułki leku
Aby to przezwyciężyć, zespół zaprojektował nanoskaliowe kapsułki z dwóch naturalnych polimerów: chitozanu, pozyskiwanego z chityny (materiału występującego w pancerzach skorupiaków), oraz siarczanu dekstranu, rozgałęzionej cząsteczki cukrowej. Poprzez staranne dobranie proporcji tych składników uzyskali stabilne cząstki o wielkości około 100–150 nanometrów i dodatnim ładunku powierzchniowym, co ułatwia ich oddziaływanie z błonami bakterii i komórek gospodarza. Tigecyklina została załadowana do tych cząstek z niezwykle wysoką efektywnością — praktycznie cały lek znalazł się wewnątrz kapsułek. W testach laboratoryjnych symulujących warunki krwi, kapsułki uwalniały większość tigecykliny w ciągu kilku godzin, co sugeruje możliwość dostarczenia silnej dawki antybiotyku w miejscach zakażenia.
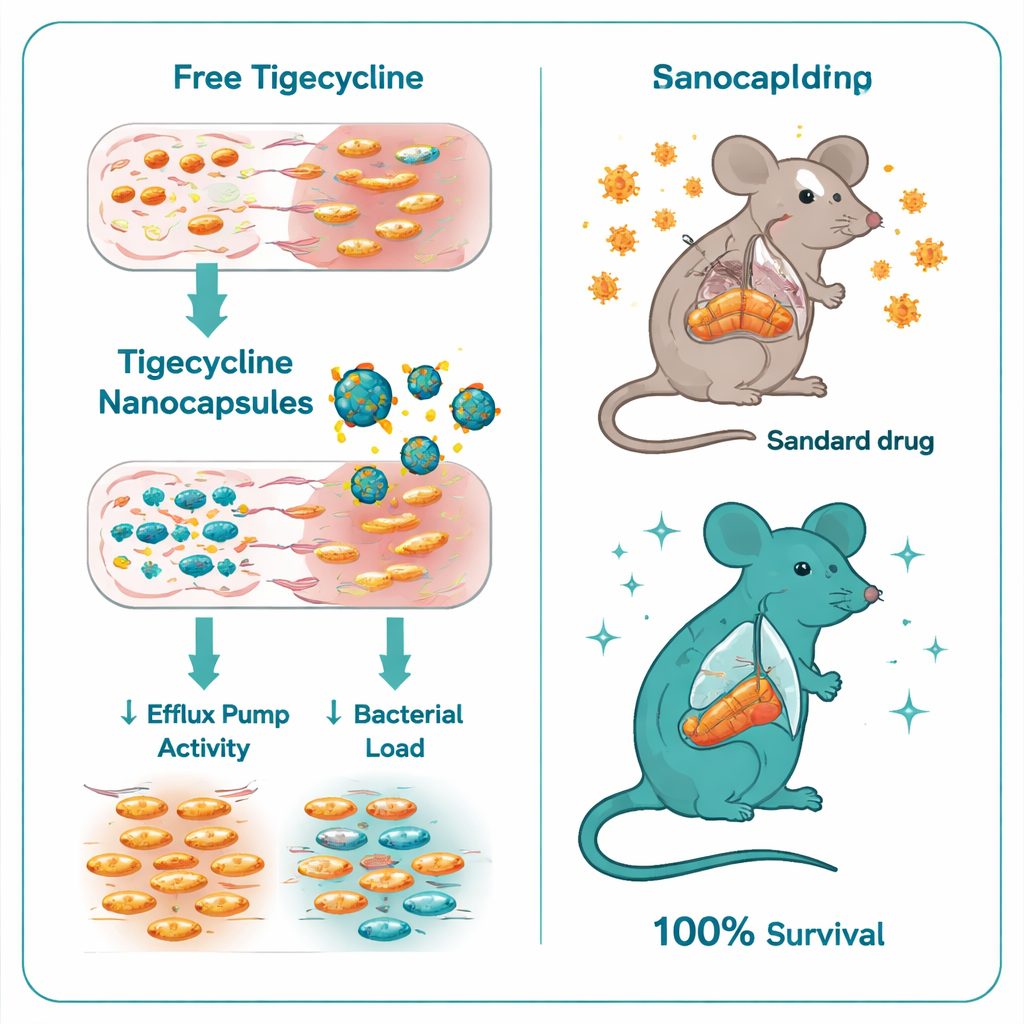
Wyciszanie bakteryjnych mechanizmów obronnych
W porównaniu zwykłej tigecykliny z tigecykliną załadowaną w nanokapsułki chitozan–siarczan dekstranu różnica była uderzająca. Minimalne stężenie hamujące wzrost bakterii spadło z 32–128 mikrogramów na mililitr dla wolnej tigecykliny do zaledwie 0,5–1 mikrograma na mililitr przy użyciu nanokapsułek — poprawa sześciokrotna do siedmiokrotnej. Eksperymenty czas‑zabijania wykazały, że forma enkapsulowana zabijała Salmonellę znacznie szybciej i skuteczniej. Na poziomie genetycznym nanokapsułki również tłumiły kluczowe regulatory oporności: ekspresja genów ramA i acrB, które kontrolują i tworzą główne pompy wypompowujące, obniżyła się wielokrotnie w bakteriach po leczeniu. Innymi słowy, kapsułki nie tylko dostarczały więcej leku; pomagały też wyłączyć jedną z głównych dróg ucieczki bakterii.
Ochrona zakażonych myszy przed śmiertelną chorobą
Zespół następnie przetestował nową formułę w modelu myszy z ciężkim zakażeniem Salmonella Typhimurium. Nieleczone zakażone myszy wszystkie zmarły w ciągu ośmiu dni. Myszy otrzymujące standardową tigecyklinę radziły sobie lepiej, ale i tak miały wysoką śmiertelność — tylko 40% przeżyło. W ostrym kontraście, wszystkie myszy leczone tigecykliną w nanokapsułkach przeżyły. Zwierzęta te miały znacznie mniej bakterii w wątrobie i jelitach, wyniki krwi bliższe normalnej funkcji wątroby i nerek oraz znacznie łagodniejsze uszkodzenia tkanek w badaniu mikroskopowym. Nawet „puste” kapsułki chitozan–siarczan dekstranu, bez antybiotyku, zapewniały pewną ochronę, prawdopodobnie dlatego, że sam chitozan ma umiarkowane działanie przeciwbakteryjne i przeciwzapalne, ale połączenie z tigecykliną było wyraźnie skuteczniejsze.
Co to może znaczyć dla przyszłych terapii
Dla osób niebędących specjalistami główny przekaz jest taki, że umieszczenie istniejącego antybiotyku w inteligentnej, biokompatybilnej nanokapsułce może przywrócić jego skuteczność przeciw wysoce opornym Salmonellom. Dzięki ułatwieniu dotarcia leku do bakterii ukrywających się wewnątrz komórek oraz stłumieniu pomp, które zwykle wyrzucają lek, system chitozan–siarczan dekstranu zmienił słabnący antybiotyk ostatniej linii w wysoce efektywne leczenie na modelu myszy, osiągając 100% przeżywalności. Chociaż przed zastosowaniem tej metody u ludzi lub zwierząt gospodarskich potrzebne są dalsze badania, podejście to oferuje obiecującą drogę do przedłużenia użyteczności ważnych antybiotyków i poprawy bezpieczeństwa żywności bez konieczności wymyślania zupełnie nowych leków od podstaw.
Cytowanie: Omar, M.R., Saeed, A.A., Malhat, S.M. et al. Chitosan-dextran sulfate nanocapsules for enhanced tigecycline efficacy against non-typhoidal Salmonella enterica. Sci Rep 16, 5016 (2026). https://doi.org/10.1038/s41598-026-35229-7
Słowa kluczowe: Salmonella, oporność na antybiotyki, nanocząstki, dostarczanie leków, tigecyklina