Clear Sky Science · pl
Zintegrowana proteomika i metabolomika ujawniają, że fito‑sekewiterpenowe laktony hamują aktywność komórek TNBC poprzez wyczerpywanie syntezy ATP i przeprogramowywanie metabolizmu pierwotnego
Związki roślinne, które głodzą agresywnego raka piersi
Rak piersi potrójnie ujemny jest jednym z najtrudniejszych do leczenia typów raka piersi, ponieważ brakuje mu zwykłych „uchwytów” hormonalnych, za które wiele leków może się zaczepić. To badanie bada dwa związki wyizolowane z rośliny leczniczej, które wydają się wyłączać wewnętrzne elektrownie tych komórek nowotworowych, odcinając ich dopływ energii przy jednoczesnym oszczędzaniu zdrowych komórek piersi. Zrozumienie mechanizmu działania może otworzyć drogę do łagodniejszych, bardziej ukierunkowanych terapii dla pacjentek, które obecnie mają ograniczone opcje.
Dlaczego celowanie w źródło energii nowotworu ma znaczenie
Każda komórka polega na niewielkich strukturach zwanych mitochondriami do wytwarzania ATP, podstawowego paliwa komórkowego. Komórki nowotworowe, zwłaszcza agresywne, często są nadmiernie zależne od mitochondriów, aby wspierać szybki wzrost, rozprzestrzenianie się i przetrwanie w warunkach stresu. Naukowcy skupili się na komórkach raka piersi potrójnie ujemnego, które stanowią około 15–20% przypadków raka piersi i mają skłonność do częstszych nawrotów i przerzutów niż inne typy. Badali naturalny związek deoksyelefantopin (DET) oraz jego zmodyfikowaną wersję DETD‑35, oba sekewiterpenowe laktony z rośliny Elephantopus. Wcześniejsze prace pokazywały, że związki te wywołują stres oksydacyjny i nietypowe formy śmierci komórkowej w komórkach nowotworowych, jednak nie było jasne, jak zaburzają one komórkowe „fabryki energii”.
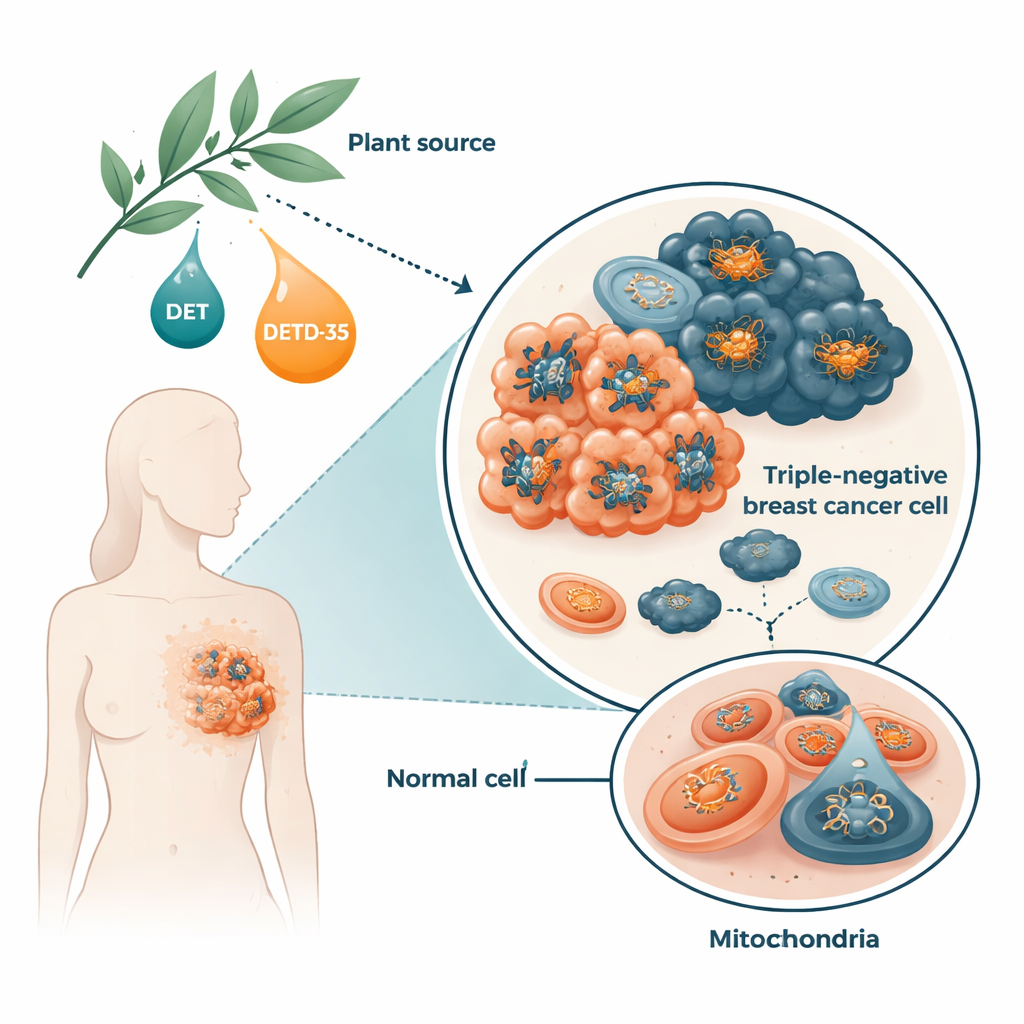
Jak molekuły roślinne zaburzają mitochondria komórek nowotworowych
Na komórkach ludzkiego raka piersi potrójnie ujemnego hodowanych w laboratorium zespół stwierdził, że DET i DETD‑35 szybko zwiększały produkcję reaktywnych form tlenu, rodzaju chemicznie reaktywnego „spalin” powstającego podczas produkcji energii. W odpowiedzi komórki zwiększały poziomy niektórych enzymów ochronnych, lecz nie wystarczało to do przywrócenia równowagi. Związki te wymuszały też otwarcie kanału w błonie mitochondrialnej znanego jako pora przejrzystości przepuszczalności (permeability transition pore), zmiany powiązane z pęcznieniem, utratą potencjału błonowego i wczesnymi etapami śmierci komórki. W ciągu zaledwie kilku godzin poziomy ATP wewnątrz komórek nowotworowych spadały gwałtownie. Gdy badacze dodali wcześniej przeciwutleniacz, te szkodliwe efekty zostały w dużej mierze odwrócone, co wskazuje, że stres oksydacyjny był kluczowym elementem procesu.
Mapowanie uszkodzeń w białkach i metabolizmie
Aby zrozumieć pełen obraz, naukowcy połączyli dwa potężne podejścia „omiczne”. Sklasyfikowali tysiące białek mitochondrialnych i zmierzyli wiele małych metabolitów w komórkach leczonych i nieleczonych. Ten zintegrowany widok ujawnił, że DET i DETD‑35 zaburzały białka zaangażowane w fosforylację oksydacyjną — główną ścieżkę, którą mitochondria wytwarzają ATP — oraz aktywowały sygnalizację związaną ze śmiercią komórkową. Jednocześnie podstawowe szlaki metaboliczne zajmujące się aminokwasami, lipidami i materiałem budulcowym DNA zostały przeprogramowane. Niektóre lipidy, które kształtują wewnętrzną błonę mitochondrialną, jak również cząsteczki powiązane z obroną przeciwutleniającą i rozkładem cukrów, zmieniały się w sposób zgodny ze stresem i niedoborem energii w komórkach nowotworowych. Co istotne, te rozległe zmiany nie były obserwowane w normalnych komórkach gruczołu piersiowego wystawionych na te same dawki, co sugeruje pewien stopień selektywności wobec komórek guzowych.
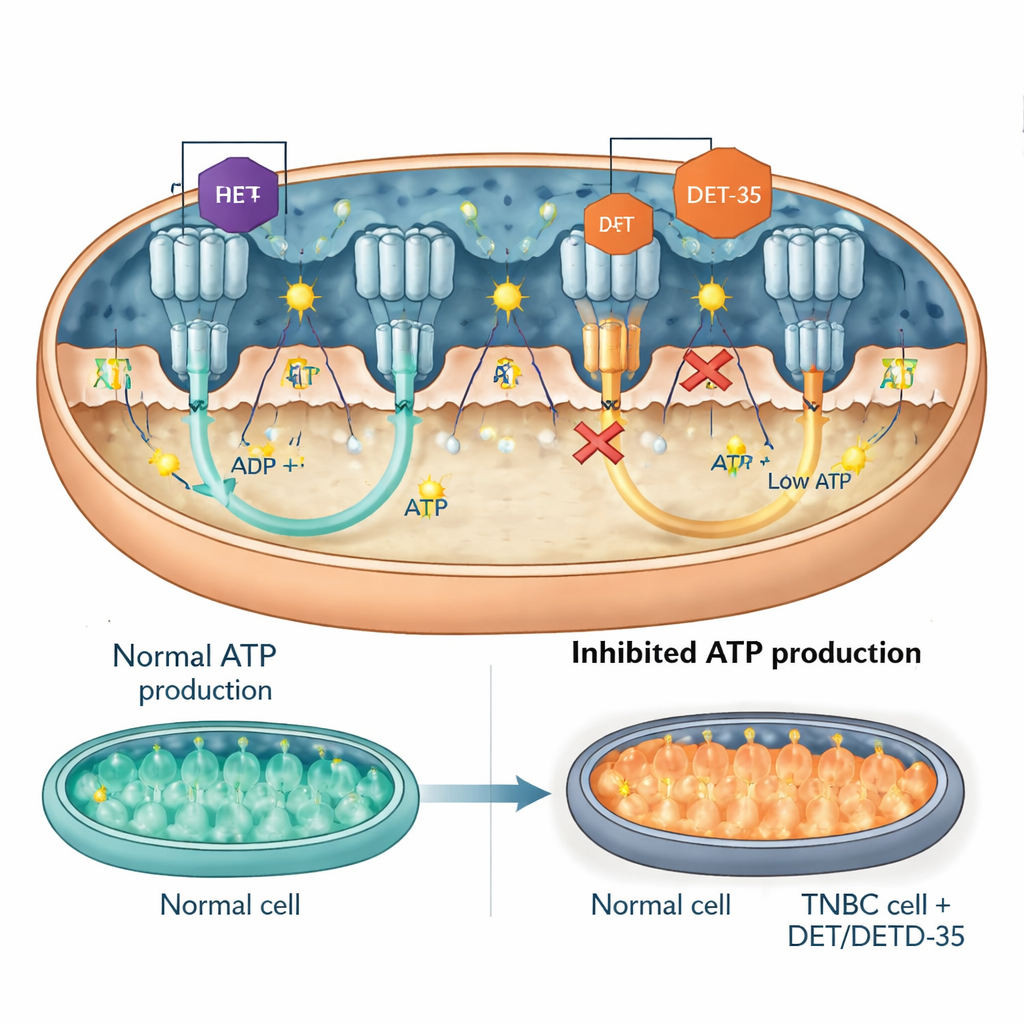
Kluczowe białko sygnałowe i sama turbina ATP
Zespół skupił się następnie na konkretnych uczestnikach tych zaburzonych sieci. Jednym z nich był PRKCA, białko sygnalizacyjne, które może migrować do mitochondriów i wpływać zarówno na produkcję energii, jak i odpowiedzi na stres. DET i DETD‑35 podnosiły poziomy PRKCA w komórkach nowotworowych. Gdy badacze użyli narzędzi genetycznych do obniżenia poziomu PRKCA, leki stały się mniej toksyczne: komórki nowotworowe miały większe szanse na przeżycie, wytwarzały więcej ATP i wykazywały mniej oznak dysfunkcji mitochondrialnej oraz apoptozy. Innym celem była syntaza ATP, molekularna „turbina”, która obracając się wytwarza ATP. Pomiary wykazały, że DET i DETD‑35 bezpośrednio zmniejszały aktywność syntazy ATP w mitochondriach komórek nowotworowych. Modele dokowania komputerowego sugerowały, że oba związki umiejscawiają się w krytycznych interfejsach enzymu, w tych samych ogólnych regionach, gdzie wiążą się znane inhibitory syntazy ATP, fizycznie utrudniając jego ruch i ograniczając produkcję ATP. U myszy niosących ludzkie guzy piersi potrójnie ujemne leczenie którymkolwiek z tych związków obniżyło poziomy składników syntazy ATP w tkance guza, co potwierdza wyniki z hodowli komórkowej.
Co to może znaczyć dla przyszłych terapii przeciwnowotworowych
Podsumowując, badanie przedstawia spójny obraz: związki pochodzenia roślinnego wpychają komórki raka piersi potrójnie ujemnego w kryzys energetyczny, przeciążając je stresem oksydacyjnym, rozchylając pory mitochondrialne i bezpośrednio blokując maszynerię wytwarzającą ATP. W miarę wyczerpywania się ATP i zaburzeń metabolizmu komórki nowotworowe tracą zdolność do wzrostu i przetrwania, podczas gdy normalne komórki piersi pozostają w dużej mierze nieuszkodzone w tych samych warunkach. Dla czytelnika niebędącego specjalistą istotne jest to, że naukowcy mogą wykorzystać silną zależność nowotworów od ich wewnętrznych „elektrowni”, stosując precyzyjnie zaprojektowane molekuły — niektóre inspirowane roślinami — aby wyczerpać „baterie” komórek guza bez wyłączania zdrowej tkanki. Potrzebne są dalsze badania, zanim takie związki mogłyby trafić do kliniki, ale ta zintegrowana perspektywa białek, metabolitów i przepływu energii oferuje obiecującą mapę drogową.
Cytowanie: Shiau, JY., Huang, HJ., Nakagawa-Goto, K. et al. Integrated proteomics and metabolomics reveal phytosesquiterpene lactones inhibit TNBC cell activity by depleting ATP synthesis and reprogramming primary metabolism. Sci Rep 16, 5264 (2026). https://doi.org/10.1038/s41598-026-35194-1
Słowa kluczowe: rak piersi potrójnie ujemny, mitochondria, syntaza ATP, produkty naturalne, metabolizm nowotworowy