Clear Sky Science · pl
miR-760 pochodzący z pęcherzyków pozakomórkowych jako nowy, obiecujący biomarker różnicujący stabilne RRMS od SPMS
Dlaczego te badania mają znaczenie dla osób z SM
Stwardnienie rozsiane (SM) może przebiegać w bardzo różny sposób. U niektórych osób występują wyraźne zaostrzenia z okresami remisji (rzutowo-remisyjne SM, RRMS), podczas gdy u innych choroba stopniowo się pogarsza (wtórnie postępujące SM, SPMS). Obecnie lekarze głównie opierają się na objawach i badaniach MRI, aby odróżnić te postaci, i nie ma prostego testu krwi, który wskazywałby, kiedy pacjent przechodzi z jednego etapu w drugi. W badaniu tym sprawdzono, czy maleńkie pęcherzyki wydzielane przez komórki do krwi, niosące małe regulatory genetyczne zwane mikroRNA, mogą zaoferować nowe, minimalnie inwazyjne narzędzie do rozróżniania stabilnego RRMS od SPMS i pomagać w podejmowaniu decyzji terapeutycznych.
Maleńkie przekaźniki podróżujące we krwi
Nasze komórki nieustannie zrzucają mikroskopijne, otoczone błoną pęcherzyki zwane pęcherzykami pozakomórkowymi do krwiobiegu. Pęcherzyki te przenoszą białka, lipidy i materiał genetyczny z komórek, z których pochodzą, działając jak przekaźniki odzwierciedlające to, co dzieje się wewnątrz organizmu. W badaniu naukowcy pobrali krew od trzech grup: osób z stabilnym RRMS, osób z SPMS oraz zdrowych ochotników. Z osocza wyizolowali pęcherzyki pozakomórkowe i potwierdzili ich wielkość, kształt oraz typowe markery powierzchniowe za pomocą mikroskopii elektronowej, rozpraszania światła i cytometrii przepływowej. Zapewniło to, że mierzone sygnały pochodziły rzeczywiście z pęcherzyków, a nie z przypadkowych fragmentów komórek czy wolno krążących cząsteczek.
Poszukiwanie molekularnego podpisu
Zespół skupił się na mikroRNA, bardzo krótkich odcinkach RNA, które precyzyjnie regulują aktywność wielu genów jednocześnie. Ponieważ są chronione wewnątrz pęcherzyków, mikroRNA są stosunkowo stabilne we krwi. Wykorzystując sekwencjonowanie RNA i uzupełniające testy PCR, badacze zmierzyli poziomy wybranych mikroRNA związanych z pęcherzykami, które są znane lub podejrzewane o udział w zapaleniu i uszkodzeniu nerwów. Jednocześnie oznaczyli szeroki panel białek sygnalizujących układ odpornościowy (cytokin), a także markery uszkodzenia neuronów i komórek wspierających, w tych samych próbkach krwi. W porównaniu między grupami stwierdzono, że cztery mikroRNA pochodzące z pęcherzyków — miR-760, miR-98-5p, miR-301a-3p i miR-223-3p — wykazywały wyraźne różnice między stabilnym RRMS a SPMS, podczas gdy wiele cząsteczek zapalnych było ogólnie wyższych w SM niż u osób zdrowych.
Wyjątkowy kandydat: miR-760
Wśród tych maleńkich regulatorów miR-760 wyróżnił się jako szczególnie informacyjny. U pacjentów ze stabilnym RRMS jego poziomy w pęcherzykach pozakomórkowych były wyraźnie niższe niż u osób zdrowych. W SPMS jednak poziomy miR-760 wracały w kierunku wartości normalnych. Gdy badacze budowali modele statystyczne, aby sprawdzić, która kombinacja markerów najlepiej rozdziela RRMS od SPMS, miR-760 konsekwentnie miał największe znaczenie. Model łączący miR-760 z innym mikroRNA (miR-146a-5p) oraz czynnikiem wzrostu związanym z podtrzymaniem nerwów (podstawowy czynnik wzrostu fibroblastów, FGF basic) poprawnie rozróżniał obie postaci SM z wysoką skutecznością. Analizy sieci genowych sugerują, że miR-760 może być powiązany ze szlakami zaangażowanymi w sygnalizację immunologiczną, naprawę osłonek mielinowych i ochronę komórek nerwowych, co sugeruje, że może to być więcej niż tylko bierny marker.
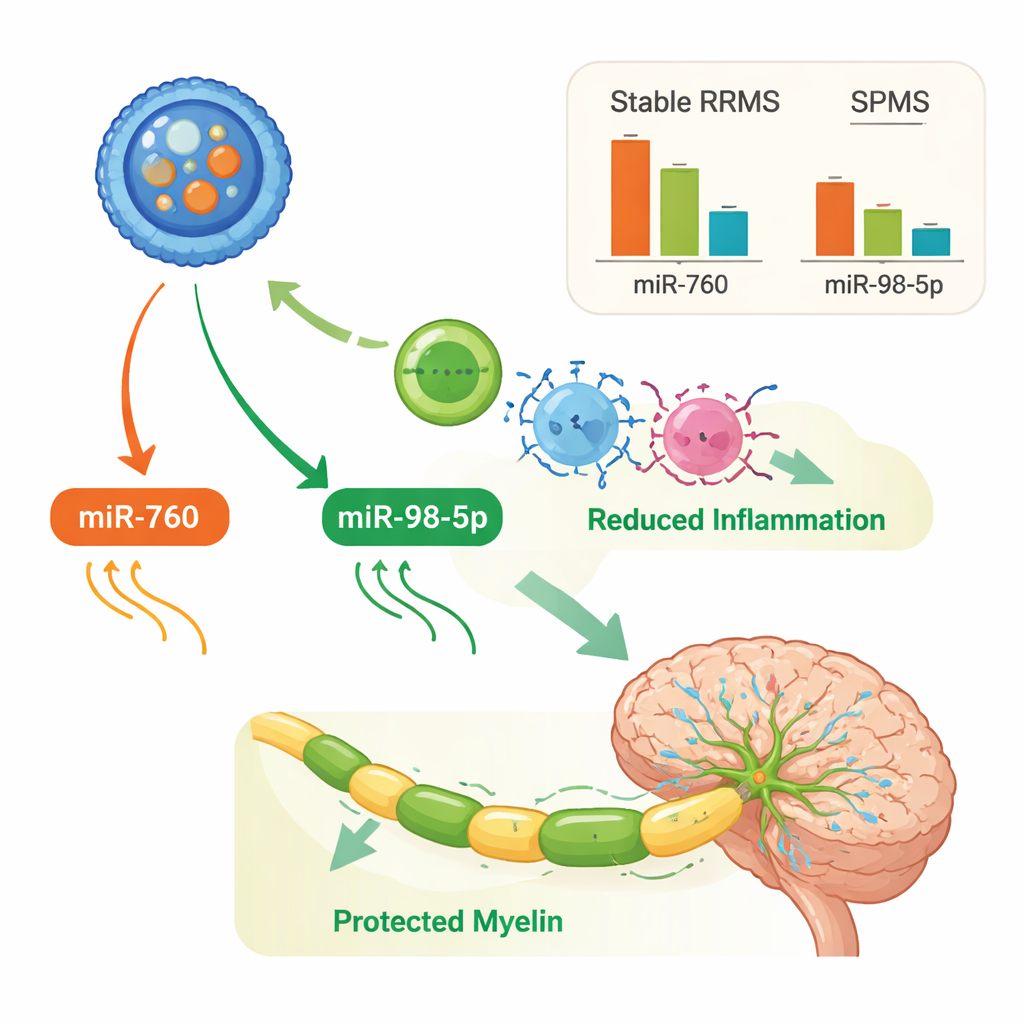
Inne wzorce odpornościowe w chorobie postępującej
Naukowcy przyjrzeli się także miR-98-5p, kolejnemu mikroRNA, które było podwyższone zarówno w RRMS, jak i w SPMS w porównaniu z osobami zdrowymi, a szczególnie wysokie było w SPMS. Wcześniejsze prace łączą miR-98-5p z ochroną bariery krew–mózg i uspokajaniem niektórych agresywnych komórek odpornościowych. W tym badaniu analizy sieci i szlaków sugerowały, że zestaw genów kontrolowanych przez miR-98-5p i inne kluczowe mikroRNA obejmuje wiele procesów istotnych dla SM, w tym zapalenie, usuwanie uszkodzonych białek oraz ścieżki wspólne z innymi chorobami mózgu, takimi jak choroba Alzheimera i ALS. Co ciekawe, niektóre związki między mikroRNA a sygnałami immunologicznymi — na przykład odwrotne relacje między miR-760 lub miR-98-5p a prozapalnymi cytokinami IL-4 i IL-17 — pojawiały się tylko w SPMS, wskazując na zmianę w sposobie, w jaki regulacja odpornościowa funkcjonuje, gdy choroba staje się postępująca.
Co to może oznaczać dla przyszłej opieki
Dla osób żyjących z SM praktyczna obietnica tych badań to przyszłość, w której proste pobranie krwi mogłoby pomóc określić, czy choroba pozostaje w fazie rzutowo-remisyjnej, czy przesuwa się w stronę bardziej stałego pogorszenia. Autorzy proponują mikroRNA pochodzące z pęcherzyków — zwłaszcza miR-760 i miR-98-5p — jako obiecujące składniki takich testów, szczególnie w połączeniu z markerami białkowymi, takimi jak FGF basic. Jednocześnie podkreślają, że wyniki te są wstępne: badanie objęło umiarkowaną liczbę pacjentów z jednego ośrodka, a biologiczne role tych mikroRNA w SM trzeba potwierdzić doświadczalnie. Konieczne będą większe, niezależne i długoterminowe badania, zanim lekarze będą mogli polegać na tych sygnałach w codziennej praktyce, niemniej wyniki stanowią ważny krok w kierunku bardziej precyzyjnych narzędzi opartych na badaniach krwi do śledzenia przebiegu SM.
Cytowanie: Wasilewska, K., Dziedzic, A., Anandan, S. et al. Extracellular vesicle-derived miR-760 as a novel promising candidate biomarker differentiating stable RRMS from SPMS. Sci Rep 16, 5208 (2026). https://doi.org/10.1038/s41598-026-35189-y
Słowa kluczowe: stwardnienie rozsiane, biomarkery, pęcherzyki pozakomórkowe, mikroRNA, postęp choroby