Clear Sky Science · pl
Rab43 łagodzi reakcję zapalną w ostrym uszkodzeniu płuc poprzez ubikwitynację MyD88
Dlaczego uspokojenie zapalenia w płucach ma znaczenie
Gdy w płucach dochodzi do poważnej infekcji lub urazu, odpowiedź immunologiczna organizmu może stać się niebezpiecznie nadmierna. Ta wymykająca się spod kontroli reakcja zapalna, znana jako ostre uszkodzenie płuc, a w najcięższej postaci jako zespół ostrej niewydolności oddechowej (ARDS), może sprawić, że pacjenci na oddziałach intensywnej terapii będą mieć poważne trudności z oddychaniem i niesie ze sobą wysokie ryzyko zgonu. Obecnie lekarze głównie stosują opiekę wspomagającą, taką jak tlen czy respirator, ponieważ nie ma precyzyjnych terapii, które stłumiłyby szkodliwe zapalenie bez osłabienia istotnych mechanizmów obronnych. W badaniu tym odkryto niewielkie komórkowe „kierowstwo” — białko Rab43, które pomaga utrzymać zapalenie płuc pod kontrolą, co wskazuje na nowy kierunek dla ukierunkowanych terapii.
Bliższe spojrzenie na przepracowane płuca
W ostrym uszkodzeniu płuc infekcja lub toksyny uszkadzają cienką barierę między pęcherzykami płucnymi a naczyniami krwionośnymi. Lokalne komórki odpornościowe, zwłaszcza makrofagi patrolujące przestrzenie powietrzne, spieszą z pomocą i zwalczają najeźdźców, wydzielając sygnały chemiczne zwane cytokinami. Chociaż cząsteczki te pomagają niszczyć drobnoustroje, w nadmiarze przyciągają tłumy białych krwinek i powodują przeciekanie płynów, wypełniając pęcherzyki i utrudniając wymianę gazową. Pacjenci mogą rozwijać niskie natlenienie krwi, rozlane zapalenie i często wymagają wentylacji mechanicznej. Zrozumienie, jak makrofagi decydują, kiedy przestać produkować te sygnały zapalne, jest więc kluczowe dla opracowania bardziej inteligentnych terapii.
Niewielki regulator o nazwie Rab43
Rab43 należy do dużej rodziny małych, przełączających się białek, które kontrolują, jak ładunki przemieszczają się wewnątrz komórek. Badacze wcześniej wykazali, że Rab43 pomaga makrofagom usuwać martwe komórki w uszkodzonych płucach. W tej nowej pracy skupili się na tym, czy Rab43 wpływa także na siłę reakcji makrofagów na składniki bakteryjne, takie jak lipopolisacharyd — cząsteczka silnie wywołująca zapalenie. Zarówno w makrofagach płuc myszy, jak i w hodowlanych makrofagach pochodzących ze szpiku kostnego, ekspozycja na lipopolisacharyd powodowała spadek poziomu Rab43. Sugerowało to, że podczas ostrego uszkodzenia płuc naturalny hamulec zapewniany przez Rab43 może być tracony właśnie wtedy, kiedy jest najbardziej potrzebny.
Co się dzieje, gdy brakuje Rab43
Aby ocenić wpływ Rab43 w żywym organizmie, zespół zmodyfikował myszy tak, by brakowało Rab43 wyłącznie w komórkach mieloidalnych, w tym w makrofagach. Następnie wywołali ostre uszkodzenie płuc, dostarczając lipopolisacharyd bezpośrednio do dróg oddechowych. W porównaniu z normalnymi myszami, zwierzęta pozbawione Rab43 rozwijały cięższe uszkodzenia płuc: miały więcej płynu w płucach, więcej napływających neutrofili oraz wyższe poziomy cytokin zapalnych, takich jak TNF-α, IL‑6 i IL‑1β we krwi i płynie płucnym. Myszom tym bardziej spadała masa ciała, wykazywały objawy utrzymującego się ogólnoustrojowego zapalenia i miały znacznie wyższy wskaźnik śmiertelności po śmiertelnej dawce lipopolisacharydu. Wyniki wskazują, że Rab43 normalnie hamuje zapalenie napędzane przez makrofagi i ogranicza szkody wtórne w tkance płucnej.
Węzeł sygnałowy, który Rab43 utrzymuje w równowadze
Pogłębiając badania, naukowcy zbadali kluczowy adaptator sygnałowy w makrofagach o nazwie MyD88, który działa bezpośrednio poniżej sensora lipopolisacharydu na powierzchni komórki. Po aktywacji MyD88 uruchamia silne szlaki, w tym NF‑κB i MAPK, które włączają geny kodujące cytokiny zapalne. W makrofagach pozbawionych Rab43 poziomy białka MyD88 były wyraźnie wyższe, a sygnały wzdłuż tych szlaków silniejsze, mimo że ilość informacyjnego RNA (mRNA) dla MyD88 nie ulegała zmianie. Wskazywało to, że Rab43 wpływa na szybkość rozkładu białka MyD88, a nie na jego produkcję. Zespół wykazał, że Rab43 sprzyja przyłączaniu do MyD88 maleńkich molekularnych „znaczników” zwanych ubikwityną, oznaczających białko do usunięcia przez komórkowy mechanizm recyklingu białek. Bez Rab43 MyD88 miał mniej tych znaczników, unikał terminowej degradacji i nadal napędzał sygnalizację zapalną.
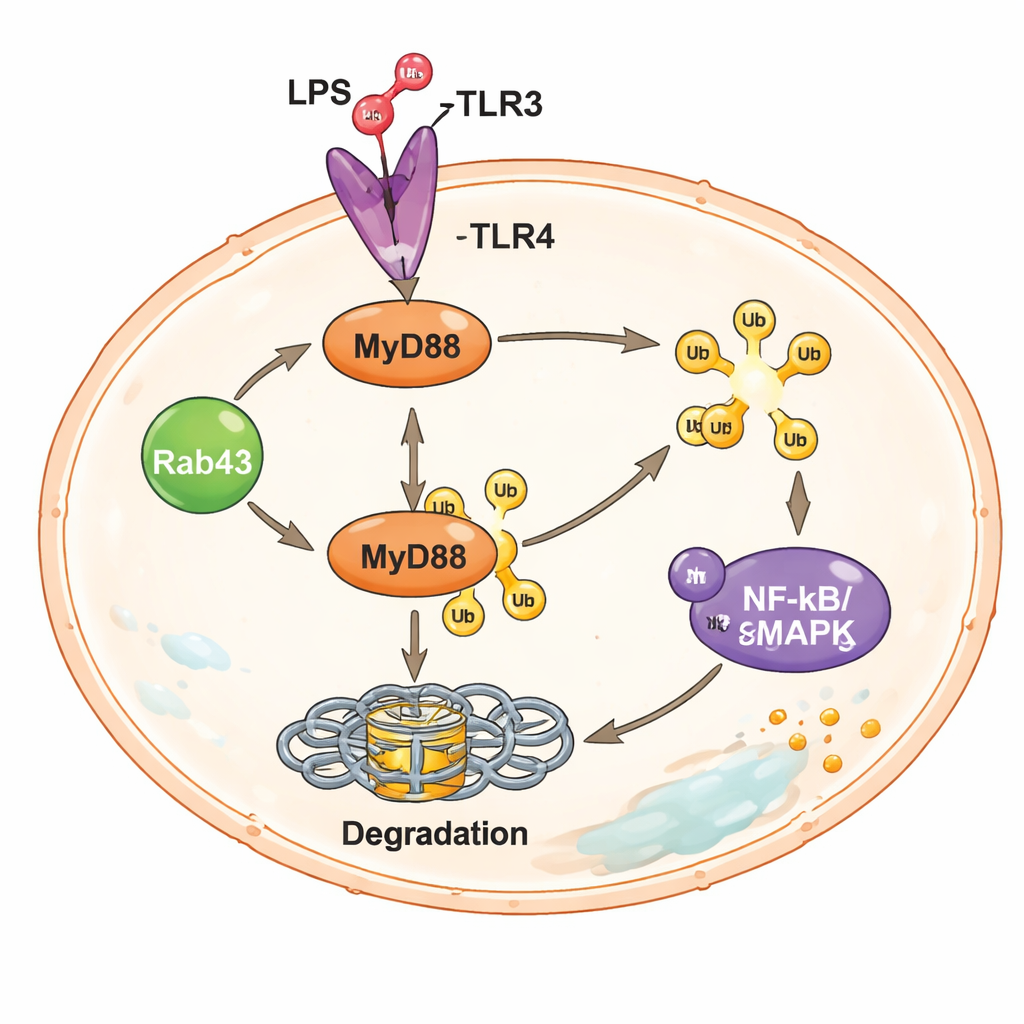
Jak to odkrycie może naprowadzić przyszłe terapie
Łącząc Rab43 z kontrolowanym usuwaniem MyD88, badanie ujawnia wbudowany system bezpieczeństwa, który powstrzymuje reakcje makrofagów przed nadmiernym rozkręceniem się po rozpoznaniu zagrożenia. Rab43 zwiększa ekspresję kilku enzymów, które umieszczają lub modyfikują znaczniki ubikwityny na MyD88, zapewniając, że ten potężny węzeł sygnałowy nie pozostaje włączony w nieskończoność. Gdy Rab43 jest nieobecny lub obniżony, MyD88 utrzymuje się dłużej, kaskady zapalne przebiegają niekontrolowanie, a tkanka płucna ulega uszkodzeniu. Chociaż terapie oparte na Rab43 nie są jeszcze dostępne, wyniki te wskazują na Rab43 oraz ścieżkę degradacji MyD88 jako obiecujące cele dla przyszłych leków mających na celu uspokojenie zagrażającego życiu zapalenia płuc przy zachowaniu zdolności organizmu do zwalczania infekcji.
Cytowanie: Wang, Y., Liu, X., Zhu, Z. et al. Rab43 mitigates the inflammatory response in acute lung injury via MyD88 ubiquitination. Sci Rep 16, 4843 (2026). https://doi.org/10.1038/s41598-026-35187-0
Słowa kluczowe: ostre uszkodzenie płuc, makrofagi, zapalanie, Rab43, MyD88