Clear Sky Science · pl
Bakterie z żywności i mikrobiota jelitowa wytwarzają metyloglikoksal, a ten metabolit prowadzi do powstawania bioaktywnych alkaloidów 1‑acetyl‑β‑carboline
Dlaczego chemiczne laboratorium twojego jelita ma znaczenie
W naszych jelitach i w wielu fermentowanych produktach tryliony bakterii nieustannie przekształcają cukry, które spożywamy, w szereg produktów ubocznych. W tym badaniu szczegółowo prześledzono jedną z takich ścieżek: jak niektóre powszechne bakterie przekształcają cukry w wysoko reaktywny związek zwany metyloglikoksalem, a następnie w rodzinę bioaktywnych substancji nazywanych 1‑acetyl‑β‑carbolinami. Ponieważ te substancje wiążą się zarówno z procesami chorobowymi, jak i z potencjalnymi nowymi lekami, zrozumienie kiedy i jak bakterie je wytwarzają może zmienić nasze postrzeganie żywności, mikrobiomu i zdrowia.
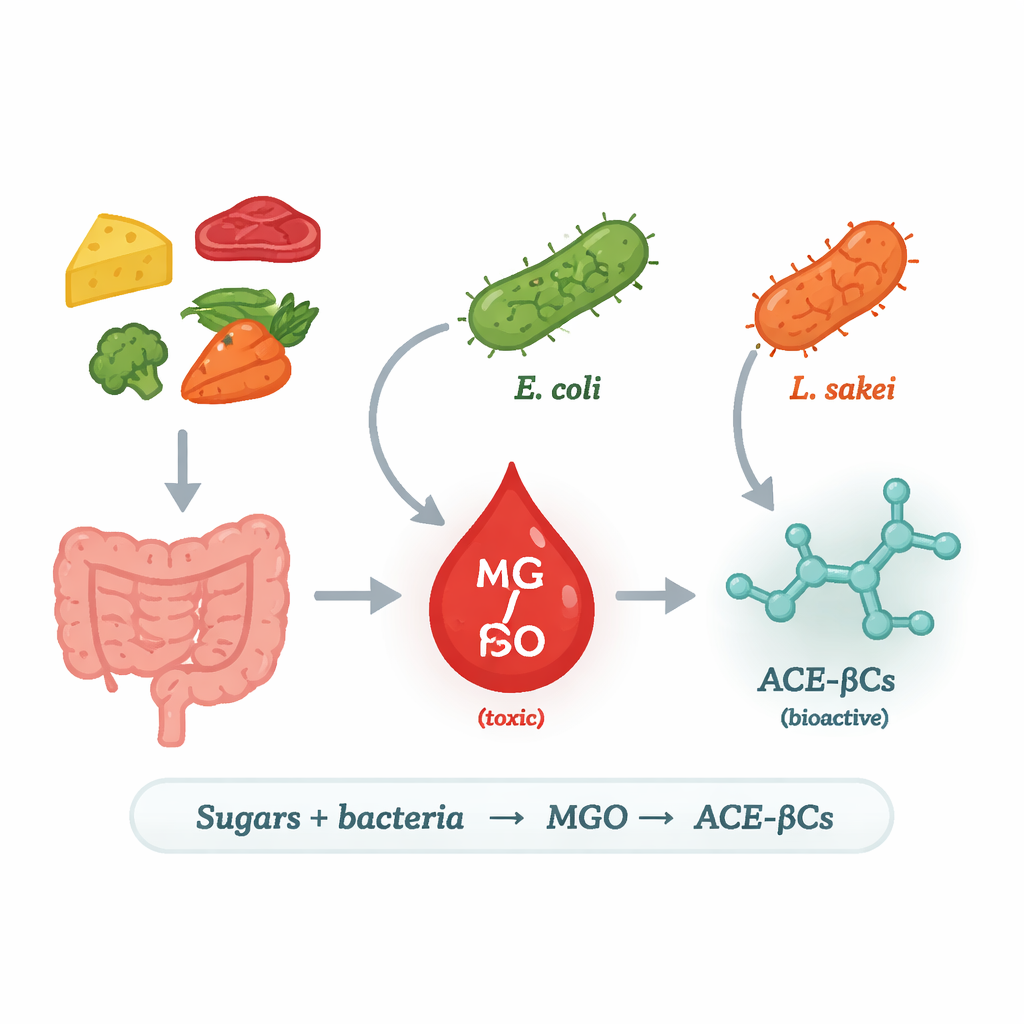
Od codziennych cukrów do ryzykownego związku
Naukowcy skupili się na metyloglikoksalu (MGO), bardzo reaktywnym, toksycznym produkcie ubocznym rozkładu cukrów. U ludzi nadmiar MGO wiąże się z cukrzycą, chorobami serca i neurodegeneracją, ponieważ może uszkadzać białka i DNA. Nasze komórki zwykle neutralizują MGO za pomocą systemów detoksykacyjnych, ale nie są jedynym jego źródłem: MGO mogą też produkować bakterie. W niektórych mikroorganizmach enzym zwany metyloglikoksalową syntazą (MgsA) przekształca pośredni produkt rozkładu cukrów bezpośrednio w MGO, tworząc „skrót” w metabolizmie energetycznym. Zespół zapytał, które bakterie z żywności i jelit używają tej drogi, w jakich warunkach, i co dzieje się z uwalnianym MGO.
Które bakterie są producentami?
Aby to ustalić, naukowcy hodowali kilka szczepów bakterii kwasu mlekowego często występujących w żywności oraz szczep laboratoryjny Escherichia coli w kontrolowanym podłożu zawierającym albo glukozę, albo galaktozę. Następnie śledzili poziomy MGO i dwóch powiązanych alkaloidów w płynie hodowlanym w czasie, używając wysokoczułej chromatografii i spektrometrii mas. Tylko E. coli i gatunek związany z mięsem, Lactilactobacillus sakei, wytwarzały znaczące ilości MGO i alkaloidów; pozostałe testowane bakterie kwasu mlekowego tego nie robiły. Przeszukiwanie genomów ujawniło kluczową różnicę: E. coli i L. sakei posiadają gen kodujący MgsA, podczas gdy większość ich krewnych z kwasu mlekowego go nie ma. Gdy badacze wprowadzili gen mgsA z L. sakei do szczepu nieprodukującego, ten zmodyfikowany bakteriofag (bakteria) zaczął wytwarzać zarówno MGO, jak i alkaloidy, co mocno powiązało MgsA z tą ścieżką.
Jak toksyczny MGO zamienia się w bioaktywne alkaloidy
Następne pytanie brzmiało: co dzieje się z MGO po jego wytworzeniu. Zespół skupił się na alkaloidach 1‑acetyl‑β‑carboline (ACE‑βC), małych cząsteczkach o opisanych właściwościach przeciwmikrobiowych, przeciwzapalnych i przeciwnowotworowych. Pokazali, że gdy bakterie produkujące MGO hodowano w obecności aminokwasu L‑tryptofanu, poziomy dwóch ACE‑βC — 1‑acetyl‑β‑carboline i jej formy 3‑kwasowej — gwałtownie wzrosły. Dodanie dodatkowego MGO do podłoża również zwiększyło ich powstawanie. Wskazuje to, że MGO wypływa z komórek i reaguje spontanicznie z L‑tryptofanem w otaczającym płynie, bez udziału dodatkowych enzymów, tworząc te bioaktywne związki. Innymi słowy, ta sama chemia, która czyni MGO niebezpiecznym, jednocześnie przekształca go w bardziej złożone cząsteczki, które mogą mieć użyteczne efekty.
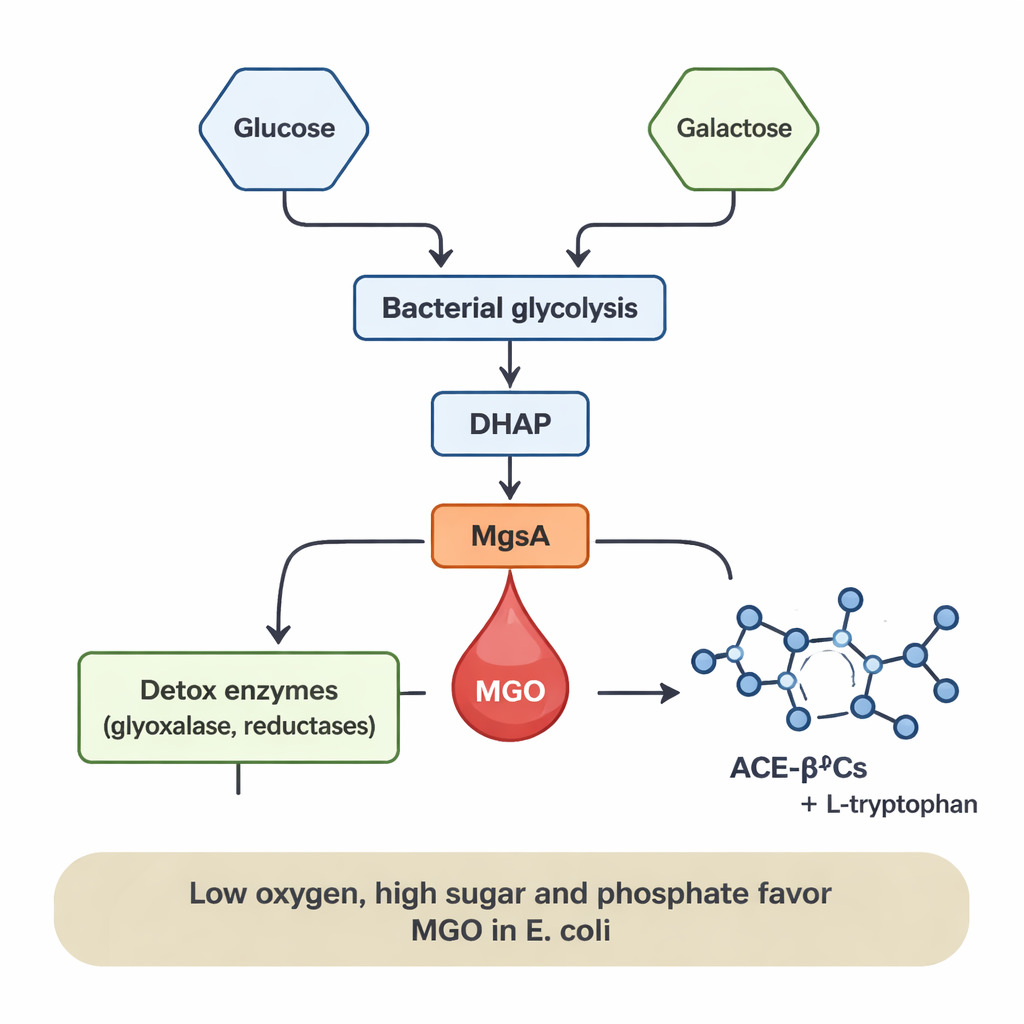
Co zwiększa lub zmniejsza produkcję
Produkcja MGO nie była stała; silnie zależała od diety i środowiska bakterii. W E. coli MGO pojawiał się tylko w obecności glukozy, a jego poziomy rosły wraz ze wzrostem stężenia glukozy. Dodanie fosforanu, powszechnego składnika mineralnego, dodatkowo wzmocniło powstawanie MGO kilkukrotnie, prawdopodobnie dlatego, że sprzyja gromadzeniu się ufosforylowanych pośredników cukrowych zasilających „skrót” MgsA. Warunki niskotlenowe (beztlenowe) — podobne do panujących w ludzkim jelicie — również faworyzowały uwalnianie MGO, podczas gdy wysokie natlenienie wyraźnie je zmniejszało, mimo że bakterie nadal dobrze rosły. W przeciwieństwie do tego L. sakei głównie generowało MGO przy wzroście na galaktozie, a produkcja zwiększała się wraz ze wzrostem poziomu tej cukrowej. Te wzorce sugerują, że kiedy przepływ cukrów przez metabolizm bakteryjny jest duży i tlenu brakuje, MGO może działać jak „zawór upustowy”, rozładowując nadmiar zgromadzonych pośredników cukrowych.
Co to może znaczyć dla żywności i zdrowia
Wyniki sugerują, że nie wszystkie bakterie jelitowe czy spożywcze są sobie równe pod względem zdolności do produkcji MGO i ACE‑βC. Gatunki posiadające enzym MgsA, takie jak niektóre szczepy L. sakei i E. coli, mogą być istotnymi producentami, szczególnie w środowiskach bogatych w cukry i ubogich w tlen, jak jelito czy niektóre fermentacje. MGO, które wydzielają, może zwiększać ogólne obciążenie chemiczne tkanek gospodarza, ale jego przekształcenie w alkaloidy ACE‑βC może także częściowo „pochłaniać” ten reaktywny związek, jednocześnie generując molekuły o własnych efektach biologicznych. Chociaż badanie przeprowadzono w kulturach laboratoryjnych, uwypukla ono prawdopodobną drogę, dzięki której dieta, skład mikrobioty i metabolizm bakteryjny razem kształtują równowagę między substancjami szkodliwymi a potencjalnie korzystnymi w naszym organizmie, i wskazuje na ACE‑βC jako możliwe markery produkcji MGO przez bakterie w żywności i jelitach.
Cytowanie: Herraiz, T., Sánchez-Arroyo, A., de las Rivas, B. et al. Bacteria from foods and gut microbiota produce methylglyoxal and this metabolite leads to the formation of bioactive 1-acetyl-β-carboline alkaloids. Sci Rep 16, 4905 (2026). https://doi.org/10.1038/s41598-026-35162-9
Słowa kluczowe: mikrobiota jelitowa, metyloglikoksal, metabolizm bakteryjny, fermentacja żywności, alkaloidy beta‑carbolinowe