Clear Sky Science · pl
Wyprowadzenie wewnętrznego markera aktywności mózgu do najwcześniejszego przewidywania spadku funkcji poznawczych
Dlaczego wczesne zmiany w mózgu mają znaczenie
Wielu starszych dorosłych zauważa subtelne zaniki pamięci na długo przed tym, jak lekarz może rozpoznać demencję. Na tym etapie standardowe obrazowanie mózgu i badania krwi często wyglądają normalnie, a jednak proces chorobowy może już się toczyć. W badaniu sprawdzano, czy prosty, nieinwazyjny test fal mózgowych — elektroencefalografia (EEG) — może ujawnić bardzo wczesne zmiany w funkcjonowaniu mózgu i wiarygodnie przewidzieć, kto z dużym prawdopodobieństwem doświadczy poważnego pogorszenia funkcji poznawczych za kilka lat.
Słuchając cichych sygnałów mózgu
Naukowcy skupili się na osobach z „subiektywnym pogorszeniem poznawczym” (SCI): starszych dorosłych, którzy odczuwają pogorszenie pamięci, ale nadal wypadają normalnie w standardowych testach. Osiemdziesiąt osiem takich osób w wieku 52–85 lat miało zarejestrowane 20 minut spoczynkowego EEG z zamkniętymi oczami i byli następnie obserwowani przez 5–7 lat. W czasie obserwacji lekarze monitorowali stan poznawczy każdego uczestnika przy użyciu ustalonych skal oceny. Pod koniec okresu część uczestników pozostała stabilna, podczas gdy inni pogorszyli się do łagodnego zaburzenia poznawczego lub rozwinęli demencję. Te wyniki pozwoliły zespołowi sprawdzić, czy subtelne wzorce w pierwotnym EEG mogły przewidzieć, kto później ulegnie pogorszeniu.
Przekształcanie fal mózgowych w predykcyjny odcisk palca
Zamiast analizować EEG wizualnie, zespół zastosował ilościowe EEG (qEEG), które przekształca surowe fale mózgowe w tysiące cech numerycznych. Cechy te odzwierciedlają, jak silne są różne pasma częstotliwości (takie jak rytmy alfa i theta), jak dobrze odległe obszary mózgu synchronizują się ze sobą (łączność i przesunięcie fazy) oraz jak złożony lub nieuporządkowany wydaje się ogólny wzorzec aktywności. Ponieważ samo normalne starzenie się również zmienia EEG, badacze matematycznie skorygowali wszystkie cechy względem wieku, a następnie wystandaryzowali je tak, by „zero” oznaczało oczekiwaną wartość dla zdrowej osoby w tym samym wieku. Aby uniknąć nadmiernego dopasowania, systematycznie zawężono ponad 6 000 kandydatów do zwartego zestawu, który był stabilny, nienadmiarowy i najlepiej rozróżniał osoby, które pozostaną stabilne, od tych, które ulegną pogorszeniu.
Uczenie maszynowe jako kryształowa kula
Z tym zredukowanym zbiorem cech zespół wytrenował kilka modeli uczenia maszynowego — regresję logistyczną, maszyny wektorów nośnych i lasy losowe — aby oszacować prawdopodobieństwo przyszłego pogorszenia dla każdego uczestnika. Powtarzana walidacja krzyżowa i specjalistyczna metoda bootstrap użyto do jak najbardziej realistycznego oszacowania wydajności. W różnych modelach dokładność przewidywania wynosiła około 80%, a pole pod krzywą ROC (AUC) wynosiło około 0,90, co wskazuje na silną zdolność rozróżniania osób stabilnych od tych, które się pogorszą. Ostateczne zamrożone modele używały tylko 14 cech qEEG, głównie pochodzących z przednich obszarów mózgu rejestrowanych za pomocą niewielkiego zestawu elektrod, co czyni podejście praktycznym do rutynowego zastosowania klinicznego.
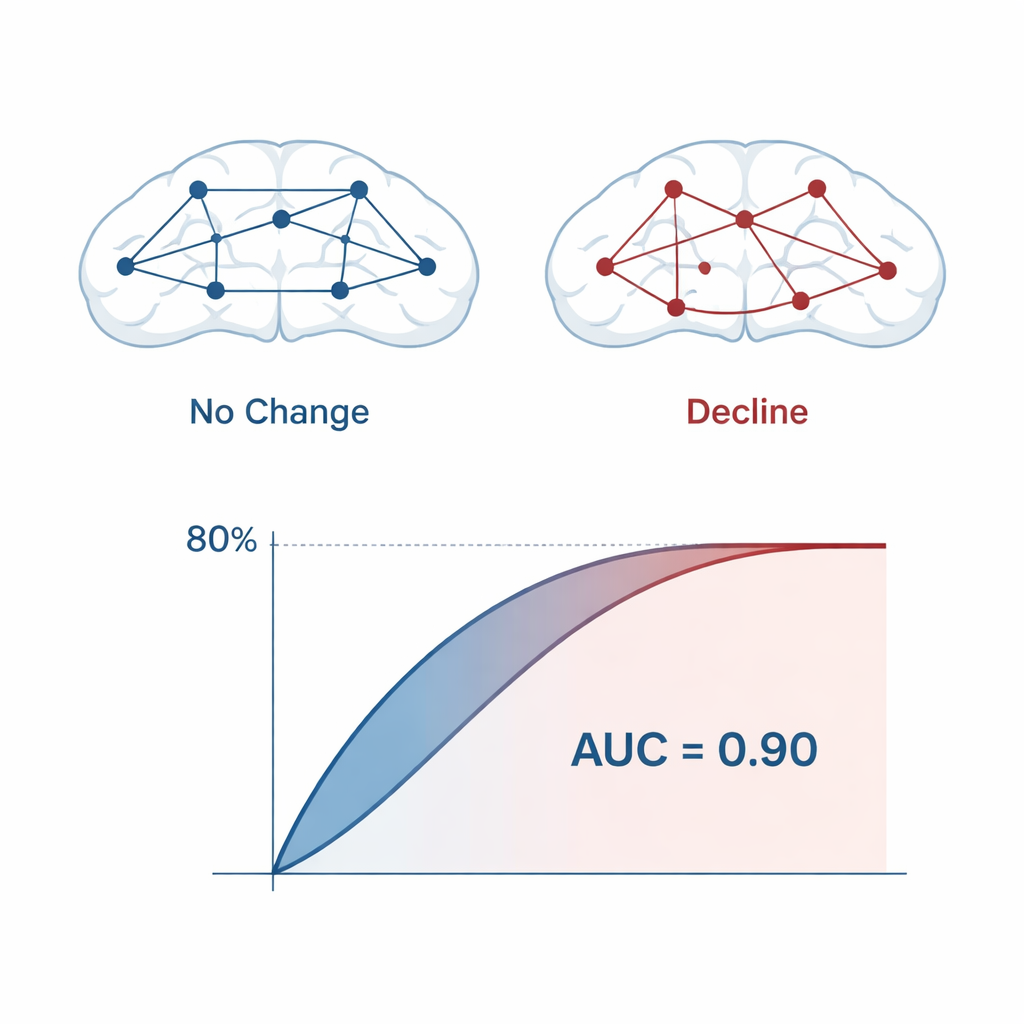
Co się zmienia w mózgu
Cechy najbardziej odpowiedzialne za dokładne przewidywanie wskazywały na wczesne zaburzenia w komunikacji między obszarami mózgu. Mierniki łączności, zwłaszcza przesunięcie fazy i asymetria między lewymi i prawymi obszarami czołowymi, były centralne dla modelu. Nieprawidłowości w pasmach alfa i theta wyróżniały się: zwiększona lub przesunięta aktywność theta w innych badaniach wiązano z atrofią hipokampa i przerzedzeniem kory, podczas gdy zmiany mocy i częstotliwości alfa mogą odzwierciedlać początkowe próby mózgu kompensacji pojawiających się uszkodzeń. Co ważne, żaden pojedynczy miernik EEG nie opowiadał całej historii. To była specyficzna kombinacja — „odcisk palca” biomarkera — która sygnalizowała podwyższone ryzyko na lata przed pojawieniem się pełnych objawów.
Testowanie narzędzia w warunkach rzeczywistych
Aby sprawdzić, czy ich biomarker uogólnia się poza grupę pierwotną, badacze przetestowali go na dwóch niezależnych kohortach ze Stanów Zjednoczonych i Włoch, każdej z różnymi ustawieniami nagrań i cechami pacjentów. Jak można się spodziewać dla całkowicie nowych danych, dokładność spadła umiarkowanie, do około 60–70%, ale model nadal działał znacznie lepiej niż losowe trafienia, co sugeruje, że sygnał, który wychwytuje, jest odporny. Zespół pokazał też, że klinicyści mogą dostosować próg decyzyjny: jego obniżenie zwiększa czułość (wykrywanie większej liczby przyszłych osób ulegających pogorszeniu kosztem większej liczby fałszywych alarmów), podczas gdy podniesienie progu zwiększa specyficzność (mniej wyników fałszywie pozytywnych, ale więcej przypadków przeoczonych). Ta elastyczność pozwala dostosować narzędzie do różnych priorytetów klinicznych.
Co to oznacza dla pacjentów i klinicystów
Mówiąc prosto, praca ta sugeruje, że krótkie, bezbolesne nagranie EEG — wykorzystujące tylko kilka elektrod umieszczonych nad czołem — może pomóc zidentyfikować starsze osoby, które dziś wydają się zdrowe, ale mają wysokie ryzyko pogorszenia funkcji poznawczych w ciągu kilku następnych lat. Chociaż potrzebne są większe badania i porównania z innymi biomarkerami, podejście jest tanie, nieinwazyjne i powtarzalne, co czyni je atrakcyjnym do szerokiego przesiewu, zwłaszcza w miejscach, gdzie zaawansowane obrazowanie lub badania płynu mózgowo-rdzeniowego są niepraktyczne. Jeśli zostanie dalej potwierdzone, biomarkery oparte na EEG mogłyby pomóc lekarzom we wcześniejszej interwencji, monitorowaniu postępu choroby i doborze uczestników do badań klinicznych na etapie, gdy terapie mają największe szanse na trwały efekt.
Cytowanie: Prichep, L.S., Zaidi, S.N., Brink, K. et al. Derivation of an intrinsic brain activity biomarker for the earliest prediction of cognitive decline. Sci Rep 16, 5500 (2026). https://doi.org/10.1038/s41598-026-35144-x
Słowa kluczowe: wczesne przewidywanie demencji, EEG fale mózgowe, subiektywny spadek funkcji poznawczych, biomarker uczenia maszynowego, ryzyko choroby Alzheimera