Clear Sky Science · pl
Analiza projektu i wydajności pionowo układanego tranzystora nanosheet typu gate-all-around z wbudowaną nanokawerną do zastosowań w biosensoryce
Mniejsze sensory, wcześniejsze ostrzeżenia
Wczesne wykrycie nowotworu często zależy od tego, jak szybko i precyzyjnie potrafimy wykryć drobne ślady choroby we krwi lub innych płynach ustrojowych. Artykuł opisuje nowy typ ultramaleńkiego czujnika elektronicznego — wykonanego w technologii podobnej do tej stosowanej w zaawansowanych układach scalonych — który może wykrywać molekuły związane z rakiem z dużo wyższą czułością niż wiele istniejących urządzeń, przy bardzo niskim zużyciu energii.
Przekształcenie tranzystora w detektor raka
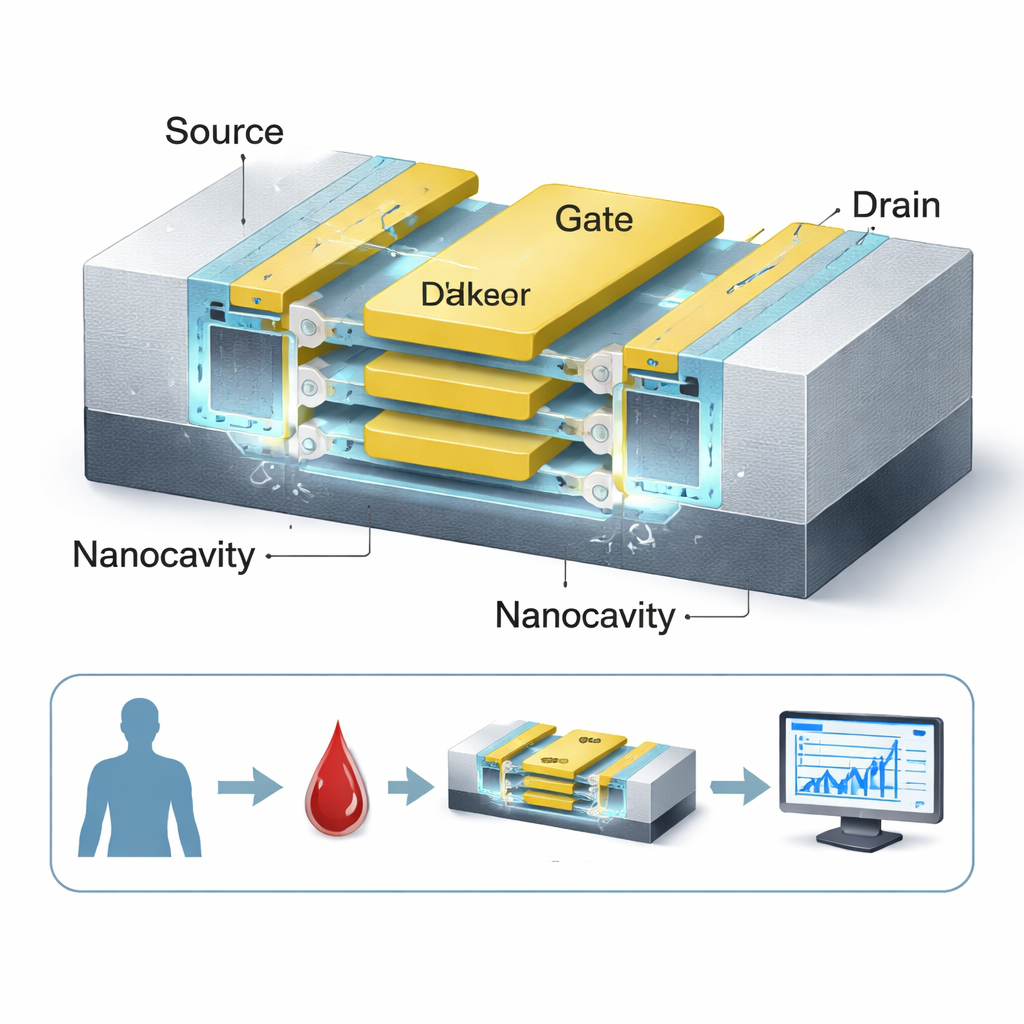
W centrum badań znajduje się przeprojektowany tranzystor, podstawowy element przełączający w elektronice. Autorzy wychodzą od nowoczesnego rodzaju urządzenia nazwanego nanosheet FET, już wdrażanego przez głównych producentów układów do procesorów 3 nm. Przebudowują go na biosensor, tworząc wokół izolowanego gate’a maleńkie puste przestrzenie, czyli nanokawerny. Gdy cząsteczki związane z rakiem — takie jak komórki nowotworowe jelita grubego czy nerek, fragmenty DNA lub żelopodobne białka — osadzają się w tych kawernach, subtelnie zmieniają sposób przepływu ładunku w urządzeniu. Tranzystor „wyczuwa” tę zmianę jako przesunięcie prądu, przekształcając zdarzenie biochemiczne w sygnał elektryczny, który można zmierzyć.
Układanie warstw dla silniejszych sygnałów
Kluczowym rozwiązaniem w projekcie jest to, że kanał sensoryczny nie jest pojedynczym przewodem, lecz trzema ultracienkimi arkuszami krzemu ułożonymi pionowo, wszystkie otoczone wspólnym gate’em. Struktura gate‑all‑around zapewnia bramce znacznie silniejszą kontrolę nad kanałem niż w tradycyjnych, płaskich tranzystorach, co zaostrza przełączanie urządzenia i wzmacnia mierzalną zmianę, gdy obecne są biomolekuły. Dwie nanokawerny umieszczono po obu stronach warstwy dielektryka o wysokim współczynniku (HfO₂), maksymalizując obszar, w którym molekuły mogą wchodzić w interakcję z polem elektrycznym. Ponieważ kanał jest „bez domieszkowania”, czyli unika intensywnego wprowadzania zanieczyszczeń chemicznych, odpowiedź sensora jest bardziej jednorodna i mniej podatna na wariacje procesowe — zaleta dla wiarygodnych testów medycznych.
Dostrajanie maleńkich kawern dla maksymalnej odpowiedzi
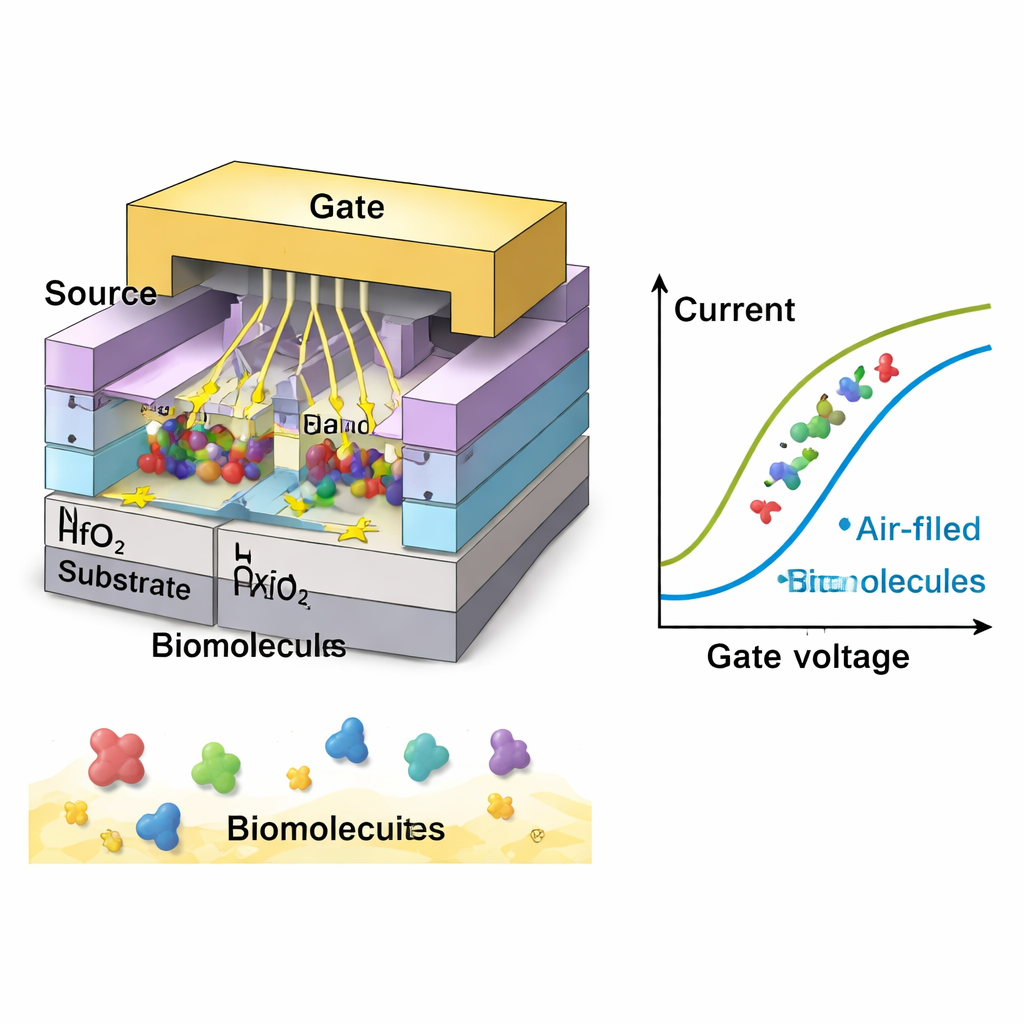
Wykorzystując szczegółowe symulacje komputerowe (TCAD), badacze systematycznie regulują geometrię kawern: ich długość, grubość i stopień wypełnienia molekułami. Krótsze i cieńsze kawerny zbliżają gate do kanału w sensie elektrostatycznym, zwiększając prąd w stanie włączenia i obniżając tzw. subthreshold swing — miarę stromizny przełączania urządzenia. W ich optymalnym projekcie sensor osiąga wyjątkowo niski współczynnik około 28 milivoltów na dekadę, dobrze poniżej granicy 60 mV/dec dla standardowych tranzystorów. Oznacza to, że urządzenie silnie reaguje na bardzo małe zmiany napięcia, co jest kluczowe przy wykrywaniu niskich stężeń biomolekuł. Pokazują też, że wraz ze wzrostem zajętości objętości kawerny — albo gdy molekuły znajdują się bliżej obszaru, od którego rozpoczyna się przepływ prądu — sygnał rośnie, wyjaśniając, jak gęstość i położenie celów wpływają na wydajność.
Odczytywanie wskazówek o raku w sygnałach elektrycznych
Zespół bada następnie, jak różne typy biomolekuł przejawiają się elektrycznie. Obiekty neutralne o wyższej względnej przenikalności dielektrycznej (właściwość opisująca, jak polaryzują się w polu) powodują większe zmiany prądu i lepszą czułość, z najsilniejszą odpowiedzią przy wartości typowej dla żelu i niektórych gęstych tkanek biologicznych. Molekuły naładowane, takie jak DNA czy powierzchnie niektórych komórek, mogą jeszcze bardziej wzmocnić sygnał. W symulacjach ujemnie naładowane biomolekuły dają największe przesunięcie prądu, następnie ładunki dodatnie, a potem obiekty neutralne. W optymalnych warunkach urządzenie osiąga czułość prądu ponad 3000 razy większą niż wartość wyjściowa, a w przypadku silnie ujemnych ładunków ponad 9000 — przewyższając kilka wcześniejszych biosensorów opartych na nanosheet. Sensor wykazuje też szybki czas reakcji, stabilne działanie w pobliżu temperatury pokojowej oraz dobrą specyficzność, czyli zdolność odróżniania docelowych molekuł od podobnych, niechcianych.
W kierunku praktycznych testów raka na poziomie chipu
Aby upewnić się, że koncepcja jest realistyczna, autorzy przedstawiają przebieg technologiczny ściśle zbliżony do dzisiejszej zaawansowanej produkcji układów scalonych, wykorzystujący standardowe wafle silikon na izolatorze (SOI), znane warstwy tlenków i metali oraz powszechne etapy trawienia do formowania nanokawern. Ponieważ struktura pozostaje kompaktowa i zgodna z procesami CMOS, w zasadzie można ją zintegrować w gęstych matrycach na jednym chipie. Dla czytelnika nietechnicznego wniosek jest taki, że praca ta przybliża biosensory oparte na tranzystorach do praktycznych urządzeń lab-on-a-chip, które mogłyby w przyszłości przesiewowo wykrywać markery nowotworowe szybko, z wysoką czułością i bez potrzeby znakowania czy złożonej chemii, wykorzystując technologię bardzo podobną do tej, która już zasila nowoczesną elektronikę.
Cytowanie: Prasanna, R.L., Karumuri, S.R., Sreenivasulu, V.B. et al. Design and performance analysis of a vertically stacked gate-all-around nanosheet FET with embedded nanocavity for biosensing applications. Sci Rep 16, 5508 (2026). https://doi.org/10.1038/s41598-026-35132-1
Słowa kluczowe: biosensor raka, tranzystor nanosheet, lab-on-a-chip, czujnik nanokawerny, wczesne wykrywanie