Clear Sky Science · pl
Dwuswoistość fosfatazy 6 zakłóca represyjną aktywność forkhead box O1 wobec CYP4A11, co pośredniczy w gromadzeniu lipidów w wątrobie
Dlaczego tłuszcz w wątrobie ma znaczenie
Zbyt dużo tłuszczu w wątrobie, często określane jako stłuszczenie wątroby, staje się coraz częstsze wraz z nowoczesnymi dietami bogatymi w cukry i tłuszcze. Choć wielu ludzi słyszało o cholesterolu lub poziomie cukru we krwi, niewiele osób wie, że maleńkie molekularne przełączniki w komórkach wątroby decydują, czy tłuszcz jest spalany, czy magazynowany. W tym badaniu przyjrzano się trzem takim „przełącznikom” — białkom DUSP6, FOXO1 i CYP4A11 — i odkryto, jak ich wzajemna rywalizacja może skłaniać komórki wątroby do magazynowania nadmiaru tłuszczu. Zrozumienie tego ukrytego systemu kontroli może wskazać drogę do nowych terapii stłuszczenia wątroby i powiązanych zaburzeń metabolicznych.
Ukryty kontroler ruchu w komórkach wątroby
Naukowcy skupili się na białku DUSP6, znanym głównie z wyłączania drogi sygnałowej ERK. Wcześniejsze prace wykazały, że myszy pozbawione DUSP6 były zaskakująco odporne na dietetycznie wywołane stłuszczenie wątroby, a ich wątroby miały niższy poziom enzymów CYP4A zaangażowanych w przetwarzanie tłuszczów. W tej pracy zespół zapytał, co DUSP6 robi w komórkach pochodzenia ludzkiego i jak może wpływać na ludzką wersję tych enzymów, CYP4A11. Użyto dwóch standardowych linii komórek raka wątroby, HepG2 i HuH‑7, jako modeli komórek wątroby człowieka i obciążono je mieszaniną kwasów tłuszczowych (kwasu palmitynowego i oleinowego), aby naśladować niezdrowe, wysokotłuszczowe środowisko. 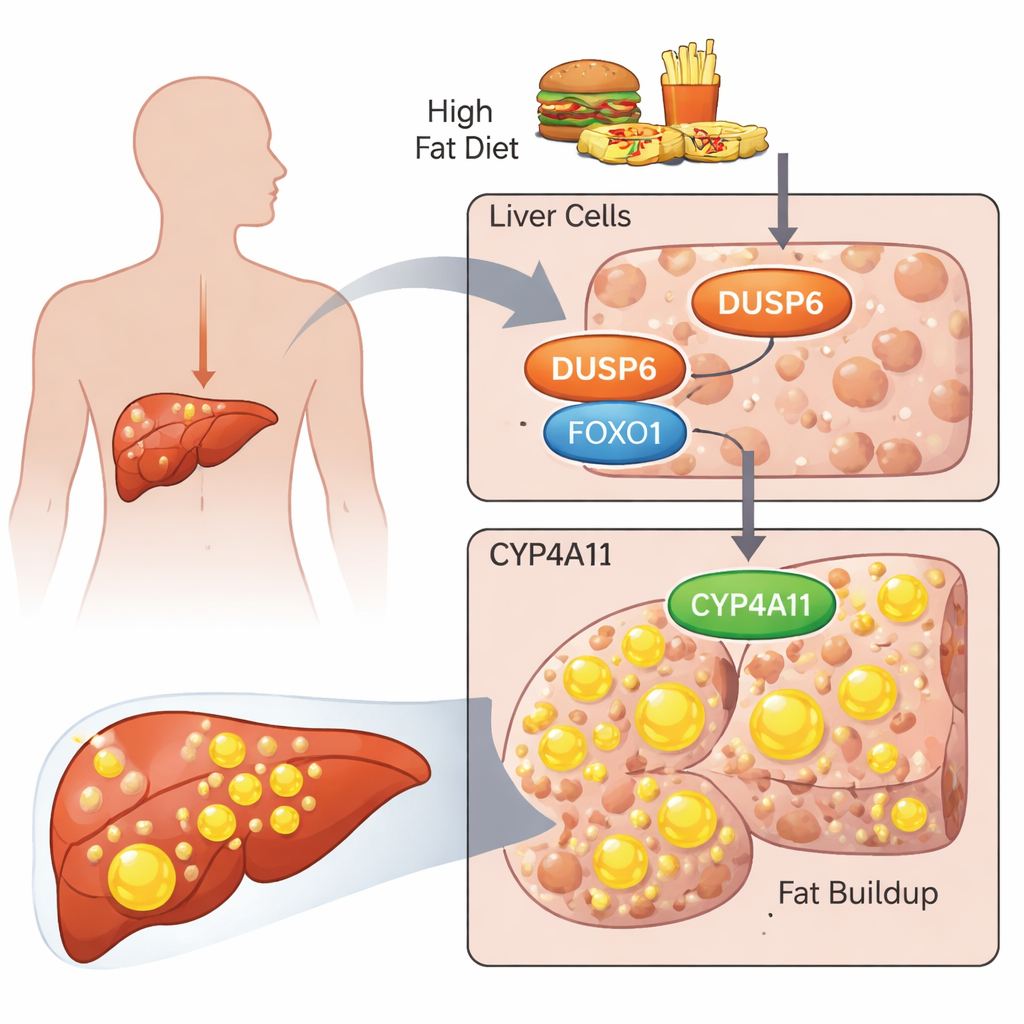
Od kwasów tłuszczowych do komórki wypełnionej tłuszczem
Gdy komórki wystawiono na działanie tych kwasów tłuszczowych, zauważalnie gromadziły krople tłuszczu, które naukowcy barwili i mierzyli. Jednocześnie wzrastały poziomy DUSP6 i CYP4A11 oraz aktywowane formy dwóch głównych białek sygnałowych, AKT i FOXO1. Zmniejszenie ekspresji DUSP6 za pomocą ukierunkowanego RNA odwróciło ten wzorzec: komórki magazynowały mniej tłuszczu, spadły poziomy CYP4A11, ale wzrosła aktywacja ERK, AKT i FOXO1. Zablokowanie samej ścieżki ERK faktycznie pogorszyło gromadzenie tłuszczu, podczas gdy blokada AKT samodzielnie je zmniejszyła. Gdy oba — ERK i AKT — zostały zahamowane jednocześnie, gromadzenie tłuszczu spadło, a poziomy CYP4A11 zmalały. Te eksperymenty ściśle powiązały CYP4A11 z stopniem odkładania tłuszczu i zasugerowały, że aktywność AKT jest szczególnie ważna dla napędzania magazynowania tłuszczu.
Hamulce genów sprzyjających tłuszczu
Kolejnym kluczowym graczem jest FOXO1 — czynnik transkrypcyjny, białko, które może wnikać do jądra komórkowego i włączać lub wyłączać geny. Wiadomo, że FOXO1 działa jako hamulec dla kilku członków tej samej rodziny enzymów co CYP4A11. Zespół wykazał, że zmniejszenie poziomu FOXO1 powodowało, że komórki gromadziły więcej tłuszczu i podnosiło CYP4A11, natomiast bezpośrednie zwiększenie CYP4A11 jeszcze bardziej potęgowało odkładanie tłuszczu. Przeciwnie, wymuszenie większej produkcji FOXO1 zmniejszało zarówno CYP4A11, jak i akumulację tłuszczu. Lek blokujący aktywność CYP4A11 (HET0016) ograniczył dodatkowy tłuszcz wywołany niskim poziomem FOXO1, co potwierdza, że CYP4A11 nie jest jedynie biernym obserwatorem, lecz przyczynia się do gromadzenia lipidów. Testy chemiczne wykazały, że HET0016 obniża poziom 20‑HETE, produktu wytwarzanego przez CYP4A11, powiązanego ze stresem oksydacyjnym i stanem zapalnym, łącząc tę ścieżkę z uszkodzeniem wątroby.
Jak DUSP6 obezwładnia hamulec
Aby zrozumieć, jak FOXO1 kontroluje CYP4A11, naukowcy zbadali region DNA przed genem CYP4A11 i znaleźli sekwencje, do których FOXO1 może się przyłączać. Przy użyciu analizy immunoprecypitacji chromatyny pokazali, że FOXO1 — szczególnie jego nieufosforylowana forma — wiąże się bezpośrednio z promotorem CYP4A11, co jest zgodne z jego rolą represyjną względem tego genu. Eksperymenty ko‑immunoprecypitacji ujawniły, że DUSP6 fizycznie wchodzi w interakcję z FOXO1, ale nie z jego ufosforylowaną wersją. Badania frakcjonowania i mikroskopii pokazały, że DUSP6 lokalizuje się w cytoplazmie komórkowej i gdy jest obecny, zatrzymuje więcej FOXO1 poza jądrem. Po wyciszeniu DUSP6 więcej FOXO1 przemieściło się do jądra, gdzie mogło wiązać DNA i hamować CYP4A11. W efekcie DUSP6 działa jak kotwica, zatrzymując FOXO1 w cytoplazmie i uniemożliwiając mu pełnienie roli hamulca dla CYP4A11. 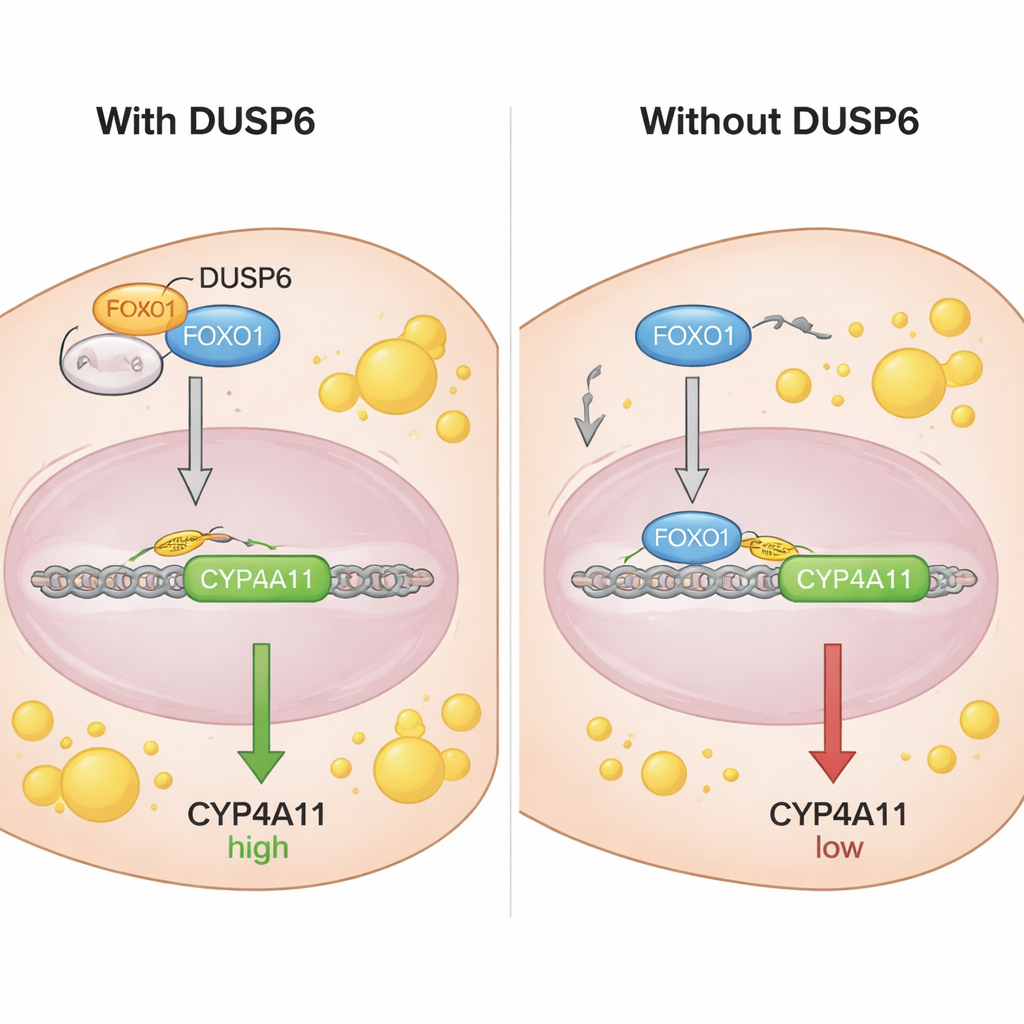
Co to oznacza dla stłuszczenia wątroby i nie tylko
Mówiąc wprost, praca ta mapuje łańcuch zdarzeń w komórkach wątroby: DUSP6 utrzymuje FOXO1 w cytoplazmie, co osłabia zdolność FOXO1 do wyciszania genu CYP4A11. Gdy FOXO1 jest odsunięty, CYP4A11 staje się bardziej aktywny, co sprzyja magazynowaniu tłuszczu i produkcji cząsteczek takich jak 20‑HETE, które mogą promować stres oksydacyjny i stan zapalny. Choć ustalenia pochodzą z hodowanych komórek pochodzenia wątrobowego, a nie z prawidłowej tkanki wątroby człowieka, podkreślają DUSP6 i CYP4A11 jako potencjalne nowe cele terapeutyczne w leczeniu metabolicznie związanej stłuszczeniowej choroby wątroby. Terapie zmniejszające aktywność DUSP6 lub łagodzące efekty CYP4A11 mogłyby teoretycznie przywrócić hamującą funkcję FOXO1 i pomóc utrzymać tłuszcz w wątrobie pod kontrolą.
Cytowanie: Kimura, M., Saiki, Y., Iwata, K. et al. Dual-specificity phosphatase 6 interferes with the repressive activity of forkhead box O1 towards CYP4A11 that mediates lipid accumulation in the liver. Sci Rep 16, 4795 (2026). https://doi.org/10.1038/s41598-026-35118-z
Słowa kluczowe: stłuszczenie wątroby, DUSP6, FOXO1, CYP4A11, metabolizm wątroby