Clear Sky Science · pl
Eksploracja DrugBanku za pomocą uczenia maszynowego ujawnia nowe kandydaty na inhibitory BCL-2
Dlaczego znalezienie mądrzejszych leków przeciwnowotworowych ma znaczenie
Komórki nowotworowe często odmawiają śmierci, gdy powinny ją przejść. Wiele guzów przetrwa dzięki nadmiernej aktywności rodziny „protektorów” nazywanych BCL-2, które blokują wbudowany program samobójczy komórki. Leki ukierunkowane na BCL-2 już istnieją, lecz mogą powodować skutki uboczne i nie działają u wszystkich pacjentów. W tym badaniu zbadano, jak współczesne techniki uczenia maszynowego mogą przesiać tysiące istniejących leków, by znaleźć nowe, bezpieczniejsze kandydaty, które mogą unieszkodliwić BCL-2 i pomóc komórkom nowotworowym w samobójczej eliminacji.
Jak komórki wybierają między życiem a śmiercią
Zdrowe tkanki stale usuwają uszkodzone lub zbędne komórki poprzez kontrolowany proces autodestrukcji znany jako apoptoza, czyli zaprogramowana śmierć komórki. Grupa białek zwana rodziną BCL-2 działa jako centralny przełącznik tej decyzji. Niektórzy członkowie skłaniają komórki ku przeżyciu, inni ku śmierci. W wielu nowotworach członkowie promujące przeżycie, w tym BCL-2 i jego bliski krewny BCL-XL, są produkowani w nadmiarze. Ta dodatkowa ochrona pozwala komórkom nowotworowym ignorować sygnały śmierci i opierać się chemioterapii. Z tego powodu blokowanie BCL-2 stało się atrakcyjną strategią w leczeniu nowotworów, ale obecne leki często trafiają także w spokrewnione białka, co prowadzi do skutków ubocznych, takich jak niebezpieczne spadki liczby płytek krwi.
Nauka komputerów rozpoznawania obiecujących cząsteczek
Zamiast szukać nowych związków od zera, badacze sięgnęli do baz danych cząsteczek już zbadanych lub stosowanych jako leki. Zaczęli od dużego zasobu publicznego o nazwie ChEMBL, który zawiera eksperymentalne pomiary siły wiązania różnych związków z BCL-2. Po starannym oczyszczeniu tych danych — usunięciu duplikatów, niepewnych pomiarów oraz zbyt dużych lub nietypowych cząsteczek — otrzymali 601 dobrze scharakteryzowanych związków. Każdą cząsteczkę przekształcono w rodzaj cyfrowego odcisku palca odzwierciedlającego jej cechy strukturalne. Te odciski użyto do trenowania i porównania siedmiu różnych modeli uczenia maszynowego w zadaniu oceniania, czy nowa cząsteczka prawdopodobnie będzie silnym blokującym BCL-2, czy też praktycznie nieaktywnym. 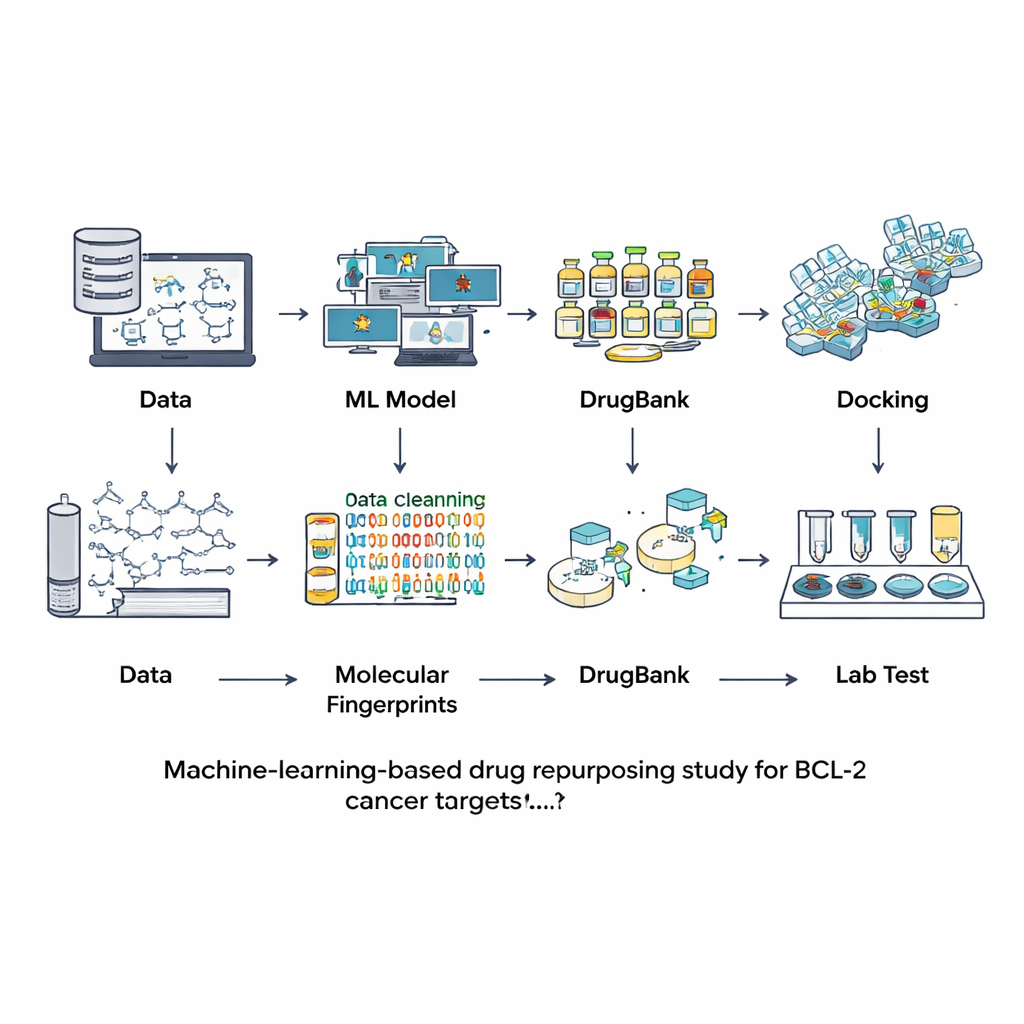
Wybór najlepszego modelu i przeszukiwanie biblioteki leków
Zespół ocenił modele za pomocą odrębnego zestawu testowego, którego modele nie widziały podczas treningu, sprawdzając nie tylko jak często dany model ma rację, ale też jak dobrze rozróżnia aktywne od nieaktywnych związków i jak zrównoważone są jego przewidywania. Najlepsze wyniki we większości miar, w tym w ogólnej dokładności i zdolności przypisywania wiarygodnych prawdopodobieństw, osiągnął model LightGBM — nowoczesna metoda boostingu oparta na drzewach. Z tym dostrojonym modelem w ręku badacze zwrócili się do DrugBanku, kuratorowanej kolekcji ponad 12 000 zatwierdzonych, eksperymentalnych i wycofanych leków. Po obliczeniu tego samego typu odcisków palców, zapytali LightGBM, które z tych cząsteczek wyglądają na potencjalne inhibitory BCL-2. Tylko dziewięć związków uzyskało wysokie wyniki — stanowiąc mniej więcej jedną dziesiątą jednego procenta całej biblioteki — co pokazuje, że wirtualny przesiew był bardzo selektywny. Cztery z tych dziewięciu były już znanymi inhibitorami BCL-2, co uspokoiło zespół, że podejście jest sensowne.
Od wyników komputerowych do interakcji molekularnych
Wśród pozostałych wysoko ocenionych związków badacze skupili się na trzech wcześniej niepowiązanych z BCL-2: Dersalazynie, Opelkonazolu i Zongertinibie. Aby sprawdzić, czy te kandydaty mogą realistycznie pasować do kieszeni wiążącej BCL-2, użyli dokowania komputerowego — techniki przewidującej, jak mała cząsteczka może zagnieździć się na powierzchni białka. Symulacje zasugerowały, że szczególnie Opelkonazol i Zongertinib tworzą sieci korzystnych kontaktów z tymi samymi kluczowymi aminokwasami, które chwytają dobrze zbadany lek referencyjny ABT-737. Ich przewidywane siły wiązania były zbliżone do tych u ustalonych inhibitorów, co sugeruje, że model uczenia maszynowego rzeczywiście odkrył cząsteczki zdolne do unieszkodliwienia BCL-2. 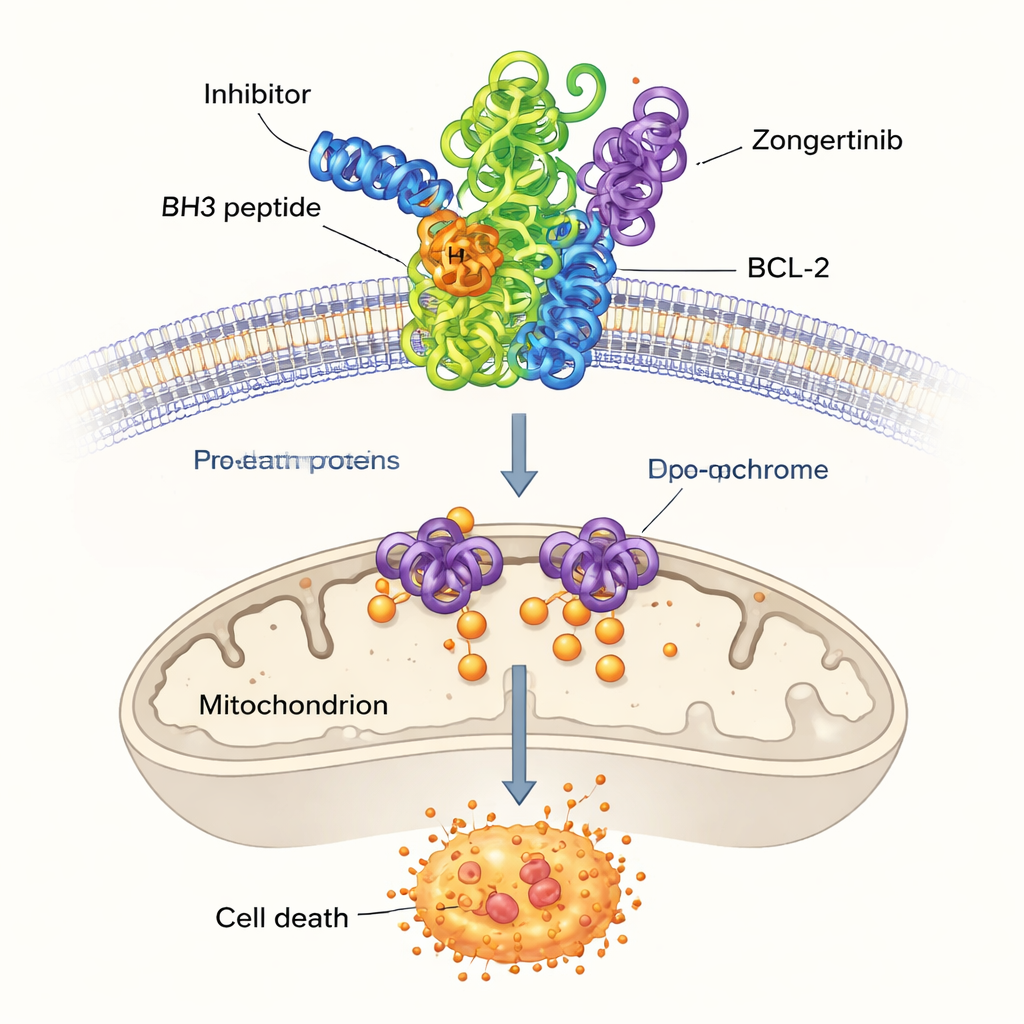
Weryfikacja przewidywań w laboratorium
Wskazówki obliczeniowe są użyteczne tylko wtedy, gdy sprawdzają się w rzeczywistych warunkach. Dlatego zespół przetestował trzy kandydaty w teście biochemicznym mierzącym, jak dobrze związek potrafi zapobiec wiązaniu się BCL-2 z jednym z jego naturalnych partnerów. Przy różnych stężeniach Dersalazyna wykazała niewielki efekt. Opelkonazol i Zongertinib natomiast obniżały aktywność BCL-2 przy wysokich dawkach, przy czym Opelkonazol niemal wygasił sygnał. Choć te stężenia są wyższe niż pożądane dla leku gotowego do zastosowania klinicznego, dowodzą one, że kandydaci rzeczywiście wchodzą w interakcję z BCL-2 i potwierdzają sens całego procesu odkrywania.
Co to oznacza dla przyszłych terapii przeciwnowotworowych
Dla osoby niebędącej specjalistą kluczowy przekaz jest taki, że badacze skutecznie wyszkolili system komputerowy do rozpoznawania, jak „wygląda” cząsteczka blokująca BCL-2, a następnie użyli go do przeszukania dużej biblioteki istniejących leków i związków podobnych do leków. Podejście odnalazło znane leki przeciw BCL-2 i wskazało nowe kandydatury, z których dwa wykazały rzeczywistą aktywność hamującą w testach laboratoryjnych. Choć przed nami wiele pracy — zwiększenie mocy działania, zrozumienie bezpieczeństwa i testy w komórkach oraz modelach zwierzęcych — to badanie pokazuje, jak uczenie maszynowe i staranna kuracja danych mogą przyspieszyć poszukiwanie lepszych leków przeciwnowotworowych poprzez recykling i ponowną ocenę związków, które już znamy.
Cytowanie: Park, J., Cho, S., Lee, H. et al. DrugBank mining with machine learning reveals novel candidates for BCL-2 inhibition. Sci Rep 16, 5482 (2026). https://doi.org/10.1038/s41598-026-35117-0
Słowa kluczowe: inhibitory BCL-2, uczenie maszynowe, ponowne zastosowanie leków, apoptoza, terapia przeciwnowotworowa