Clear Sky Science · pl
Grafowa sieć neuronowa z uwzględnieniem zasad fizyki do przybliżania powinowactwa wiązania z użyciem dokowania dla DYRK2 w remapowaniu leków na Alzheimera
Dlaczego to ma znaczenie dla choroby Alzheimera
Choroba Alzheimera rośnie na świecie, a większość dostępnych leków łagodzi jedynie objawy zamiast zatrzymać postęp choroby. Testowanie nowych leków w laboratorium jest czasochłonne i kosztowne, szczególnie w przypadku mniej poznanych białek mózgowych, które mogą wpływać na pamięć i zdrowie neuronów. W tym badaniu autorzy badają inteligentny skrót: wykorzystanie modelu sztucznej inteligencji świadomego zasad fizyki do przewidywania, jak dobrze istniejące leki na Alzheimera mogą wiązać się z mało zbadanym białkiem o nazwie DYRK2, co potencjalnie otwiera nowe ścieżki terapeutyczne.
Nowy sposób patrzenia na stare leki
Zamiast projektować całkowicie nowe związki od podstaw, badacze skupiają się na remapowaniu leków — znajdowaniu nowych zastosowań dla leków już zatwierdzonych i stosunkowo bezpiecznych. Analizują cztery znane leki na Alzheimera (brexpiprazol, donepezil, galantamina i rywastygmina) i pytają, jak silnie każdy z nich może wiązać się z DYRK2, kinazą białkową zaangażowaną we wzrost i funkcję komórek nerwowych. DYRK2 jest słabo zbadane w kontekście choroby Alzheimera, lecz wstępne dowody łączą je z synapsami, aksonami i pamięcią, co czyni je interesującym celem, który mógłby uzupełniać istniejące terapie.
Przekształcanie cząsteczek w sieci
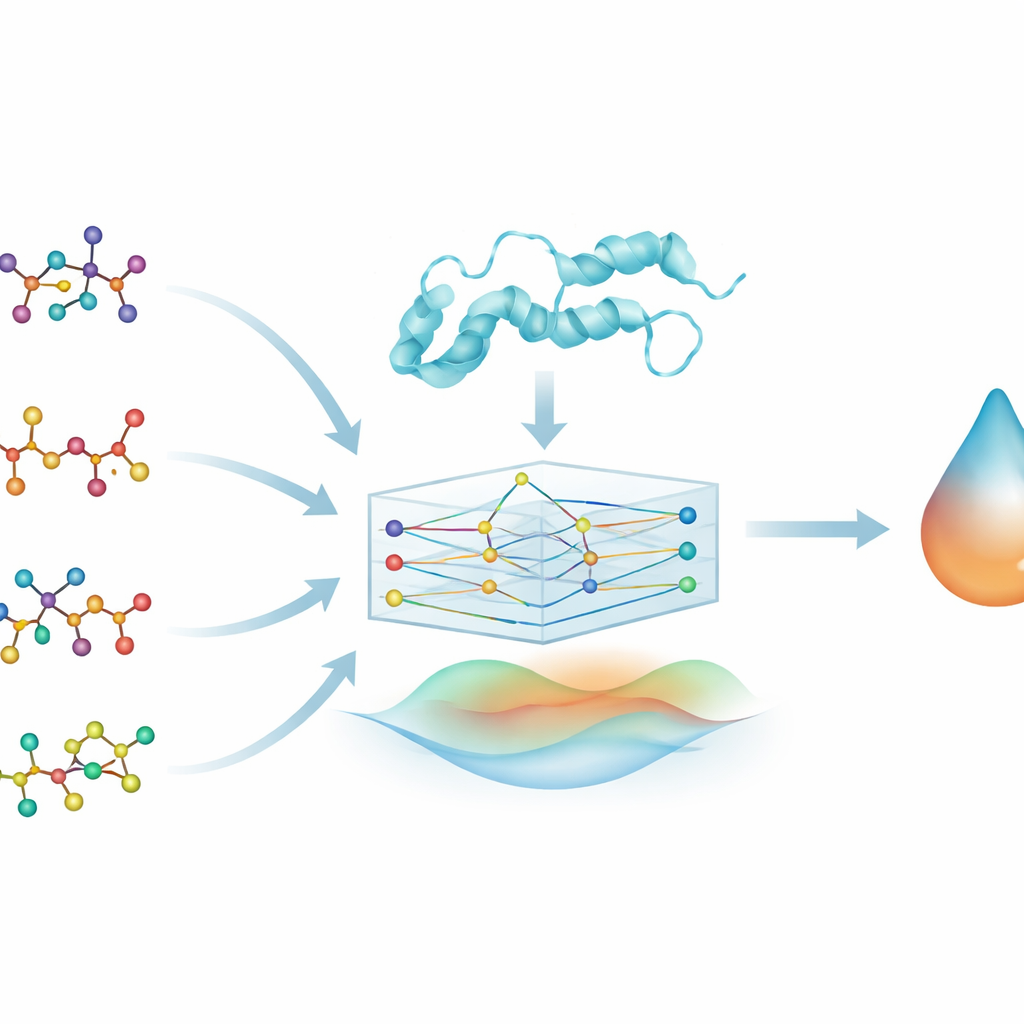
Aby zbadać relacje między lekami a białkiem, zespół reprezentuje każdą cząsteczkę leku jako graf: atomy stają się węzłami, a wiązania chemiczne — krawędziami je łączącymi. Podobnie odwzorowują białko DYRK2, przedstawiając jego sekwencję aminokwasową jako łańcuch połączonych jednostek. Typ modelu uczenia maszynowego zwany grafową siecią neuronową (GNN) naturalnie operuje na takich grafowych wejściach, przesyłając informacje wzdłuż połączeń, aby wyłapywać wzorce kształtu i chemii. Dzięki temu model o nazwie PhysDual‑GCN „odczytuje” zarówno lek, jak i DYRK2 jako sieci wchodzące ze sobą w interakcje, a nie jako proste ciągi czy listy cech.
Łączenie fizyki ze sztuczną inteligencją
Większość narzędzi głębokiego uczenia w odkrywaniu leków uczy się wyłącznie z danych, co utrudnia interpretację ich działania. W tym podejściu autorzy celowo wplatają podstawowe pojęcia fizyczne dotyczące interakcji atomów. Obok uczonych cech grafowych PhysDual‑GCN oblicza dwa klasyczne składniki energii: jeden opisujący przyciąganie i odpychanie elektryczne między ładunkami częściowymi, oraz drugi opisujący efekty van der Waalsa — siły popychania i przyciągania. Te składniki energetyczne oparte na fizyce są łączone z wewnętrzną reprezentacją GNN przed wygenerowaniem przewidywanej siły wiązania. W efekcie model jest trenowany tak, aby naśladować zachowanie standardowych programów dokujących — w szczególności AutoDock Vina i pokrewnych narzędzi — ale robi to szybciej, pozostając jednocześnie osadzonym w znanych zasadach fizycznych.
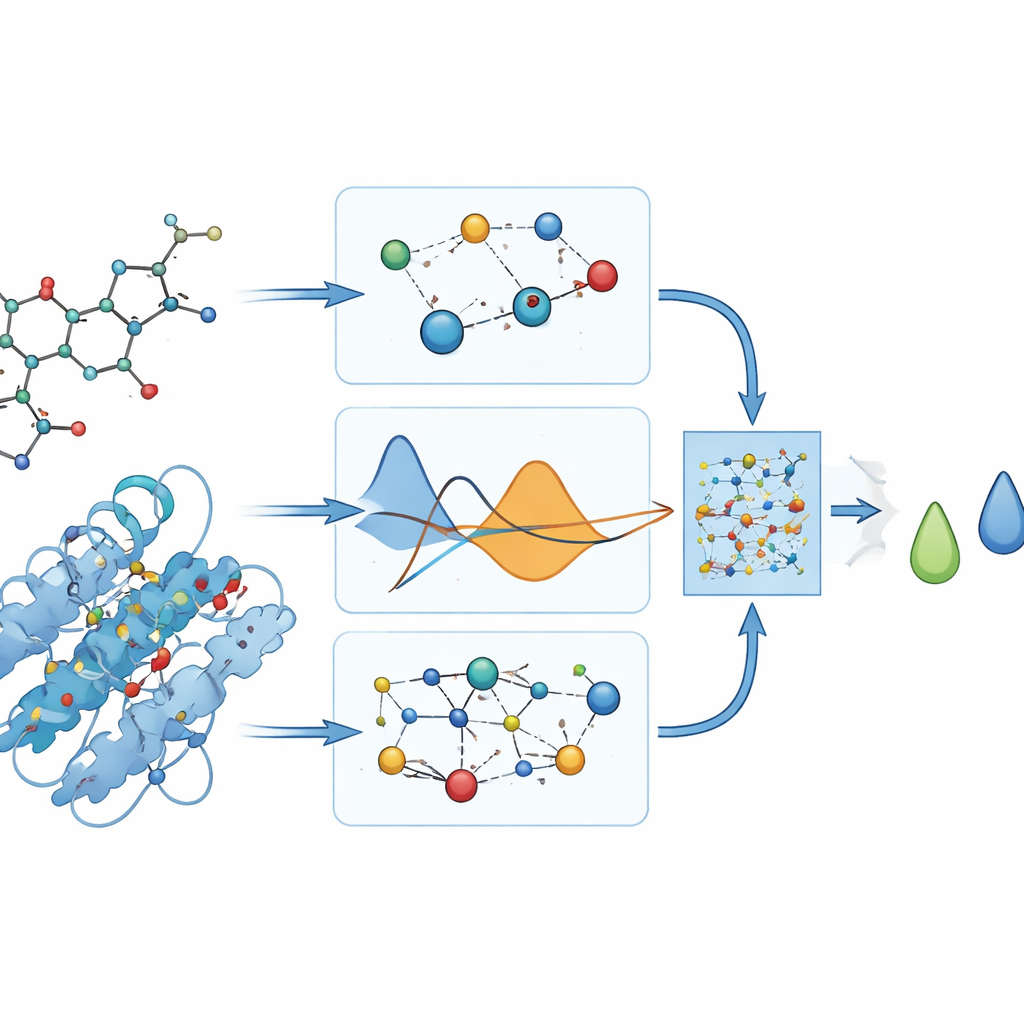
Co model faktycznie przewiduje
Ponieważ nie ma laboratoryjnych pomiarów siły wiązania tych leków do DYRK2, autorzy polegają na programach dokujących, które dostarczają „referencyjnych” wyników wiązania w jednostkach energii. Ostrożnie unikają włączania tych wartości do procesu treningowego i używają ich jedynie później do oceny, na ile PhysDual‑GCN się nauczył. Dla czterech leków na Alzheimera model odtwarza wartości z dokowania z niskimi średnimi błędami (rzędu jednej trzeciej kilokalorii na mol) i poprawnie porządkuje związki: donepezil i brexpiprazol wypadają jako najsilniejsze ligandy, podczas gdy galantamina i rywastygmina wydają się słabsze, lecz wciąż stosunkowo stabilne. Wyniki te pokazują, że fizycznie świadoma GNN może pełnić rolę obliczeniowego substytutu dla wolniejszych przebiegów dokowania.
Obietnice i ograniczenia podejścia
Pomimo zachęcających wyników autorzy podkreślają wyraźne ograniczenia pracy. Zbadano jedynie cztery leki, a wszystkie oceny opierają się na innych programach komputerowych, a nie na rzeczywistych eksperymentach biochemicznych. Białko DYRK2 jest modelowane głównie jako graf jednowymiarowej sekwencji, a nie pełna struktura trójwymiarowa, więc model nie potrafi jeszcze uwzględnić szczegółowego kształtu kieszeni wiążących. Same składowe energetyczne są uproszczone, wykorzystując standardowe parametry pól siłowych i odcięcia. W rezultacie praca powinna być traktowana jako dowód koncepcji: pokazuje, że fizycznie ukierunkowane grafowe sieci neuronowe potrafią blisko śledzić klasyczne wyniki dokowania w warunkach ograniczonych danych, ale nie dowodzi jeszcze, że przewidywania odpowiadają rzeczywistości w probówce czy w klinice.
Co to oznacza dla przyszłych badań nad Alzheimerem
Dla osób niebędących specjalistami główny przekaz jest taki, że inteligentne, świadome zasad fizyki algorytmy mogą pomóc naukowcom szybciej niż tradycyjne metody eksplorować nowe cele w Alzheimerze, takie jak DYRK2. Wskazując donepezil i brexpiprazol jako obiecujących wiążących DYRK2 oraz oferując przejrzysty sposób przybliżania wyników dokowania, PhysDual‑GCN daje punkt wyjścia do głębszych badań laboratoryjnych. Z większymi bibliotekami leków, bardziej szczegółowymi danymi 3D białek i walidacją eksperymentalną tego typu model mógłby stać się praktycznym narzędziem do przesiewania kandydatów na leki i prowadzenia wysiłków remapowania leków mających na celu spowolnienie lub zmianę przebiegu choroby Alzheimera.
Cytowanie: Gider, V., Budak, C. A physics-informed graph neural network to approximate docking-based binding affinity for DYRK2 in Alzheimer’s drug repurposing. Sci Rep 16, 8357 (2026). https://doi.org/10.1038/s41598-026-35102-7
Słowa kluczowe: choroba Alzheimera, remapowanie leków, grafowe sieci neuronowe, wiązanie białko–ligand, kinaza DYRK2