Clear Sky Science · pl
Identyfikacja i charakterystyka depolimerazy fagowej Dpo52 przeciwko karbapenemoodpornej Salmonella enteritidis
Dlaczego to badanie ma znaczenie dla zdrowia codziennego
Zatrucia pokarmowe wywołane Salmonellą są dobrze znane wielu osobom, lecz coraz więcej szczepów tych bakterii jest opornych na nasze najsilniejsze „ostatniej szansy” antybiotyki — karbapenemy. Gdy Salmonella osiada w śliskiej, ochronnej warstwie zwanej biofilmem, staje się jeszcze trudniejsza do zwalczenia. W tym badaniu zbadano alternatywną broń: wirusa atakującego bakterie oraz specjalny enzym, który on niesie, nazwany Dpo52, mogący usuwać ochronną powłokę Salmonelli i zapobiegać osiedlaniu się tych groźnych zarazków.
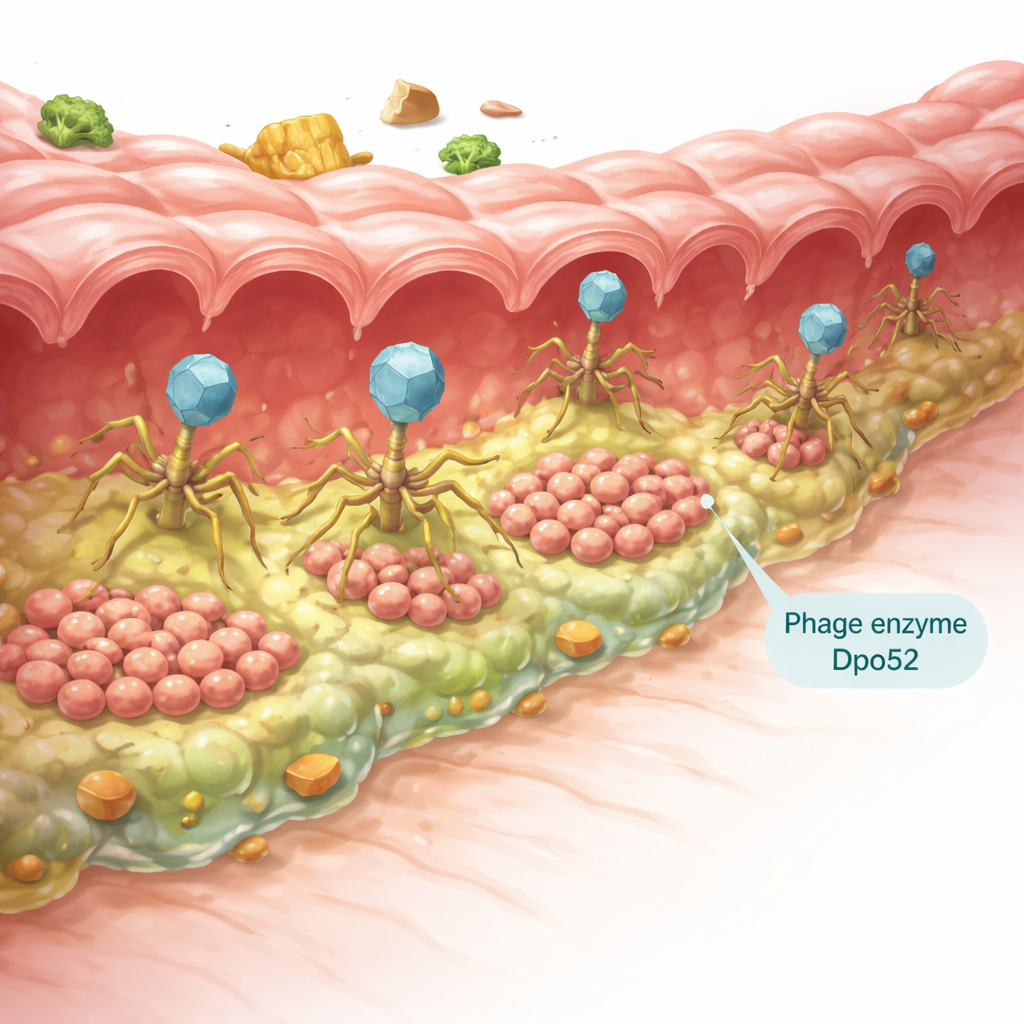
Rośnie problem na naszych talerzach
Salmonella enteritidis jest jedną z najczęstszych przyczyn chorób przenoszonych przez żywność na świecie, często wiąże się z skażonymi jajami, drobiem i innymi produktami zwierzęcymi. Lekarze zwykle polegają na antybiotykach, aby zwalczyć te infekcje, ale wiele szczepów Salmonelli nauczyło się unikać działania wielu leków, w tym karbapenemów stosowanych zwykle w ciężkich przypadkach. Jednym z kluczowych powodów jest tworzenie biofilmów — śliskich społeczności przylegających do powierzchni, takich jak śluzówka jelit, urządzenia przetwórstwa żywności czy same produkty spożywcze. W obrębie tych biofilmów bakterie są osłonięte przed antybiotykami i układem odpornościowym, co zamienia rutynową infekcję w znacznie trudniejszy problem.
Przekształcanie wirusów bakteryjnych w sojuszników
Naukowcy skoncentrowali się na bakteriofagach, w skrócie fagach — wirusach specyficznie atakujących bakterie. Wyizolowali fag z szamba szpitalnego w Chinach, który atakuje karbapenemoodporną S. enteritidis i nazwali go vB_Sen_S3P. Fag ten potrafił zakażać 22 z 30 izolowanych od pacjentów szczepów Salmonelli, w tym najbardziej oporne. Obrazy z mikroskopii elektronowej ujawniły klasyczną budowę faga z geometryczną główką i krótkim ogonem, a testy wzrostu wykazały, że szybko się mnoży, uwalniając tysiące nowych cząstek wirusa z każdej zainfekowanej bakterii. Sekwencjonowanie genomu potwierdziło brak znanych genów oporności na antybiotyki czy czynników wirulencji, co czyni go obiecującym kandydatem do bezpiecznego zastosowania terapeutycznego.
Specjalny enzym, który zdziera śluz
W DNA faga zespół zidentyfikował gen oznaczony ORF52, który prawdopodobnie koduje depolimerazę — enzym rozcinający długie łańcuchy cukrowe tworzące otoczkę bakteryjną i macierz biofilmu. Klonowali ten gen w laboratoryjnym E. coli, wytworzyli białko i nazwali je Dpo52. Modele strukturalne sugerowały, że jedna część Dpo52 rozpoznaje i wiąże powierzchnię Salmonelli, podczas gdy inna działa jako molekularne „nożyce” dla zewnątrzkomórkowych polisacharydów. W testach laboratoryjnych krople oczyszczonego Dpo52 umieszczone na warstwach Salmonelli tworzyły wyraźne strefy halo — dowód, że enzym rozkłada materiał ochronny wokół komórek, nie zabijając ich bezpośrednio.
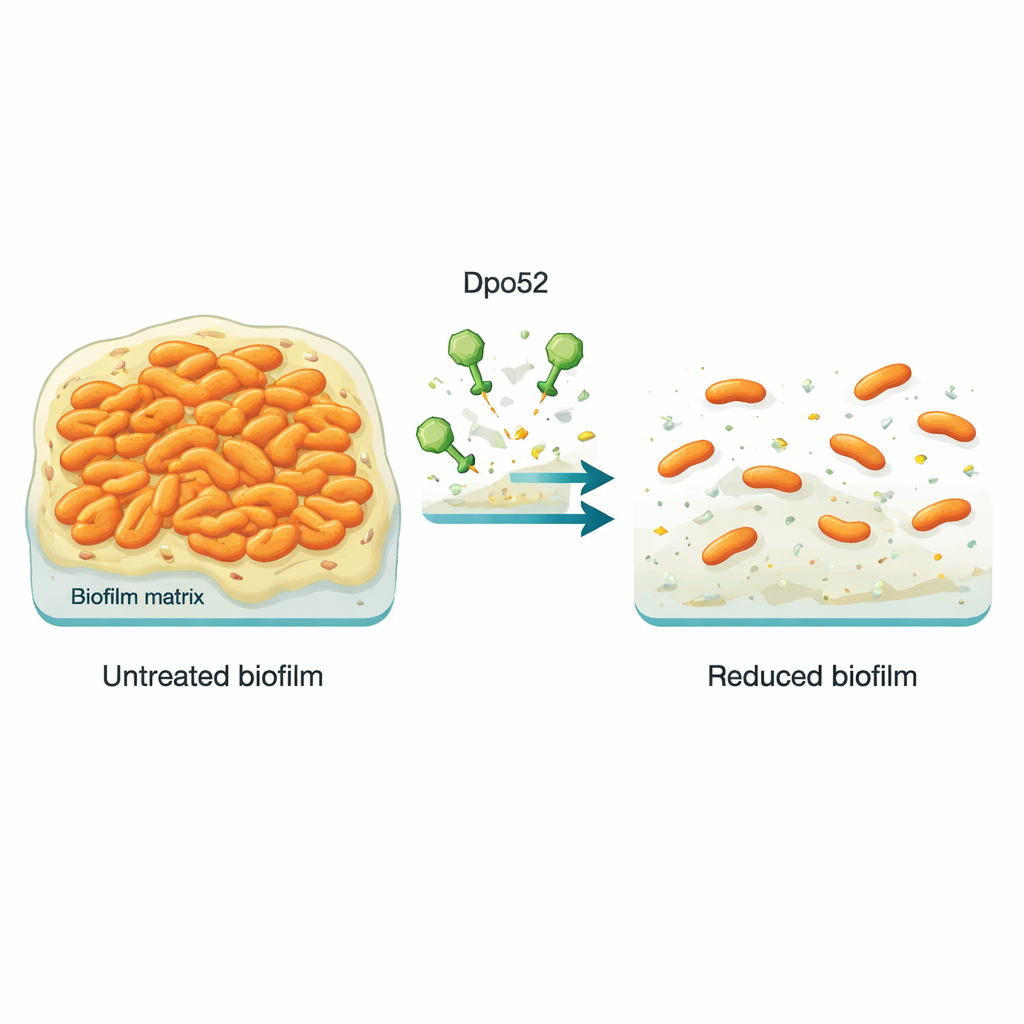
Powstrzymywanie powstawania biofilmu
Aby sprawdzić, czy Dpo52 może zapobiegać tworzeniu się biofilmów, naukowcy hodowali dwa szczepy karbapenemoodpornej Salmonelli w małych plastikowych dołkach, z różnymi dawkami enzymu i bez niego. Po inkubacji barwili dołki, aby zmierzyć ilość nagromadzonego lepkiego biofilmu. Dołki traktowane umiarkowanymi i wysokimi dawkami Dpo52 wykazały znacznie mniej barwienia, co wskazuje, że enzym silnie ograniczał tworzenie biofilmu w sposób zależny od dawki. Jednak gdy biofilm miał najpierw dojrzeć, a dopiero potem był traktowany, Dpo52 nie był w stanie go rozbić — prawdopodobnie dlatego, że gęsta, wielowarstwowa struktura uniemożliwiała enzymowi dotarcie do całej macierzy cukrowej.
Bezpieczeństwo, stabilność i przyszłe zastosowania
Dpo52 okazał się odporny: zachowywał aktywność w szerokim zakresie temperatur od zimnych warunków lodówkowych do 60 °C oraz w warunkach od umiarkowanie kwaśnych po zasadowe. Co ważne, testy na ludzkich komórkach odpornościowych (komórkach podobnych do makrofagów THP‑1) nie wykazały wykrywalnej toksyczności, nawet przy wysokich dawkach. Mikroskopia potwierdziła, że Dpo52 usuwa bladą otoczkę otaczającą komórki Salmonelli, zgodnie z jego rolą w trawieniu polisacharydów zewnątrzkomórkowych. W sumie te cechy sugerują, że Dpo52 mógłby być dodawany do powierzchni, produktów spożywczych lub terapii opartych na fagach jako ukierunkowane narzędzie zapobiegające osadzaniu się trudnych do leczenia, opornych Salmonelli w postaci biofilmów.
Co to oznacza w walce z trudnymi infekcjami
Dla czytelników niebędących specjalistami kluczowy przekaz jest taki, że badanie identyfikuje wysoce specyficzny, nietoksyczny enzym, który pomaga zdzierać ochronną „powłokę śluzu” groźnej, opornej na leki Salmonelli, zanim zdąży się ona zadomowić. Chociaż Dpo52 nie rozpuszcza w pełni dojrzałych biofilmów, wykazuje duży potencjał jako środek zapobiegawczy — stosowany samodzielnie lub razem z fagami i antybiotykami — w celu zwiększenia bezpieczeństwa żywności i środowisk medycznych. W miarę jak naukowcy udoskonalają takie enzymy i poszerzają ich zakres działania, mogą stać się ważnym elementem naszego przyszłego zestawu narzędzi przeciwko infekcjom odpornym na antybiotyki.
Cytowanie: Li, W., Yuan, M., Che, J. et al. Identify and characterize a carbapenem-resistant Salmonella enteritidis phage depolymerase Dpo52. Sci Rep 16, 4906 (2026). https://doi.org/10.1038/s41598-026-35081-9
Słowa kluczowe: Salmonella, oporność na antybiotyki, terapia bakteriofagowa, biofilmy, enzymy depolimerazowe