Clear Sky Science · pl
Struktura krystaliczna cystatyny B Echinococcus multilocularis ujawnia nowe cechy klasycznych stefin
Dlaczego „tajna broń” pasożyta wątroby ma znaczenie
Alveolarna echinokokoza to trudna do wymówienia nazwa choroby wywoływanej przez niewielkiego tasiemca, który w wątrobie zachowuje się podobnie do wolno rosnącego nowotworu. Często bywa śmiertelna, a dostępne leki działają słabo i mogą powodować poważne skutki uboczne. W badaniu przyjrzano się jednemu z cząsteczek wydzielanych przez pasożyta — białku nazwanym EmCystatin-B — aby zrozumieć, w jaki sposób może ono pomagać robakowi unikać naszych mechanizmów obronnych i jak mogłoby być w przyszłości wykorzystane jako cel nowych terapii.
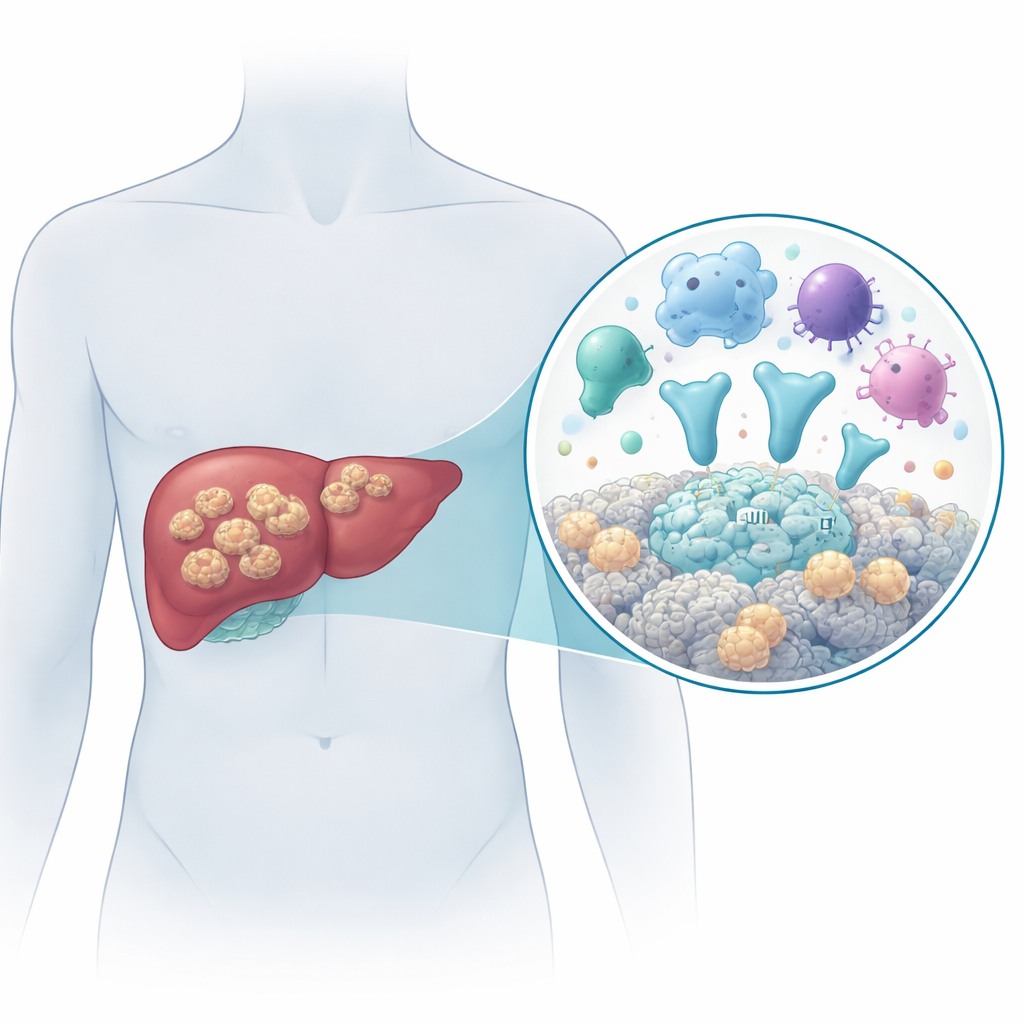
Niebezpieczny tasiemiec rosnący jak guz
Chorobę wywołuje larwalna forma tasiemca Echinococcus multilocularis. Do zakażenia dochodzi przez przypadkowe połknięcie jaj pasożyta, na przykład w skażonej żywności lub wodzie. Po dostaniu się do organizmu larwy osiadają głównie w wątrobie i rozwijają się jako liczne małe, wypełnione płynem torbiele, które naciekają okoliczne tkanki, rozprzestrzeniają się do pobliskich narządów, takich jak śledziona, a niekiedy docierają do odległych miejsc — płuc czy mózgu. Bez skutecznego leczenia ponad 9 na 10 pacjentów umiera w ciągu 10–15 lat. Najlepszą dostępną opcją jest obecnie operacja połączona z długotrwałym leczeniem przeciwpasożytniczym, lecz wczesne rozpoznanie jest trudne, a leki nie gwarantują wyleczenia. Dlatego kluczowe jest zrozumienie na poziomie molekularnym, jak pasożyt wchodzi w interakcje z organizmem człowieka.
Białko pasożyta, które unieszkodliwia tnące enzymy
Wiele organizmów, w tym ludzie, produkuje rodzinę białek zwanych cystatynami, które działają jak blokady bezpieczeństwa dla silnych enzymów trawiących — cysteinowych proteaz. Te enzymy rozcinają inne białka i biorą udział w takich procesach jak usuwanie zużytych elementów komórkowych czy uruchamianie reakcji odpornościowych. Pasożyty nauczyły się wytwarzać własne białka podobne do cystatyn, aby zakłócać działanie enzymów gospodarza i modulować jego układ odpornościowy. W tej pracy badacze zidentyfikowali u E. multilocularis białko podobne do cystatyny i nazwali je EmCystatin-B. Stwierdzili, że gen EmCystatin-B jest znacznie bardziej aktywny w dojrzałych głowach larwalnych (protoskoleksach) niż w otaczającej tkance torbieli, a białko lokalizuje się w cytoplazmie i jądrze komórek pasożyta, zwłaszcza w dzielących się, „macierzystych” komórkach germinatywnych. Badania laboratoryjne wykazały, że EmCystatin-B silnie blokuje aktywność ludzkiej katepsyny B — ważnej cysteinowej proteazy zaangażowanej w odporność i przebudowę tkanek.
Znany kształt z niespodziewanym obrotem
Aby dokładnie poznać budowę EmCystatin-B, zespół skrystalizował oczyszczone białko i zastosował krystalografię rentgenowską, rozwiązując trójwymiarową strukturę z niemal atomową rozdzielczością. Podobnie jak inne cystatyny, każda jednostka EmCystatin-B ma charakterystyczny kształt: centralny segment helikalny wsparty kilkoma płaskimi, wstęgowymi β‑strukturalnymi elementami, tworząc klin, który normalnie pasuje do centrum aktywnego proteazy. Na podstawie sekwencji i braku oczywistego peptydu sygnałowego dla sekrecji, EmCystatin-B należy do podgrupy „stefin” — zwykle małych, wewnątrzkomórkowych cystatyn pozbawionych stabilizujących mostków dwusiarczkowych. Ku zaskoczeniu, struktura ujawniła, że chociaż poszczególne jednostki EmCystatin-B mają przewidywane złożenie, sposób ich łączenia jest nietypowy i specyficzny dla gatunku w porównaniu z ludzką cystatyną B.
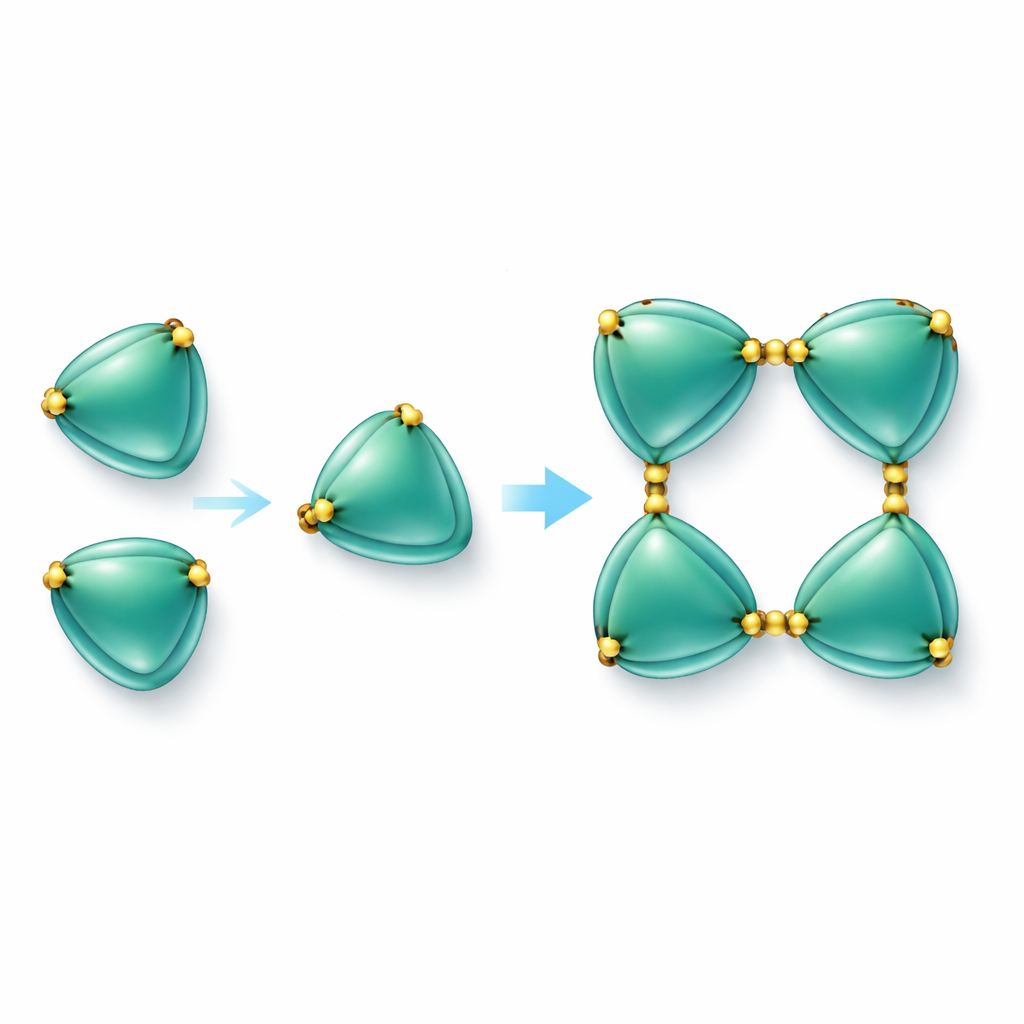
Budowanie łańcuchów białkowych za pomocą siatek siarczkowych
Najbardziej uderzającym odkryciem było to, że cząsteczki EmCystatin-B nie występują jedynie jako pojedyncze monomery. Zamiast tego mogą łączyć się stopniowo, tworząc dimery (pary), a następnie tetramery (grupy po cztery). Dwa różne mechanizmy wspierają tworzenie początkowych dimerów. W jednym przypadku część jednej cząsteczki „przechodzi” nad sąsiadem i dopełnia jego strukturę — zjawisko znane jako wymiana domen (domain swapping). W drugim przypadku pary cząsteczek są spajane mostkami dwusiarczkowymi — silnymi wiązaniami chemicznymi między aminokwasami zawierającymi siarkę (cysteinami). W EmCystatin-B cysteina na pozycji 4 jednej cząsteczki łączy się z cysteiną na pozycji 76 partnera. Cztery takie międzycząsteczkowe wiązania stabilizują następnie tetramer. Zastosowanie wielu wiązań dwusiarczkowych między cząsteczkami jest zjawiskiem całkowicie nowym dla klasycznych stefin, które zwykle takich mostków nie posiadają. Gdy badacze zastąpili te kluczowe cysteiny innymi aminokwasami, białko przestało efektywnie składać się w wyższe kompleksy, a jego zdolność hamowania katepsyny B znacznie spadła.
Co to oznacza dla walki z zakażeniem
Dla nietechnicznego czytelnika przekaz jest taki: pasożyt wyewoluował szczególnie „uzbrojoną” wersję powszechnego rodzaju białek, wykorzystując dodatkowe chemiczne „nitowania”, aby zablokować kilka jednostek inhibitory razem. Forma oligomeryczna wydaje się ważna dla unieszkodliwienia enzymu gospodarza, który w przeciwnym razie pomagałby w kontroli infekcji. Odkrycie dokładnej architektury EmCystatin-B i jej unikatowych zespołów połączonych mostkami dwusiarczkowymi poszerza nasze rozumienie, jak cystatyny mogą być dostrajane między gatunkami. W dłuższej perspektywie te wnioski mogą ukierunkować projekt leków, które albo zablokują ochronne działanie EmCystatin-B na pasożyta, albo będą naśladować jego właściwości łagodzące odpowiedź immunologiczną w leczeniu chorób zapalnych.
Cytowanie: Hong, W., Cheng, Z., Xu, Z. et al. Crystal structure of Echinococcus multilocularis cystatin B reveals a novel feature in classical stefins. Sci Rep 16, 5114 (2026). https://doi.org/10.1038/s41598-026-35060-0
Słowa kluczowe: alveolarna echinokokoza, Echinococcus multilocularis, cystatyna B, struktura białka, modulacja odporności