Clear Sky Science · pl
Zakłócenie montażu inflamasomu NLRP3 poprzez remodelowanie interfejsów domeny pirynowej indukowane ligandem
Dlaczego ważne jest stłumienie wymykającego się spod kontroli stanu zapalnego
Wiele chorób przewlekłych — od zapalenia stawów i dny moczanowej po choroby serca i neurodegenerację — napędzanych jest przez nadmiernie aktywny wewnątrzkomórkowy system alarmowy odporności. Kluczową częścią tego alarmu, zwanym inflamasomem NLRP3, jest pomoc w zwalczaniu infekcji, ale może też wywoływać szkodliwe zapalenie, gdy działa nieprawidłowo. W tym badaniu opisano nową małą cząsteczkę nazwaną E9, która celuje w wczesny krok aktywacji NLRP3, oferując nową perspektywę projektowania leków łagodzących szkodliwe zapalenie bez całkowitego wyłączania układu odpornościowego.
Komórkowy alarm pożarowy z mroczną stroną
Gdy w organizmie pojawia się zagrożenie, komórki odpornościowe składają inflamasom NLRP3 — duży kompleks białkowy działający jak molekularny alarm pożarowy. Po utworzeniu ta struktura aktywuje enzym zwany kaspazą-1, który z kolei uruchamia silne mediatory zapalenia, w tym cytokiny IL-1β i IL-18. Sygnały te są niezbędne do zwalczania infekcji i usuwania uszkodzonych tkanek. Jednak jeśli inflamasom pozostaje aktywny zbyt długo lub włącza się w niewłaściwym momencie, przyczynia się do przewlekłych stanów zapalnych obejmujących stawy, naczynia krwionośne, mózg i inne narządy. Dlatego badacze na całym świecie poszukują precyzyjnych metod kontrolowania NLRP3 bez szerokiego tłumienia odporności.
Patrząc poza zwykłe cele leków
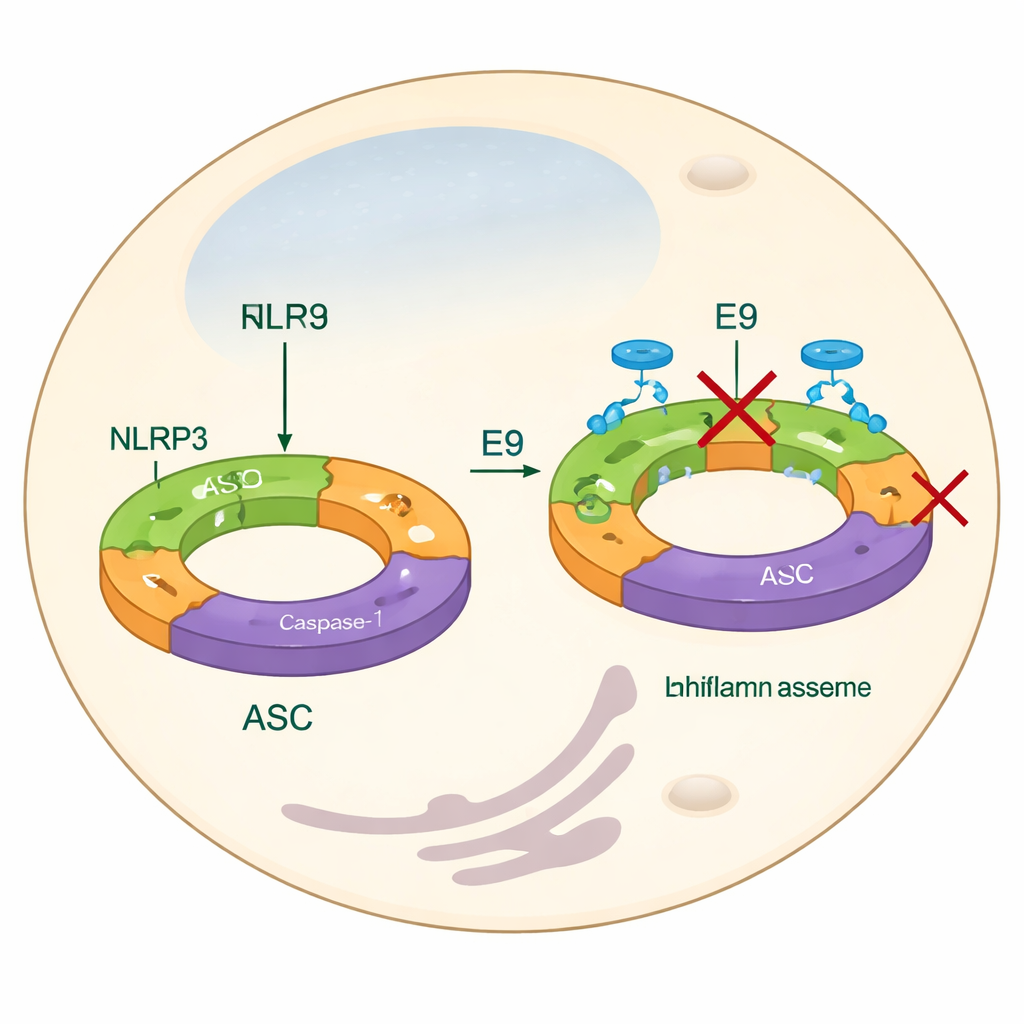
Większość obecnych strategii tłumienia NLRP3 koncentruje się na blokowaniu jego produktów końcowych — jak IL-1β — lub na zakłócaniu centralnej, „silnikowej” domeny wykorzystującej cząsteczki energii, takie jak ATP. Chociaż te podejścia mogą działać, mogą nie obejmować najwcześniejszych etapów składania i nie wyjaśniają w pełni, jak białka NLRP3 łączą się, tworząc funkcjonalną maszynę. W tej pracy autorzy skupiają się zamiast tego na domenie pirynowej, części NLRP3, która pomaga pojedynczym jednostkom łączyć się w długie filamenty. Filamenty te następnie rekrutują inny białkowy adaptor, ASC, który aglomeruje w jasne „kropki” wewnątrz komórek — widoczny znak aktywacji inflamasomu. Znalezienie związków chemicznych, które uniemożliwiają prawidłowe dopasowanie domen pirynowych, ma na celu powstrzymanie tworzenia inflamasomu od samego początku.
Znalezienie cząsteczki, która przerywa łańcuch
Badacze przesiewali bibliotekę 1500 nowo syntezowanych małych cząsteczek za pomocą sprytnego testu opartego na świetle. Połączyli rozdzielone fragmenty enzymu lucyferazy z domeną pirynową NLRP3; gdy dwie domeny pirynowe się łączyły, fragmenty enzymu ponownie się składały i emitowały światło. Związki blokujące kontakt piryna–piryna powodowały spadek sygnału świetlnego. Z tego przesiewu wyłoniono cztery obiecujące kandydaty, z których jeden — E9 — wyróżniał się silną i spójną inhibicją. Dalsze pomiary techniką mikroskalowej termoforezy wykazały, że E9 wiąże się mocno z domeną pirynową w bardzo niskich (submikromolowych) stężeniach, potwierdzając, że jego efekt nie był przypadkowym artefaktem, lecz wynikiem specyficznej interakcji.
Obserwacja efektu w żywych komórkach
Aby sprawdzić, czy E9 działa także w systemie żywym, zespół wykorzystał ludzkie komórki o cechach odpornościowych zmodyfikowane genetycznie do wytwarzania fluorescencyjnej wersji ASC. Gdy komórki te są stymulowane składnikami bakteryjnymi i drugim bodźcem, NLRP3 włącza się, a białka ASC grupują się w jasne kropki, które można zliczyć pod mikroskopem. W obecności E9 liczba tych kropek znacząco spadła, porównywalnie lub lepiej niż w przypadku niektórych znanych blokerów NLRP3. Pokazuje to, że zakłócenie kontaktów domen pirynowych wystarcza, by zmniejszyć składanie inflamasomu i wczesne etapy zapalnego obumierania komórek, przynajmniej w warunkach laboratoryjnych.
Jak E9 przekształca szkielet inflamasomu
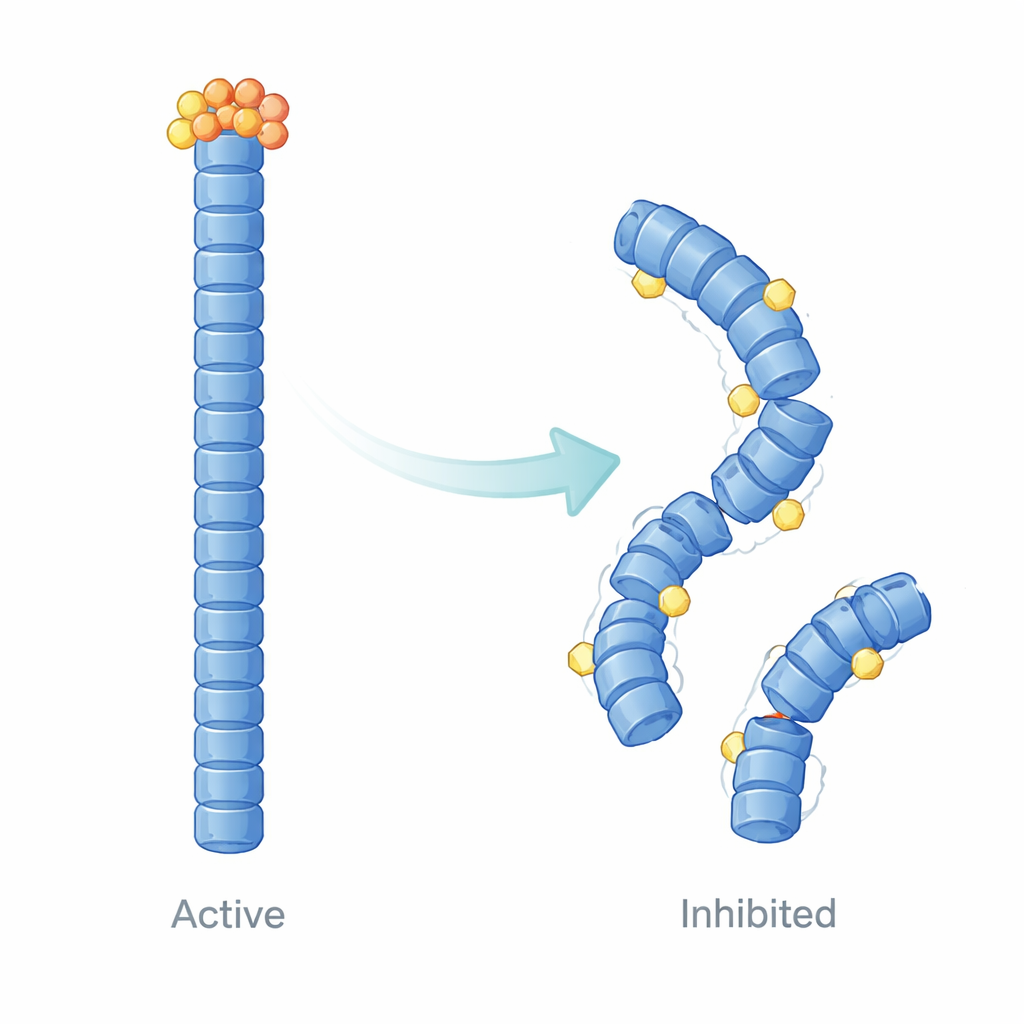
Ponad samo pomiar wiązania, autorzy użyli komputerowego modelowania strukturalnego i symulacji dynamiki molekularnej, by zwizualizować, jak E9 zmienia zachowanie filamentów NLRP3 w czasie. Ich obliczenia sugerują, że E9 osadza się na określonych powierzchniach kontaktowych, gdzie domeny pirynowe się stykają, subtelnie poluzowując i przekształcając filament. Zamiast jednolicie stabilnej, kooperatywnej struktury, filament staje się niejednorodny: regiony w pobliżu związanych cząsteczek E9 stają się bardziej elastyczne i tracą precyzyjne wyrównanie, podczas gdy inne części ulegają dynamicznej izolacji. Te zmiany tłumią ruchy na dużą skalę i ścisłą komunikację potrzebną do skutecznej rekrutacji ASC, dostarczając fizycznego wyjaśnienia obserwowanego w komórkach zmniejszenia formowania kropek.
Co to może znaczyć dla przyszłych terapii
Podsumowując, wyniki przedstawiają E9 jako prototyp nowej klasy leków celujących w inflamasom, działających przez zaburzanie interfejsów między elementami budulcowymi NLRP3, zamiast blokować jego wykorzystanie energii czy produkty końcowe. Choć obecne prace ograniczają się do testów in vitro, symulacji komputerowych i hodowli komórkowych — i potrzebne są dalsze badania na zwierzętach i ludziach — wykazano, że starannie zaprojektowane małe cząsteczki mogą remodelować sam szkielet inflamasomu. Dla pacjentów z chorobami napędzanymi przez wymykające się spod kontroli zapalenie, leki skupione na interfejsach mogłyby kiedyś zaoferować bardziej precyzyjną kontrolę, przyciszając szkodliwą aktywację odporności przy zachowaniu istotnych mechanizmów obronnych.
Cytowanie: Khosravifard, S., Hosseinkhani, S., Bakhtiary, N. et al. Disruption of NLRP3 inflammasome assembly via ligand-induced remodeling of pyrin domain interfaces. Sci Rep 16, 4951 (2026). https://doi.org/10.1038/s41598-026-35050-2
Słowa kluczowe: inflamasom NLRP3, domena pirynowa, inhibitor małocząsteczkowy, odporność wrodzona, piroptoza