Clear Sky Science · pl
TTF2 jako potencjalny biomarker i cel immunoterapii w diagnozie i prognozowaniu glejaka
Dlaczego to badanie nowotworów mózgu ma znaczenie
Guzy mózgu zwane glejakami należą do najbardziej śmiertelnych nowotworów — większość pacjentów żyje zaledwie kilka lat po rozpoznaniu. Lekarze pilnie potrzebują lepszych metod przewidywania przebiegu choroby oraz nowych celów leczenia, zwłaszcza dla nowoczesnych terapii opartych na układzie odpornościowym. W tym badaniu skupiono się na mało znanej cząsteczce, TTF2, i postawiono proste pytanie o dalekosiężnych konsekwencjach: czy poziomy TTF2 w guzach mózgu mogą pomóc w dokładniejszym rozpoznaniu glejaka, prognozowaniu przeżycia i ukierunkowaniu przyszłej immunoterapii?
Nowy sygnał ukryty w genach guza
Glejaki nie są jednorodną chorobą, lecz grupą guzów mózgu różniących się tempem wzrostu i reakcją na leczenie. Obecne narzędzia, takie jak badanie mikroskopowe i kilka markerów genetycznych, nie wyjaśniają w pełni, dlaczego niektórzy pacjenci mają lepsze rokowania, a inni szybko się pogarszają. Naukowcy sięgnęli do dużych, publicznych baz danych genetycznych z USA i Chin, aby poszukać dodatkowych wskazówek molekularnych. Skoncentrowali się na TTF2, białku uczestniczącym w wyłączaniu aktywności genów, które było powiązane z kilkoma innymi nowotworami, lecz nie było dogłębnie badane w kontekście glejaka.
Wysokie TTF2, wyższe ryzyko
Porównując tysiące próbek, zespół odkrył, że poziomy TTF2 są znacznie wyższe w tkance glejaka niż w normalnym mózgu. W obrębie glejaków guzy z najwyższym TTF2 miały tendencję do większego zaawansowania, należały do agresywniejszych podtypów i były częściej wykrywane u starszych pacjentów. Śledząc wyniki chorych, badacze zauważyli wyraźny wzorzec: osoby, których guzy zawierały więcej TTF2, miały z reguły krótsze całkowite przeżycie i częstszy postęp choroby. Nawet po uwzględnieniu silnych istniejących markerów, takich jak stopień guza, status mutacji IDH czy delecja 1p/19q, TTF2 pozostał niezależnym czynnikiem prognostycznym. Grupa opracowała wykres predykcyjny łączący TTF2 z tymi standardowymi czynnikami, który dobrze odzwierciedlał rzeczywiste przeżycia po jednym, trzech i pięciu latach w dwóch odrębnych zestawach danych pacjentów.
Wskazówki z otoczenia guza
Aby zrozumieć, dlaczego TTF2 może wiązać się ze złym rokowaniem, badacze przeanalizowali, które inne geny zmieniają swój poziom wraz z nim oraz jakie procesy biologiczne reprezentują te zestawy genów. Guzy z wysokim TTF2 wykazywały silniejszą aktywność szlaków związanych z sygnalizacją immunologiczną, produkcją przeciwciał i komunikacją międzykomórkową, a także w dobrze poznanych drogach nowotworowych, takich jak PI3K–AKT. Wykorzystując narzędzia obliczeniowe wnioskające o składzie komórek odpornościowych na podstawie wzorców ekspresji genów, przeanalizowano mikrośrodowisko guza. Glejaki bogate w TTF2 były również bogate w pewne komórki odpornościowe — limfocyty pomocnicze Th2, makrofagi i neutrofile — które często kojarzą się z „stłumioną” odpowiedzią przeciwnowotworową, oraz miały mniej komórek dendrytycznych plazmacytoidalnych, które mogą pobudzać silniejszą odporność.
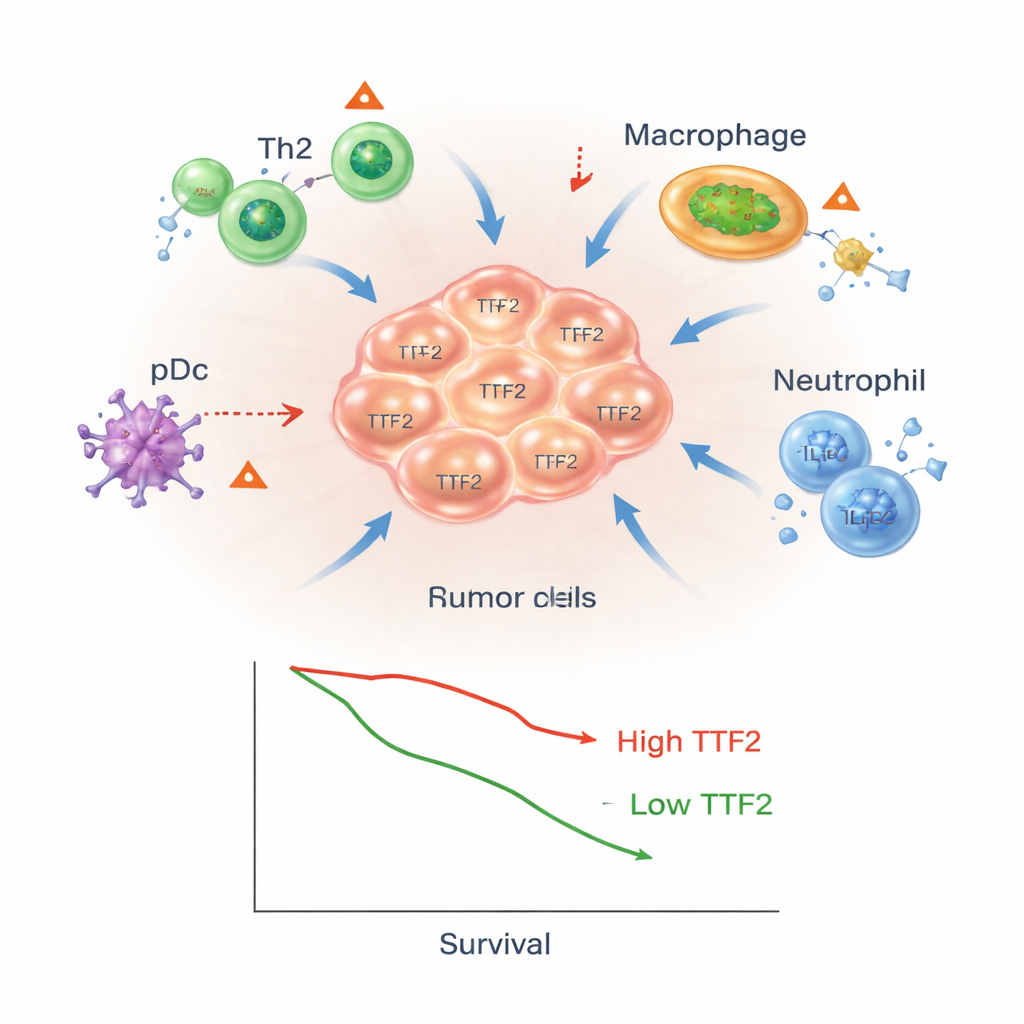
W jaki sposób TTF2 może pomagać guzom się ukrywać
Wyniki sugerują, że TTF2 robi więcej niż tylko oznacza agresywne guzy; może aktywnie pomagać w tworzeniu ochronnej osłony wokół nich. Autorzy proponują, że poprzez wpływ na sposób wyłączania genów, TTF2 mógłby zmieniać poziomy kluczowych przekaźników immunologicznych i chemokin — cząsteczek przyciągających lub odpychających komórki odpornościowe. To z kolei mogłoby kierować limfocyty w stronę stanu zdominowanego przez Th2, który jest mniej skuteczny w zabijaniu komórek nowotworowych, oraz sprzyjać gromadzeniu makrofagów i neutrofili wspierających guz. Chociaż te idee wynikają z analizy danych, a nie z bezpośrednich manipulacji laboratoryjnych TTF2, stanowią testowalny model tego, jak ta cząsteczka mogłaby promować wzrost guza i ucieczkę przed układem odpornościowym.
Co to oznacza dla pacjentów
Badanie konkluduje, że TTF2 jest silnie przewyrażany w glejakach, a jego wyższe poziomy wiążą się konsekwentnie z gorszym przeżyciem i bardziej agresywnymi cechami choroby. Dla pacjentów otwierają się dzięki temu dwie obiecujące perspektywy. Po pierwsze, mierzenie TTF2 w próbkach guza mogłoby pomóc lekarzom w precyzyjniejszym rozpoznaniu i spersonalizowaniu oceny ryzyka ponad to, co dają dziś standardowe badania. Po drugie, jeśli przyszłe prace laboratoryjne potwierdzą, że TTF2 pomaga guzom unikać układu odpornościowego, leki blokujące lub modulujące TTF2 — albo jego szlaki efektorowe — mogłyby stać się częścią nowych terapii skojarzonych, które zwiększą skuteczność immunoterapii u osób z tym wyniszczającym rakiem mózgu.
Cytowanie: Shi, D., Chen, F., Chen , Z. et al. TTF2 as a potential biomarker and immunotherapy target in glioma diagnosis and prognosis. Sci Rep 16, 7653 (2026). https://doi.org/10.1038/s41598-026-35049-9
Słowa kluczowe: glejak, TTF2, marker nowotworu mózgu, mikrośrodowisko immunologiczne guza, cel immunoterapii