Clear Sky Science · pl
Oś miR-181d-5p/SPP1 hamuje migrację i inwazję raka jelita grubego poprzez szlak RhoA
Dlaczego te badania mają znaczenie dla zdrowia codziennego
Rak jelita grubego jest jednym z najczęstszych i najbardziej śmiertelnych nowotworów na świecie, głównie dlatego, że często rozprzestrzenia się do innych części ciała zanim zostanie wykryty. W tym badaniu przyglądamy się niewielkiemu regulatorowi genetycznemu — mikroRNA nazwanemu miR-181d-5p — które działa jak naturalny hamulec ograniczający zdolność komórek raka jelita grubego do przemieszczania się i inwazji. Zrozumienie, jak działa ten wbudowany hamulec, może otworzyć drogę do nowych metod spowalniania rozprzestrzeniania się guza i poprawy przeżywalności.
Małe RNA o dużej ochronnej roli
MikroRNA to bardzo krótkie fragmenty RNA, które same nie kodują białek, lecz subtelnie regulują włączanie i wyłączanie innych genów. Rodzina miR-181 była powiązana z nowotworami w wielu narządach. W tym badaniu autorzy stwierdzili, że jeden z członków tej rodziny, miR-181d-5p, jest znacznie obniżony w ludzkich tkankach raka jelita grubego oraz w kilku liniach komórkowych raka jelita w porównaniu z sąsiednią tkanką nie-nowotworową i normalnymi komórkami jelitowymi. Taki wzorzec sugeruje, że w warunkach zdrowych miR-181d-5p pomaga utrzymać wzrost i ruch komórek w ryzach, a jego utrata może dawać komórkom nowotworowym większą swobodę rozprzestrzeniania się.
Jak hamulec wpływa na zachowanie komórek nowotworowych
Aby sprawdzić, co miR-181d-5p faktycznie robi, zespół sztucznie podniósł jego poziom w jednej linii komórek raka jelita i obniżył go w innej. Kiedy miR-181d-5p był zwiększony, komórki nowotworowe rosły wolniej, wolniej zamykały „rany” przypominające zadrapania w hodowlach laboratoryjnych i miały mniejszą zdolność przechodzenia przez porowate membrany — trzy standardowe testy agresywności guza. Kiedy poziom mikroRNA został obniżony, wszystkie te zachowania przyspieszyły. Komórki zmieniały też kształt: wyższy poziom miR-181d-5p powodował, że były bardziej zaokrąglone z osłabionym wewnętrznym szkieletem, natomiast niższe poziomy dawały komórki wydłużone z silnymi włóknami napięcia (stress fibers), formą lepiej przystosowaną do przemieszczania się po organizmie.
Kluczowy białkowy cel w rozprzestrzenianiu się nowotworu
Następnie badacze zapytali, którym genem kontroluje miR-181d-5p. Korzystając z predykcji komputerowych i testów reporterowych, wykazali, że to mikroRNA bezpośrednio przyłącza się do matrycy informacyjnej białka zwanego SPP1 (również znanego jako osteopontyna) i blokuje jego produkcję. SPP1 często występuje na wysokim poziomie w agresywnych nowotworach i jest znane z promowania ruchu i przeżycia komórek. W próbkach pacjentów i liniach komórkowych SPP1 było podwyższone tam, gdzie miR-181d-5p było niskie, ujawniając odwrotną zależność między nimi. Zmiany poziomów miR-181d-5p w komórkach nowotworowych powodowały odpowiednie wzrosty lub spadki SPP1, wraz z regulatorem dalszym o nazwie RhoA, który przebudowuje wewnętrzny szkielet komórki i pomaga jej pełzać.
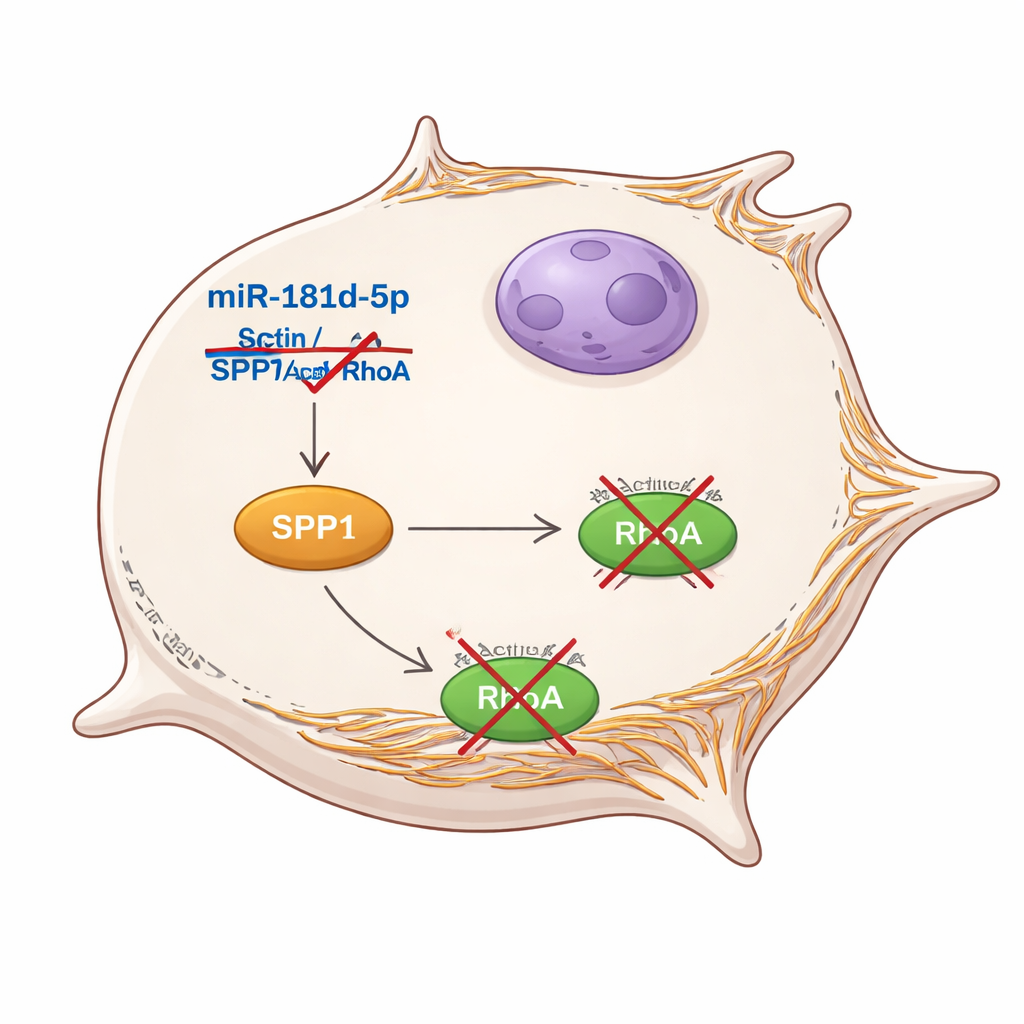
Rozplątywanie szlaku, który napędza inwazję
W dalszej kolejności autorzy bezpośrednio manipulowali SPP1. W komórkach o wysokim SPP1 wzrastały wzrost, ruch i inwazja, a markery molekularne przesuwały się w stronę bardziej mobilnego, mniej przyczepnego stanu. Gdy SPP1 zostało wyciszone, następowała odwrotna zmiana. Co kluczowe, gdy podnieśli miR-181d-5p, ale jednocześnie zmusili komórki do wytwarzania dodatkowego SPP1, wiele korzyści płynących z mikroRNA zostało utraconych. Ten eksperyment „uratowania” (rescue) pokazuje, że miR-181d-5p hamuje komórki raka jelita grubego w dużej mierze przez utrzymanie SPP1 — a w konsekwencji szlaku RhoA — pod kontrolą. W modelach myszich guzy powstałe z komórek bogatych w miR-181d-5p rosły wolniej, wykazywały mniej oznak agresywnych zmian tkankowych i miały niższe poziomy SPP1, RhoA oraz markera podziału komórkowego Ki-67.
Co to może oznaczać dla przyszłych terapii
Prosto mówiąc, to badanie identyfikuje łańcuch dowodzenia w raku jelita grubego: mikroRNA miR-181d-5p działa jako główny przełącznik, który wycisza SPP1, co z kolei uspokaja system RhoA pomagający komórkom nowotworowym zmieniać kształt i rozprzestrzeniać się. Gdy ten ochronny mikroRNA jest utracony, SPP1 i RhoA stają się nadaktywne, a guzy rosną i invade łatwiej. Chociaż przed zastosowaniem tych odkryć w terapii wciąż daleka droga, przywrócenie miR-181d-5p lub blokowanie SPP1 mogłoby pewnego dnia stać się strategią spowalniania lub zapobiegania przerzutom raka jelita grubego i poprawy wyników leczenia pacjentów.
Cytowanie: Hou, S., Guo, T., Wu, J. et al. The miR-181d-5p/SPP1 axis inhibits the migration and invasion of colorectal cancer via the RhoA patyway. Sci Rep 16, 4883 (2026). https://doi.org/10.1038/s41598-026-35040-4
Słowa kluczowe: rak jelita grubego, microRNA, przerzuty, SPP1, sygnalizacja RhoA