Clear Sky Science · pl
Aktywacja CD13 tworzy kompleksy sygnalizacyjne fosfoinozytydów (PI), które regulują cytoszkielet aktynowy
Komórki sięgające, by pomóc sąsiadom
Kiedy tkanki są uszkodzone lub poddane stresowi, komórki muszą szybko komunikować się, by zdecydować, czy naprawiać się, przemieścić, czy nawet zainicjować śmierć. Badanie to ujawnia, jak mało znane białko powierzchniowe, o nazwie CD13, pomaga komórkom budować długie, cienkie pomosty, które fizycznie łączą odległe komórki. Przez te mosty komórki mogą przesyłać sygnały, takie jak fale wapniowe, potencjalnie koordynując przeżycie i naprawę w obrębie uszkodzonej tkanki.
Żywe mosty komórkowe pod wpływem stresu
Naukowcy pracowali z ludzkimi komórkami wywodzącymi się z mięsakopodobnego nowotworu Kaposiego, rodzaju guza, którego komórki chętnie tworzą wypustki w trudnych warunkach, takich jak brak składników odżywczych czy wysokie stężenie cukru. Pod wpływem stresu komórki normalne tworzyły wiele długich, uniesionych wypustek błonowych bogatych w aktynę — białko strukturalne kształtujące komórki. Te wypustki unosiły się nad powierzchnią i rozciągały na znaczne odległości, łącząc komórki, które się nie stykały. Gdy naukowcy genetycznie usunęli CD13, komórki wytwarzały znacznie mniej i krótsze wypustki, które pozostawały blisko powierzchni. Pokazało to, że CD13 jest niezbędne do budowy tych imponujących połączeń międzykomórkowych.
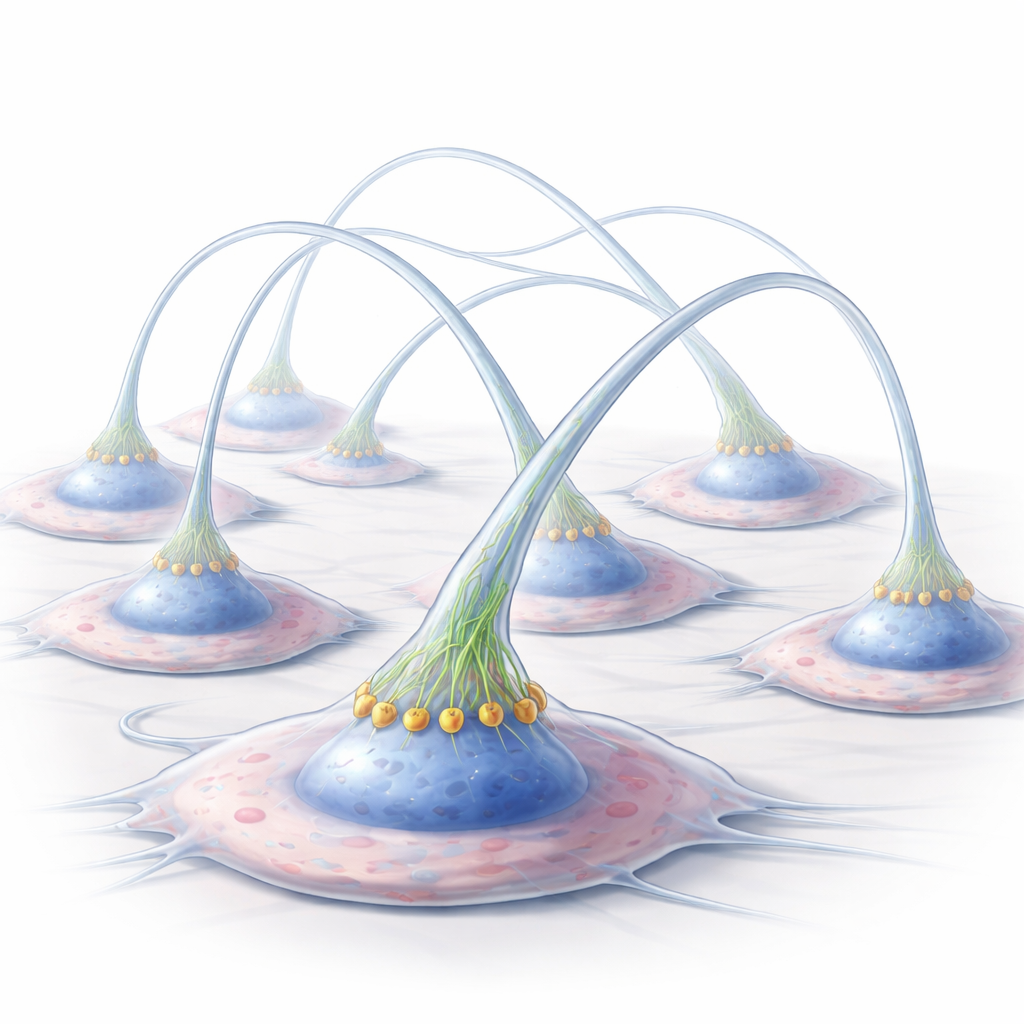
Włączenie komórkowego majstra budowy
CD13 znajduje się w zewnętrznej błonie komórkowej, ale ma króciutki ogonek wewnątrz komórki. Zespół użył specjalnego przeciwciała, które grupuje i „włącza” CD13, naśladując silną aktywację. To działanie znacząco zwiększyło powstawanie wypustek w komórkach normalnych, ale nie miało efektu, gdy CD13 było nieobecne lub gdy użyto przeciwciała nieaktywującego. Zablokowanie aktywności enzymatycznej CD13 także nie miało znaczenia, co wskazuje, że jego rola tutaj polega na funkcjonowaniu jako centrum sygnalizacyjnego, a nie jako enzym rozcinający białka. Gdy naukowcy wprowadzili krótki peptyd zaprojektowany, by blokować interakcje przy wewnętrznym ogonku CD13, powstawanie wypustek zmalało, mimo że CD13 wciąż znajdowało się na powierzchni. Razem te wyniki pokazują, że CD13 działa jak majster budowy: po aktywacji gromadzi odpowiednią załogę białek przy błonie, by wypychać powierzchnię komórki na zewnątrz.
Od lipidów i białek do rosnących wypustek
Wewnątrz komórki CD13 przyciąga kilka kluczowych elementów sygnalizacyjnych, w tym kinazy Src i FAK, rusztowanie IQGAP1 oraz małą GTPazę ARF6. Molekuły te regulują zarówno szkielet aktynowy, jak i skład błony. Badanie pokazuje, że po aktywacji CD13 pomaga rekrutować ten kompleks białkowy do określonych miejsc, gdzie uruchamia kolejny enzym, PIP5K. PIP5K wytwarza lipid sygnalizacyjny zwany PI(4,5)P2 bezpośrednio w błonie. PI(4,5)P2 jest silnym organizatorem: wiąże białka regulujące aktynę i sprzyja polimeryzacji aktyny, co fizycznie napędza powstawanie wypustek błonowych. Autorzy stwierdzili, że PI(4,5)P2, CD13 i aktyna gromadzą się u podstawy oraz wzdłuż tych struktur, ujawniając ściśle skoordynowany mechanizm białkowo-lipidowy wypychający błonę na zewnątrz.
Komórkowe linie telefoniczne dla sygnałów wapniowych
Te zależne od CD13 wypustki robią więcej niż tylko efektownie wyglądać; zachowują się jak prywatne linie telefoniczne między komórkami. Używając barwnika raportującego poziom wapnia, zespół mechanicznie stymulował jedną komórkę i obserwował falę wzrostu wapnia w sąsiednich komórkach. W komórkach normalnych, bogatych w wypustki, sygnał wapniowy rozchodził się szybko i efektywnie do wielu połączonych komórek, nawet gdy zewnętrzny wapń był zablokowany. Natomiast komórki pozbawione CD13, a więc i solidnych wypustek, wykazywały znacznie słabsze rozprzestrzenianie się tego sygnału. Wypustki zawierały białko połączeń szczelinowych Connexin 43, które tworzy kanały między komórkami, co wspiera pogląd, że są to „zamknięte koniecowo rurki tunelowe” wyspecjalizowane w przekazywaniu sygnałów wewnętrznych, a nie w swobodnej wymianie materiału masowego.
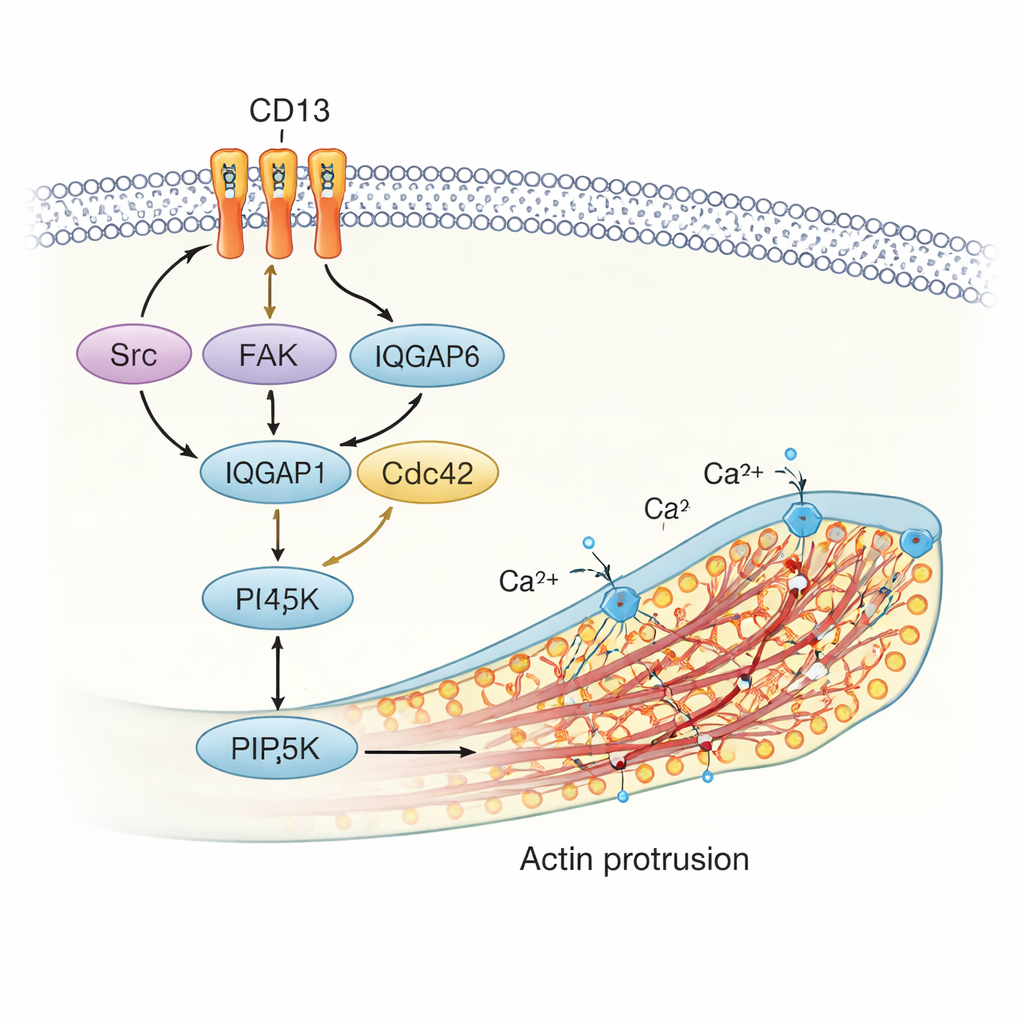
Dlaczego to ma znaczenie dla gojenia i chorób
Odkrywając, jak CD13 organizuje lokalne centrum sygnalizacyjne, by przekształcać szkielet aktynowy i lipidy błonowe, praca ta identyfikuje CD13 jako centralny przełącznik pomagający komórkom budować mosty komunikacyjne pod wpływem stresu. Dla laików kluczowa myśl jest taka, że komórki nie tylko krzyczą chemicznymi komunikatami do otoczenia; potrafią też układać fizyczne „kable”, by wysyłać celowane sygnały do odległych partnerów. Ponieważ CD13 jest bogato obecne i aktywowane w tkankach uszkodzonych i zapalnych, zrozumienie tej ścieżki może inspirować nowe strategie wspierające naprawę tkanek, ograniczające szkodliwe zapalenie lub nawet przerywające złą komunikację komórek nowotworowych w raku.
Cytowanie: Meredith, E., Aguilera, B., Sharma, R. et al. CD13 activation assembles phosphoinositide (PI) signaling complexes to regulate the actin cytoskeleton. Sci Rep 16, 5191 (2026). https://doi.org/10.1038/s41598-026-35022-6
Słowa kluczowe: komunikacja komórkowa, cytoszkielet aktynowy, wypustki błonowe, białko CD13, sygnalizacja fosfoinozytydowa