Clear Sky Science · pl
Profilowanie molekularne guza pierwotnego kontra sparowany, niesynchroniczny przerzut jasnokomórkowego raka nerki ujawnia heterogenność mikrośrodowiska immunologicznego guza
Dlaczego to badanie raka nerki ma znaczenie
Rak nerki często rozsiewa się do innych części ciała, a współczesne immunoterapie nie działają jednakowo dobrze u wszystkich pacjentów ani wobec każdego guza. W tym badaniu przyjrzano się bliżej jasnokomórkowemu rakowi nerkowemu — najczęstszemu podtypowi raka nerki — aby sprawdzić, jak układ odpornościowy zachowuje się inaczej w guzie pierwotnym w nerce w porównaniu z późniejszymi przerzutami. Zrozumienie tych różnic może pomóc wyjaśnić, dlaczego niektóre guzy lepiej reagują na leczenie niż inne, i może ukierunkować bardziej precyzyjną, spersonalizowaną opiekę.
Zajrzenie do guzów pierwotnych i przerzutów
Naukowcy skupili się na 19 pacjentach, u których usunięto guz nerkowy (guz pierwotny), a następnie rozwinęły się przerzuty w miejscach takich jak płuca, kości, wątroba, nadnercze, węzły chłonne czy tkanki miękkie. Od tych pacjentów zebrano 42 próbki guza: 19 guzów pierwotnych i 23 nieleczone przerzuty. Z cienkich skrawków zachowanej tkanki wyizolowano RNA — cząsteczkę odzwierciedlającą, które geny są aktywne — i zastosowano sekwencjonowanie wysokoprzepustowe, aby uchwycić aktywność genów w tysiącach genów w każdej próbce. 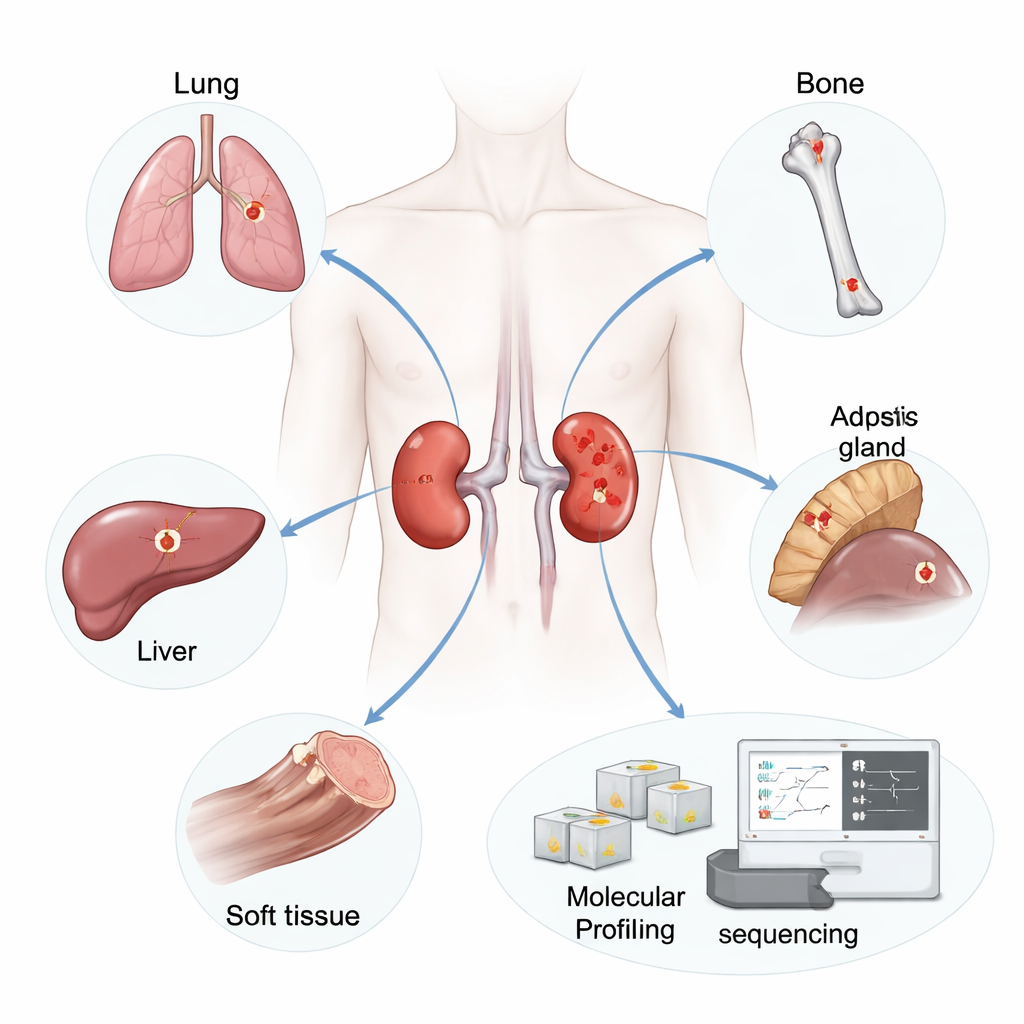
Guzy pierwotne i przerzutowe są molekularnie różne
Analiza wzorców aktywności genów wykazała, że guzy nerki pierwotne miały tendencję do grupowania się razem i były bardziej podobne do siebie nawzajem niż do własnych przerzutów. Innymi słowy, przerzut u danego pacjenta mógł różnić się bardziej od pierwotnego guza tego samego pacjenta niż od przerzutu innej osoby. Tysiące genów były bardziej lub mniej aktywne w przerzutach w porównaniu z guzami pierwotnymi. Guzy przerzutowe wykazywały silniejsze sygnały z programów genowych związanych z szybkim podziałem komórek i agresywnym zachowaniem, w tym szlaków uczestniczących w punktach kontrolnych cyklu komórkowego i produkcji białek. Natomiast guzy pierwotne były bardziej wzbogacone w szlaki odpowiedzi na stres i sygnalizacji, takie jak hipoksja (niskie stężenie tlenu) i sygnalizacja zapalna, co sugeruje różne presje biologiczne w nerce w porównaniu z odległymi narządami.
Lanscape immunologiczny zmienia się w miarę rozprzestrzeniania się raka
Ponad surową aktywnością genową, naukowcy oszacowali, jakie typy komórek odpornościowych były obecne w każdym guzie, używając metody obliczeniowej dekonwolucji danych RNA z tkanek całościowych. Odkryli uderzającą różnicę: guzy pierwotne nerki zawierały znacząco większy odsetek limfocytów T regulatorowych (Treg), rodzaju komórek odpornościowych tłumiących odpowiedź immunologiczną i mogących chronić guzy przed atakiem. W pierwotnych guzach było też więcej spoczynkowych komórek dendrycznych, monocytów, komórek NK oraz limfocytów CD8+. Natomiast przerzuty były bogatsze w tzw. makrofagi typu M2 — komórki odpornościowe często związane z gojeniem się ran i środowiskiem wspierającym guz, a nie gojącym go — wraz z większą liczbą komórek plazmatycznych i aktywowanych komórek dendrycznych. 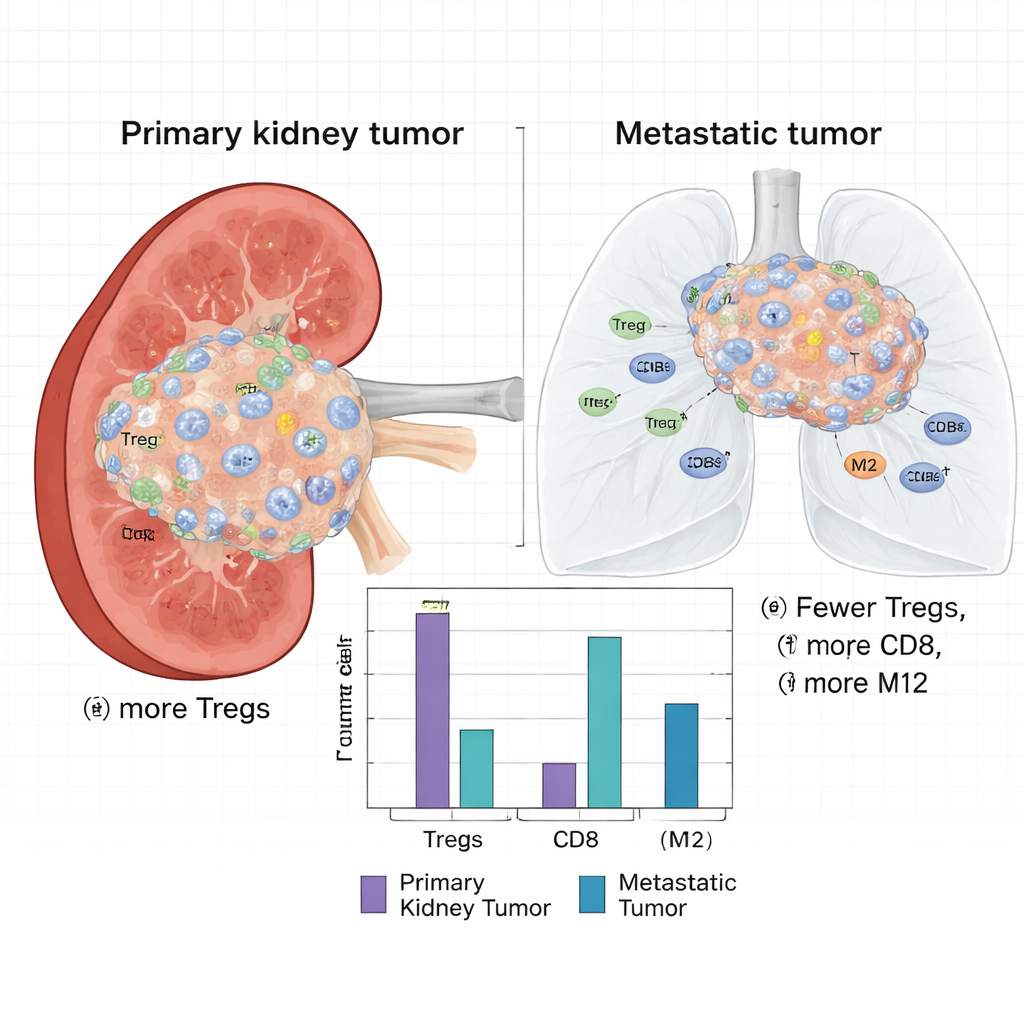
Przerzuty do płuc i kości opowiadają inne immunologiczne historie
Po przyjrzeniu się konkretnym miejscom przerzutów wyłoniły się istotne niuanse. Przerzuty do płuc wykazywały zwiększoną aktywność zestawów genów związanych z kontrolą podziału komórek (checkpoint G2M) i czynnikami transkrypcyjnymi E2F, a także wysoką ekspresję horneryny, białka powiązanego z tworzeniem naczyń krwionośnych w guzach. Ich dopasowane guzy pierwotne w nerce były bardziej wzbogacone w programy genowe związane z hipoksją i ponownie miały więcej Tregów. Z kolei przerzuty do kości wyróżniały się silniejszą aktywacją przejścia nabłonkowo-mezenchymalnego (EMT), procesu ułatwiającego komórkom rakowym zwiększoną ruchliwość i inwazyjność. Te zmiany kostne zawierały także wyższe poziomy makrofagów M2, podczas gdy guzy pierwotne, które dały początek tym przerzutom, wykazywały zwiększoną ekspresję HHLA2 — niedawno rozpoznanego białka punktu kontrolnego immunologicznego. Razem te obserwacje podkreślają, że środowiska immunologiczne i molekularne przerzutów nie tylko różnią się od pierwotnych guzów, lecz także różnią się między poszczególnymi miejscami przerzutów.
Równowaga komórek odpornościowych a rokowanie pacjentów
Aby zrozumieć, co te wzorce immunologiczne oznaczają dla pacjentów, zespół sięgnął do trzech dużych publicznych zestawów danych jasnokomórkowego raka nerki. Użyli tej samej metody obliczeniowej do oszacowania poziomów Tregów i limfocytów CD8+ i powiązali je z wynikami przeżycia. W przekrojach kohort osoby, których guzy miały kombinację niskich poziomów limfocytów CD8+ (głównych komórek zabijających raka) i wysokich poziomów Treg, miały gorsze wyniki pod względem przeżycia bez progresji lub przeżycia specyficznego dla choroby, nawet po uwzględnieniu wieku, stopnia złośliwości guza i zaawansowania. Choć ogólny etap choroby nadal silnie wpływał na przeżycie, równowaga między supresywnymi Tregami a atakującymi komórkami CD8+ wyłoniła się jako dodatkowy wskaźnik ryzyka.
Co to oznacza dla przyszłej opieki nad chorymi na raka nerki
Mówiąc prostym językiem, to badanie pokazuje, że guz pierwotny w nerce i jego przerzuty żyją w różnych immunologicznych „sąsiedztwach”. Guz pierwotny wydaje się szczególnie efektywny w rekrutowaniu komórek uspokajających układ odpornościowy, co może częściowo tłumaczyć, dlaczego guzy w miejscu pierwotnym często słabiej odpowiadają na immunoterapię niż ogniska przerzutowe. Przerzuty z kolei rozwijają własne lokalne systemy wsparcia, które różnią się w zależności od narządu. Te wnioski sugerują, że lekarze czasem mogą potrzebować pobrać próbki zarówno guza nerkowego, jak i przerzutów, aby w pełni zrozumieć chorobę pacjenta, oraz że terapie łączące inhibitory punktów kontrolnych z strategiami ukierunkowanymi na Tregi lub makrofagi M2 mogą poprawić wyniki u chorych z przerzutowym jasnokomórkowym rakiem nerkowokomórkowym.
Cytowanie: Cotta, B., Nallandhighal, S., Monda, S. et al. Molecular profiling of primary versus paired asynchronous metastatic clear cell renal cell carcinoma reveals heterogeneity in tumor immune microenvironment. Sci Rep 16, 5473 (2026). https://doi.org/10.1038/s41598-026-35021-7
Słowa kluczowe: rak nerki, mikrośrodowisko guza, immunoterapia, przerzut, limfocyty T regulatorowe