Clear Sky Science · pl
Strukturalne podstawy działania diosgeniny jako odwrotnego agonisty receptora bliźniaczego dla kwasu retinowego γ (RORγ)
Dlaczego związek roślinny i przełącznik immunologiczny mają znaczenie
Wiele przewlekłych chorób — od schorzeń autoimmunologicznych, takich jak stwardnienie rozsiane i łuszczyca, po otyłość i cukrzycę typu 2 — wynika z nadmiernie aktywnych sygnałów układu odpornościowego i zaburzonych wskazówek metabolicznych. Naukowcy od dawna poszukują bezpieczniejszych leków, które potrafią precyzyjnie wyregulować te sygnały. W tym badaniu zbadano, jak diosgenina, naturalna cząsteczka występująca w niektórych roślinach leczniczych i w jarmużu (yams), wiąże się z białkiem regulującym odporność o nazwie RORγ i przekształca je w stan mniej aktywny. Zrozumienie tej interakcji na poziomie atomowym może otworzyć drogę do łagodniejszych, bardziej ukierunkowanych terapii opartych na dobrze znanym naturalnym szkielecie molekularnym.
Główny regulator odporności i metabolizmu
RORγ należy do dużej rodziny „receptorów jądrowych” — białek wewnątrz komórek, które włączają lub wyłączają geny w odpowiedzi na małe cząsteczki. To konkretne białko jest kluczowym kontrolerem grupy komórek odpornościowych znanych jako komórki Th17, które produkują prozapalny sygnał IL-17A i wiążą się z chorobami autoimmunologicznymi, takimi jak stwardnienie rozsiane, łuszczyca, reumatoidalne zapalenie stawów i choroba Leśniowskiego-Crohna. RORγ wpływa także na rozwój adipocytów i reakcję organizmu na insulinę, co łączy go z otyłością i cukrzycą. Z uwagi na ten szeroki zakres działania, RORγ stał się atrakcyjnym celem terapeutycznym, ale wiele syntetycznych związków wiążących ten receptor napotkało problemy związane z bezpieczeństwem, selektywnością lub skutecznością u ludzi.
Tradycyjny środek źródłem obiecującego leku
Diosgenina to cząsteczka podobna do steroidów, wyizolowana z roślin, w tym gatunków z rodzaju Dioscorea (dziki jam) oraz kilku tradycyjnych ziół leczniczych. Była badana pod kątem właściwości przeciwzapalnych, przeciwnowotworowych, przeciwcukrzycowych i kardioprotekcyjnych w modelach komórkowych i zwierzęcych. Wcześniejsze prace sugerowały, że diosgenina może wpływać na szlak RORα/γ i hamować szkodliwe odpowiedzi Th17, ale nie było jasne, czy działa bezpośrednio na RORγ i w jaki sposób modyfikuje zachowanie białka. Aby to ustalić, autorzy przesiewali bibliotekę związków naturalnych używając czułego testu wiązania i zidentyfikowali diosgeninę jako silny ligand dla regionu wiążącego ligand RORγ.
Jak diosgenina cofa RORγ
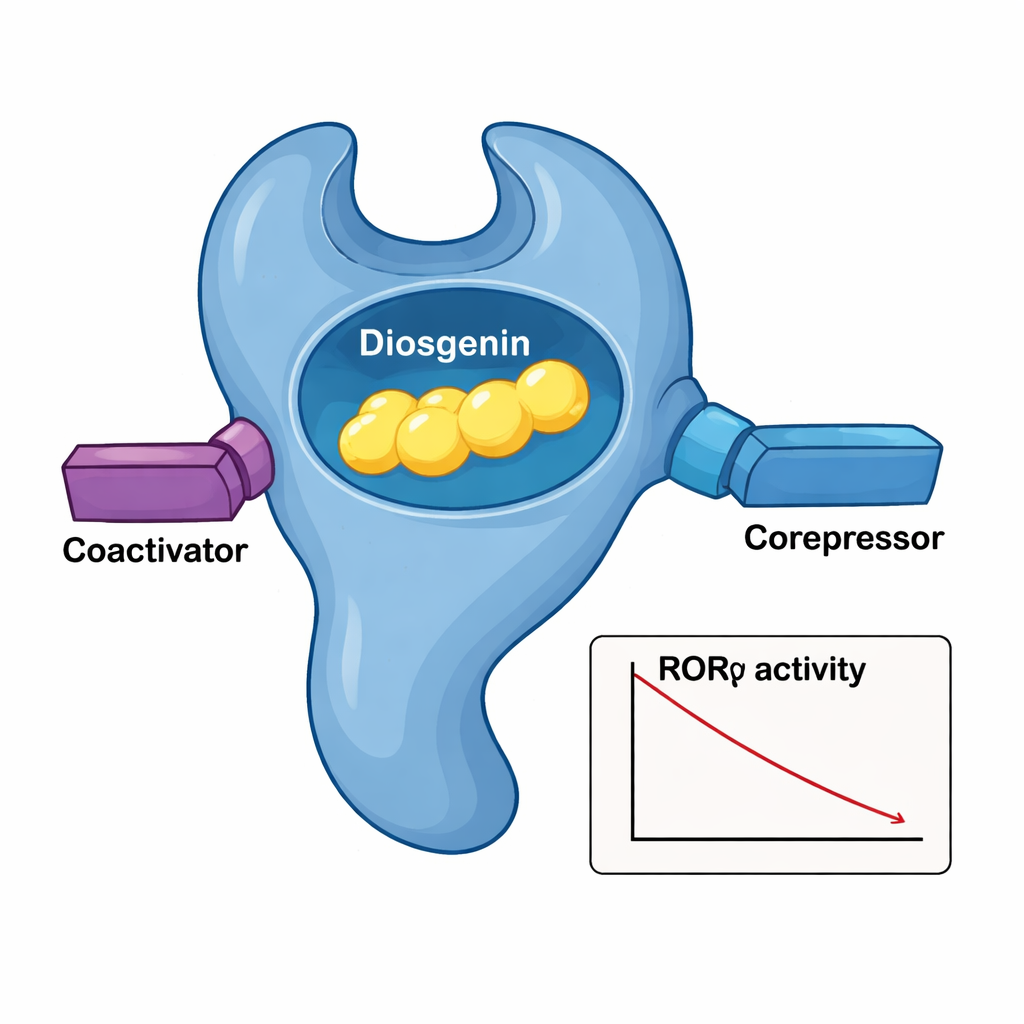
Naukowcy zbadali, jak diosgenina wpływa na zdolność RORγ do rekrutowania białek pomocniczych, które albo wzmacniają (koaktywatory), albo tłumią (korrepresory) aktywność genów. Ku zaskoczeniu, diosgenina sprzyjała wiązaniu się RORγ z obiema kategoriami partnerów, co różniło się od wzorca znanego naturalnego antagonisty o nazwie kwas ursolowy. W testach na komórkach, śledzących przełączanie genów, diosgenina systematycznie obniżała aktywność napędzaną przez RORγ w sposób zależny od dawki, z aktywnością w zakresie poniżej mikromolarnym. Takie zachowanie odpowiada profilowi „odwrotnego agonisty”: związku, który nie tylko blokuje aktywność podstawową, ale aktywnie wymusza stan wyłączenia receptora, nawet gdy normalnie byłby on aktywny.
Zbliżenie na molekularne uścisk dłoni
Aby zobaczyć, jak dokładnie diosgenina mieści się w RORγ, zespół rozwiązał trójwymiarową strukturę krystaliczną domeny wiążącej ligand receptoru z diosgeniną umieszczoną w środku. Receptor składa się z ułożonego w warstwy pęku helis tworzących kieszeń, która mieści steroidopodobne ciało diosgeniny. Sieć dopasowanych oddziaływań hydrofobowych z kilku aminokwasów działa jak dopasowana rękawica wokół szkieletu cząsteczki, podczas gdy krytyczna grupa hydroksylowa na diosgeninie tworzy pośredniczone przez wodę wiązania wodorowe z dwiema resztami argininy. Gdy te reszty kieszeni były modyfikowane pojedynczo, zdolność diosgeniny do wyciszania RORγ malała, potwierdzając ich znaczenie. Porównania strukturalne z kompleksem RORγ–kwas ursolowy wykazały, że diosgenina utrzymuje kluczową helisę ogonową (AF‑2) w pozycji przypominającej aktywną, mimo iż jednocześnie obniża łączną aktywność transkrypcyjną, co wyjaśnia, dlaczego może jednocześnie przyciągać koaktywatory i korrepresory.
Od struktury krystalicznej do przyszłych leków
Szczegółowy obraz interakcji diosgeniny z RORγ uwypukla dwie istotne zalety dla projektowania leków. Po pierwsze, kieszeń receptora wykazuje wystarczającą elastyczność, by rozpoznawać różne kształty ligandów, co oznacza, że chemicy mogą dopracować szkielet diosgeniny, aby zwiększyć selektywność wobec RORγ i zmniejszyć niepożądane wiązanie z innymi receptorami jądrowymi. Po drugie, naturalne pochodzenie diosgeniny i jej znana niska toksyczność w modelach przedklinicznych czynią ją atrakcyjnym punktem wyjścia w porównaniu z niektórymi całkowicie syntetycznymi związkami, które ugrzęzły w badaniach klinicznych. W prostych słowach, praca ta pokazuje, jak cząsteczka pochodzenia roślinnego może przyczepić się do centralnego przełącznika immunologicznego i metabolicznego i cofnąć jego działanie, oferując strukturalny wzorzec do opracowania bezpieczniejszych i skuteczniejszych terapii w chorobach związanych z RORγ.
Cytowanie: Chen, S., Tian, S., Liang, J. et al. Structural basis for diosgenin as an inverse agonist of retinoic acid receptor-related orphan receptor γ. Sci Rep 16, 4765 (2026). https://doi.org/10.1038/s41598-026-35006-6
Słowa kluczowe: ROR gamma, diosgenina, choroba autoimmunologiczna, receptor jądrowy, odwrotny agonista