Clear Sky Science · pl
Charakterystyka transkryptomiczna zaburzonego alternatywnego składania RNA w mięśniach szkieletowych pacjentów z sarkopenią
Dlaczego starzejące się mięśnie tracą siłę
Sarkopenia — stopniowa utrata masy i siły mięśniowej wraz z wiekiem — jest jednym z głównych powodów, dla których osoby starsze mają trudności z codziennymi czynnościami, od wchodzenia po schodach po noszenie zakupów. To badanie zagląda do wnętrza starzejącego się mięśnia na poziomie RNA, czyli komunikatów, które mówią komórkom, jakie białka mają produkować. Autorzy pokazują, że w sarkopenii wiele z tych komunikatów RNA jest wycinanych i składanych w nietypowy sposób, co może zaburzać produkcję energii w mięśniu i wskazywać nowe cele terapeutyczne.
Utrata mięśni a „edycja” genów w komórce
Nasze geny zapisane są w DNA, ale komórki pracują na kopiach tych genów — RNA. Zanim komunikat RNA zostanie użyty, komórki zazwyczaj przycinają i składają go — trochę jak montaż filmu — tak że jeden gen może dawać kilka wersji białka. Ten proces, zwany alternatywnym składaniem, jest szczególnie aktywny w mięśniach, które potrzebują precyzyjnie dostrojonych białek do kurczenia się, naprawy i adaptacji do wysiłku. Gdy składanie przebiega nieprawidłowo, powstają niewłaściwe wersje białek lub giną istotne warianty, co przyczynia się do chorób takich jak dystrofia mięśniowa czy niektóre zaburzenia mózgu. Autorzy przypuszczali, że podobna ukryta warstwa błędnej edycji RNA może napędzać sarkopenię.
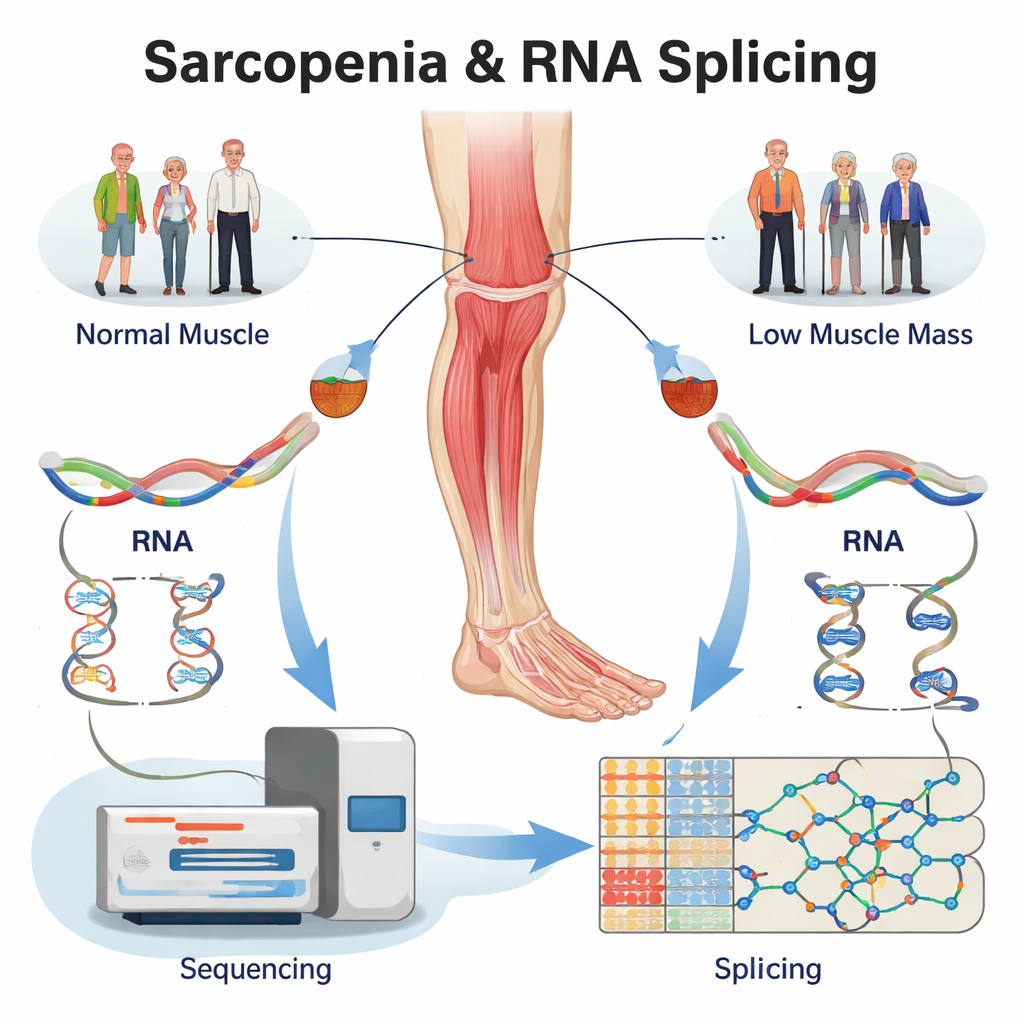
Ponowna analiza istniejących danych w poszukiwaniu ukrytych błędów RNA
Zamiast rekrutować nowych ochotników, zespół ponownie przeanalizował duży, istniejący zestaw danych z sekwencjonowania RNA z biopsji mięśni uda u ludzi. Próbki pochodziły z czterech grup: osób starszych z pełnoobjawową sarkopenią, osób z samą niską masą mięśniową, osób z samą niską siłą mięśniową oraz zdrowych kontroli dobranych wiekowo. Używając specjalistycznego oprogramowania, najpierw potwierdzili, że setki genów są w mięśniach chorych włączone lub wyłączone. Co ważniejsze, przeanalizowali następnie sposób, w jaki RNA każdego genu jest składane, katalogując ponad 5 000 zmian składania w trzech grupach problemowych w porównaniu ze zdrowymi mięśniami. Zmiany te koncentrowały się w kilku podstawowych typach — takich jak pomijanie eksonu czy wybór alternatywnego miejsca cięcia — wzorcach, które są znane z silnego wpływu na strukturę białek.
Zakłócenia w fabrykach energii i szlakach „czujnika paliwa” komórki
Zmiany składania pojawiły się w genach leżących u podstaw biologii mięśnia. Wiele z dotkniętych genów koduje elementy mitochondriów, drobnych fabryk energii, które napędzają skurcz mięśni. W mięśniach sarkopenicznych 16 genów zaangażowanych w fosforylację oksydacyjną — proces przekształcania składników odżywczych w użyteczną energię — wykazywało zmienione składanie, zwłaszcza elementów kompleksów mitochondrialnych odpowiedzialnych za transport elektronów i pompowanie protonów. Inne zmiany dotyczyły genów syntetyzujących lub wykorzystujących NAD⁺, kluczową cząsteczkę dla energii i naprawy komórkowej. Zamiast prostych różnic w obfitości, ważne enzymy takie jak CD38, PARP2 i kilka sirtuin produkowały różne warianty RNA, co sugeruje, że równowaga między produkcją a zużyciem NAD⁺ jest zniekształcona na poziomie składania. Dotknięte geny skupiały się także w dobrze znanych szlakach sygnalizacyjnych mięśnia, w tym AMPK i FoxO, które działają jak komórkowe wskaźniki paliwa i reagenci stresu.
Wspólne wzorce na różnych etapach choroby — i u innych gatunków
Co uderzające, wiele tych samych genów wykazywało zmiany składania nie tylko u osób z pełną sarkopenią, ale także u tych z samą niską masą mięśniową lub samą słabością. To sugeruje, że nieprawidłowe składanie zaczyna się wcześnie i przekracza różne kliniczne oblicza choroby. Aby sprawdzić, czy zmiany te można odtworzyć w modelu zwierzęcym, badacze wywołali zanik mięśni u myszy za pomocą sterydu deksametazonu, standardowego sposobu na imitowanie niektórych cech sarkopenii. Myszy rozwinęły słabszy chwyt oraz gorsze wyniki w testach biegu i równowagi. Gdy zespół poddał sekwencjonowaniu RNA mięśni myszy, ponownie znalazł setki genów ze zmienionym składaniem. Około jednej piątej z nich pokrywała się z genami związanymi z sarkopenią u ludzi, a wiele z nich uczestniczyło w regulacji transkrypcji, strukturze chromatyny i samym procesie składania — wyższych poziomach przełączników, które mogą przekształcić cały program produkcji białek w komórce.
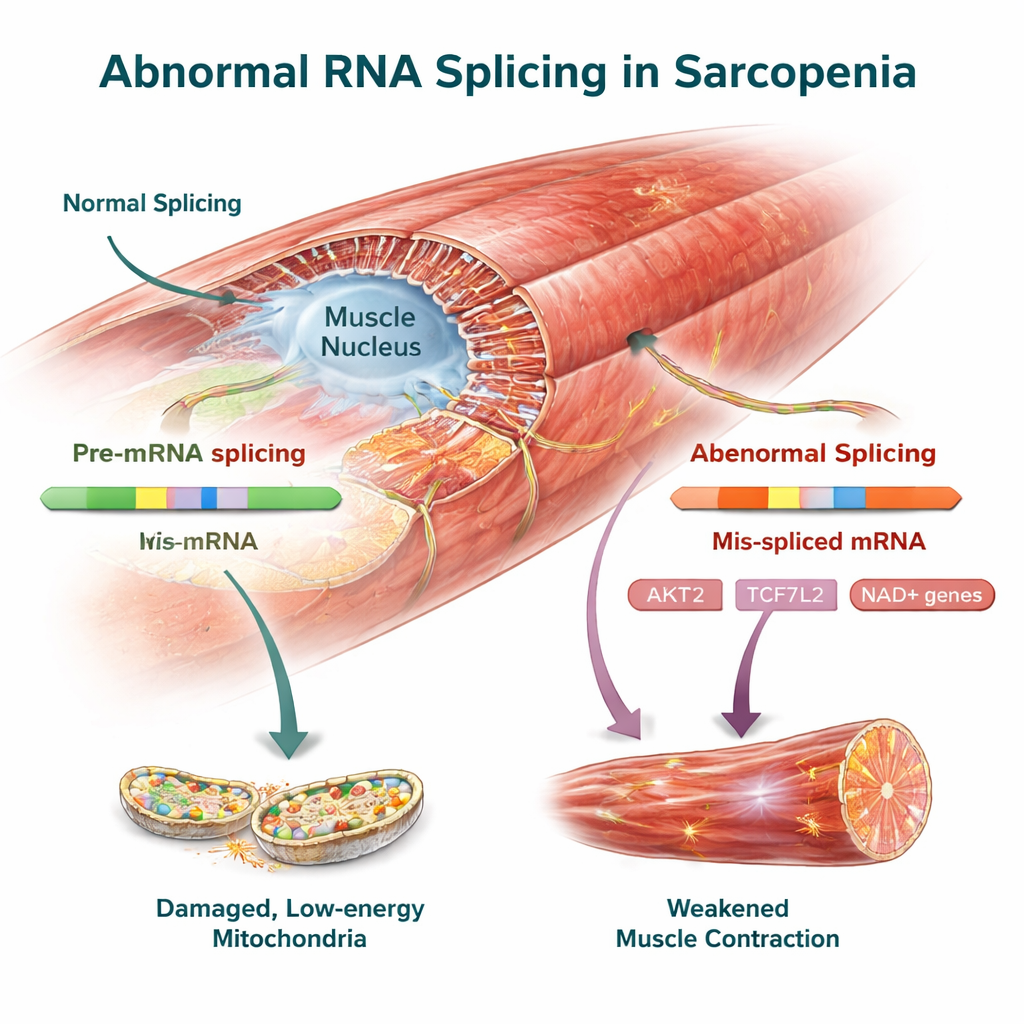
Kluczowe geny kontrolujące mięsień jako potencjalne cele terapeutyczne
Wśród zmian zachowanych między gatunkami znalazło się kilka genów już powiązanych ze zdrowiem mięśni. AKT2, centralny regulator wzrostu i budowy białek w mięśniu, wykazywał wyraźne przesunięcia składania zarówno u ludzi, jak i u myszy, które mogą osłabiać jego zdolność do utrzymania masy mięśniowej. TCF7L2, część szlaku sygnalizacyjnego Wnt, razem z FMNL2 i USP40, które pomagają organizować wewnętrzny szkielet mięśnia i nadzór jakości białek, także miały zmienione warianty RNA. Zespół potwierdził te zmiany składania eksperymentalnie w mięśniach myszy, co wzmacnia tezę, że są one rzeczywistymi cechami choroby, a nie artefaktami analizy danych.
Co to znaczy dla zapobiegania osłabieniu
Dla nietechnicznych czytelników kluczowa wiadomość jest taka, że sarkopenia to nie tylko „zużywanie się” mięśni czy proste włączanie i wyłączanie genów. Obejmuje także szeroko zakrojoną niewłaściwą edycję komunikatów RNA, które kierują tym, jak komórki mięśniowe tworzą i utrzymują swoje mechanizmy, zwłaszcza systemy generujące energię i wykrywające stres. Ponieważ składanie można w zasadzie skorygować za pomocą precyzyjnie zaprojektowanych leków opartych na RNA, zachowane błędy składania odkryte tutaj — w szczególności w genach takich jak AKT2 i TCF7L2 — oferują nowy zestaw wskazówek do opracowania terapii pomagających starzejącym się mięśniom zachować siłę na dłużej.
Cytowanie: Li, Y., Guo, X., Li, S. et al. Transcriptomic characterization of the aberrant alternative splicing in skeletal muscles of sarcopenia patients. Sci Rep 16, 5334 (2026). https://doi.org/10.1038/s41598-026-35002-w
Słowa kluczowe: sarkopenia, starzenie się mięśni, składanie RNA, mitochondria, AKT2