Clear Sky Science · pl
Model fenomenologiczny stabilizacji transtyretyny
Dlaczego to ma znaczenie dla pacjentów i rodzin
Amyloidoza transtyretynowa to poważne schorzenie, w którym normalne białko krwi — transtyretyna (TTR) — rozpada się, a jego fragmenty mogą tworzyć szkodliwe złogi w sercu i nerwach. Nowe leki, takie jak tafamidis i acoramidis, zostały zaprojektowane tak, by utrzymywać to białko w bezpiecznej, czteroczęściowej formie, i już poprawiły wyniki leczenia u wielu osób. Lekarze jednak obserwują zastanawiające zjawisko u leczonych pacjentów: stężenie TTR we krwi rośnie o ponad 30%, i nie jest to oczywiste dlaczego. Artykuł wykorzystuje uproszczony, matematyczny model, by zbadać, co może dziać się w organizmie i co to znaczy dla rzeczywistego działania tych leków. 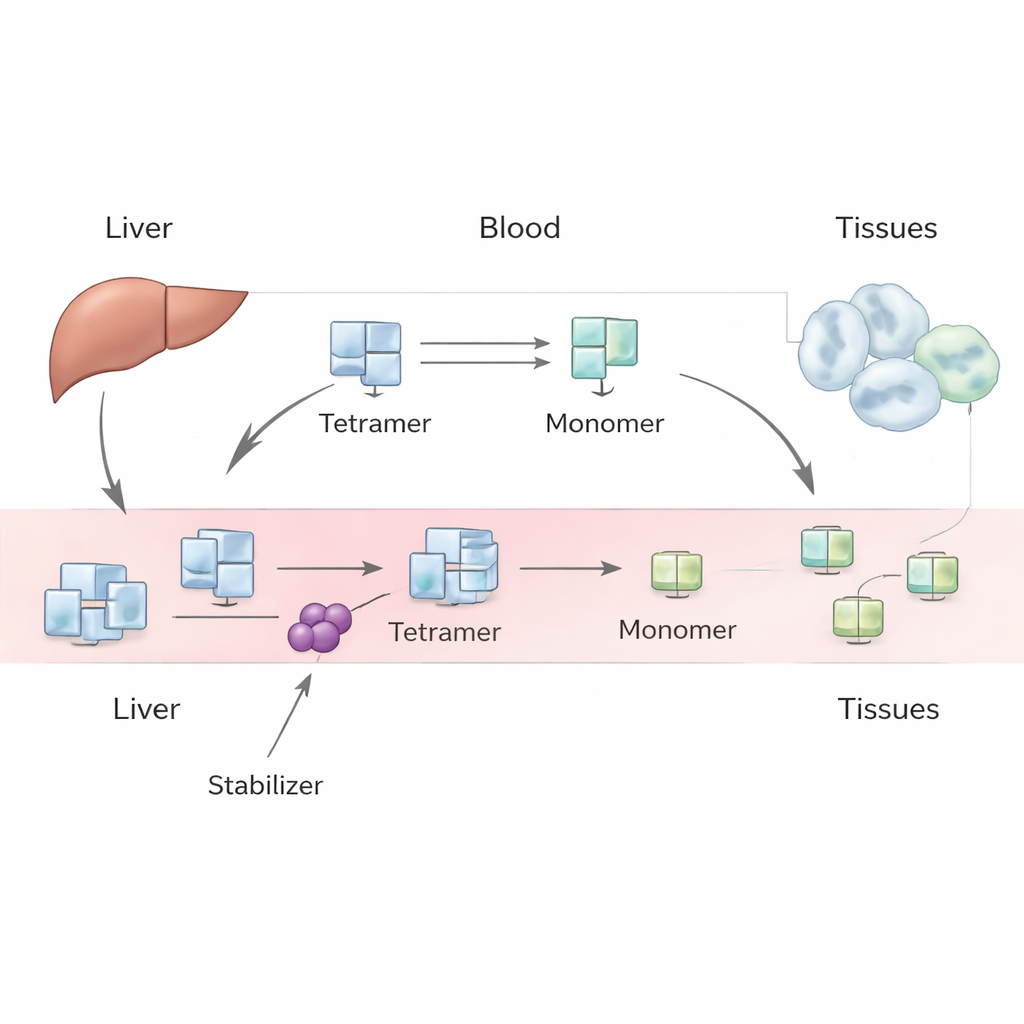
Białko, które może pomagać lub szkodzić
TTR jest wytwarzana głównie w wątrobie i normalnie krąży we krwi jako stabilny kompleks czterech identycznych podjednostek, zwany tetramerem. Transportuje hormon tarczycy i witaminę A. W pewnych warunkach, w tym podczas starzenia się lub wskutek dziedzicznych wariantów genów, tetramer może się rozpaść na pojedyncze podjednostki, czyli monomery. Te monomery mogą ulegać niewłaściwemu fałdowaniu i łączyć się w włókna amyloidowe, które uszkadzają tkanki i prowadzą do amyloidozy transtyretynowej serca (kardiomiopatii) lub nerwów (neuropatii). Leki takie jak tafamidis i acoramidis mają za zadanie wiązać tetramer i utrudniać jego rozpad, spowalniając postęp choroby. Jednak po rozpoczęciu terapii u pacjentów mierzalne stężenia TTR we krwi niezawodnie rosną, a ten wzrost jest większy niż sugerowałyby proste eksperymenty laboratoryjne.
Budowanie prostego obrazu złożonego systemu
Autorzy podchodzą do tej zagadki za pomocą modelu fenomenologicznego — skupiającego się na ogólnym obserwowalnym zachowaniu zamiast na każdym mikroskopijnym detalu. W ich ramie wątroba produkuje tetramery TTR w stałym tempie, które następnie trafiają do krwiobiegu. Po wejściu do krążenia tetramery mogą dysocjować do monomerów i ponownie się łączyć, a zarówno tetramery, jak i monomery mogą być usuwane z krwi przez wychwyt do tkanek i degradację. Popisując parę równań bilansu masy dla tetramerów i monomerów, zespół bada różne scenariusze: taki, w którym monomery głównie ponownie tworzą tetramery, taki, w którym są szybko usuwane, oraz pośredni, gdzie oba procesy mają znaczenie. Wykorzystują historyczne badania z użyciem znaczników u ludzi i nowoczesne dane z laboratoriów, by oszacować kluczowe wielkości, takie jak tempo klarowania tetramerów, szybkość ich rozpadu i siłę, z jaką leki spowalniają ten rozpad.
Dlaczego samo stabilizowanie tetrameru nie wystarcza
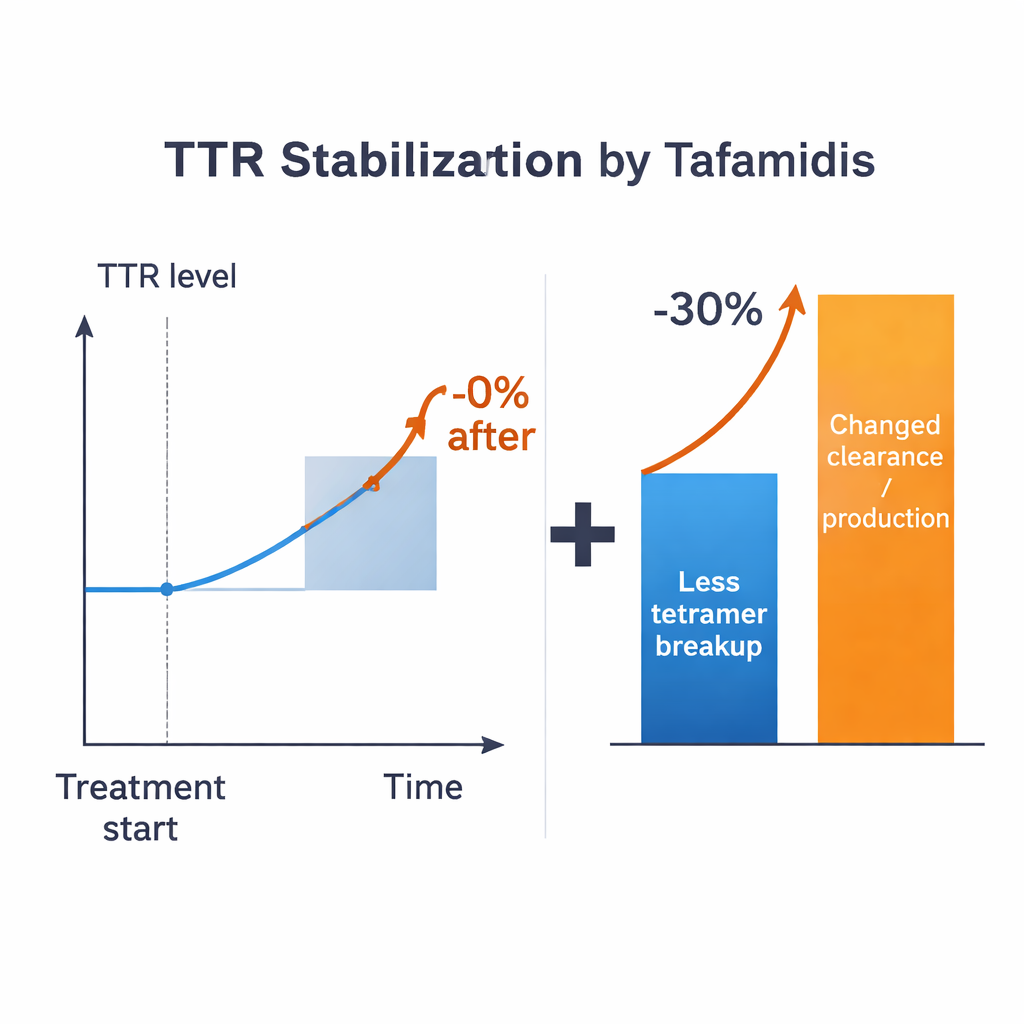
W oparciu o te oszacowania badacze zadają bezpośrednie pytanie: gdyby lek mógł idealnie zapobiec rozpadowi tetramerów, o ile wzrosłoby stężenie TTR we krwi? We wszystkich realistycznych reżimach odpowiedź jest skromna — rzędu maksymalnie około 15% dla typowych wartości parametrów, a często mniej, w zależności od losu monomerów. To jest daleko od obserwowanego u leczonych pacjentów wzrostu >30%. Rozbieżność utrzymuje się nawet przy szerokim uwzględnieniu niepewności w znanych parametrach. Model sugeruje zatem, że samo spowolnienie rozpadu tetramerów nie wyjaśnia w pełni klinicznego efektu. Muszą zachodzić także zmiany w innych procesach kontrolujących tempo produkcji TTR, jej wychwytu przez komórki lub rozkładu, gdy obecne są leki stabilizujące.
Wskazówki z poziomu leków i sprytnych eksperymentów
Aby powiązać ekspozycję na lek z zachowaniem TTR, autorzy łączą podstawowy model farmakokinetyczny tafamidu (jak lek porusza się po organizmie w czasie) ze specjalistycznymi testami „wymiany podjednostek”. W tych eksperymentach znakowane i nieznakowane tetramery TTR są mieszane w osoczu ludzkim, a stopniowa wymiana podjednostek ujawnia, jak często tetramery się rozrywają. Pomiary tego procesu przy różnych stężeniach leku dostarczają bezpośredniego, opartego na danych związku między poziomem tafamidu a efektywną stabilnością tetrameru, bez konieczności wiedzy, ile leku jest związane z albuminą czy hormonem tarczycy. Ten fenomenologiczny związek trafia do modelu i sprytnie omija wiele nieznanych biochemicznych szczegółów. Nawet z tą zaletą obliczenia nadal ograniczają spodziewany wzrost TTR do około połowy obserwowanego klinicznie przyrostu, co wzmacnia wniosek, że zmiany w klarowaniu, internalizacji, degradacji, a nawet syntezie muszą być częścią tego obrazu.
Co to oznacza na przyszłość
Dla osób niebędących specjalistami kluczowy przekaz jest taki: leki stabilizujące prawdopodobnie robią więcej niż tylko „sklejanie” tetramerów TTR. Prawdopodobnie wpływają też na to, jak organizm produkuje, usuwa lub odzyskuje to białko. Autorzy argumentują, że proste, przejrzyste modele takie jak ich są potężne, ponieważ ujawniają takie luki w naszym rozumieniu i wskazują konkretne eksperymenty — na przykład bezpośrednie mierzenie, jak szybko monomery są usuwane, jak szybko różne formy TTR są wychwytywane przez komórki, lub czy TTR związana z lekiem jest traktowana inaczej niż białko niezwiązane. Lepsze odpowiedzi na te pytania nie tylko dopracują leczenie amyloidozy transtyretynowej, lecz mogą także ujawnić ogólne zasady dotyczące innych chorób, w których normalne białka przekształcają się w szkodliwe agregaty.
Cytowanie: Lisowski, B., Ulaszek, S., Wiśniowska, B. et al. Phenomenological model of transthyretin stabilization. Sci Rep 16, 4904 (2026). https://doi.org/10.1038/s41598-026-35000-y
Słowa kluczowe: amyloidoza transtyretynowa, stabilizacja białek, tafamidis, modelowanie farmakokinetyczne, choroby amyloidowe