Clear Sky Science · pl
Spektroskopia ATR‑FTIR w połączeniu z chemometrią ujawnia zmiany molekularne i działanie przeciwnowotworowe ekstraktu z Nigella sativa w ludzkich komórkach raka jelita grubego
Starożytna przyprawa, współczesne pytanie onkologiczne
Nasiona czarnuszki, znane w medycynie ludowej jako Nigella sativa, od dawna stosowane są jako domowy środek leczniczy. W tym badaniu zadano bardzo współczesne pytanie dotyczące tej starożytnej przyprawy: co dokładnie dzieje się wewnątrz komórek raka jelita grubego po zastosowaniu ekstraktu z tych nasion, molekuła po molekule? Zamiast ograniczać się do prostych testów „zabija czy nie zabija”, badacze śledzą, jak ekstrakt zakłóca wewnętrzną chemię komórek nowotworowych i badają, czy mógłby on kiedyś uzupełniać istniejące terapie raka jelita grubego.
Rak jelita grubego i poszukiwanie łagodniejszych wsparć
Nowotwory okrężnicy i odbytnicy razem należą do najczęstszych przyczyn zgonów na świecie, a standardowe metody leczenia, takie jak operacja, chemioterapia i radioterapia, choć często ratują życie, mogą wiązać się z poważnymi skutkami ubocznymi i czasem tracić skuteczność. Wielu naukowców bada więc produkty naturalne jako terapie uzupełniające — nie jako cudowne lekarstwa, lecz jako potencjalne wsparcie, które mogłoby zwiększyć skuteczność leczenia lub zmniejszyć jego toksyczność. Nasiona czarnuszki są obiecującym kandydatem, ponieważ zawierają bogactwo biologicznie czynnych związków, w tym dobrze przebadany tymochinon, a wcześniejsze badania sugerowały działanie przeciwnowotworowe w różnych typach guzów.
Patrząc na komórki przez ich molekularne „odciski palców”
W tym badaniu zespół nie skupiał się na pojedynczym, oczyszczonym związku. Zamiast tego użyto surowego ekstraktu metanolowego z nasion Nigella sativa, zachowując naturalną mieszankę lipidów, związków aromatycznych i innych składników roślinnych, które mogą działać współdziałając. Eksponowano ludzkie komórki raka jelita grubego (linię komórkową Caco‑2) na różne stężenia tego ekstraktu przez 24 godziny i mierzono przeżywalność komórek. Około połowa komórek zginęła przy dawce średniej, którą wybrano do pogłębionej analizy. Aby zobaczyć, co zmieniło się w komórkach, które przeżyły, zastosowano technikę zwaną spektroskopią ATR‑FTIR, która przepuszcza światło podczerwone przez wysuszone próbki komórek i rejestruje szczegółowe „widmo” odzwierciedlające ilości i struktury głównych składników komórkowych, takich jak lipidy, białka i DNA. Zaawansowane metody komputerowe porządkowały i porównywały te spektroskopowe odciski palców.
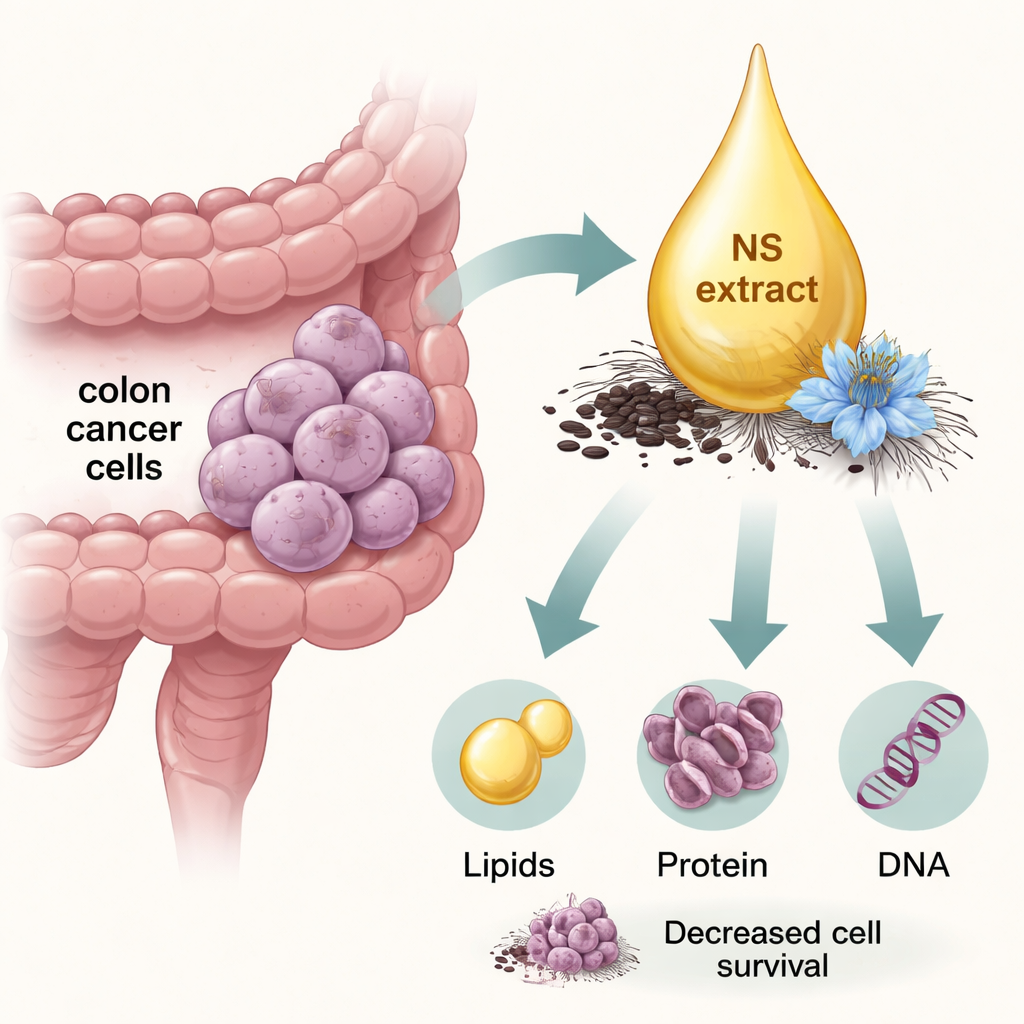
Jak ekstrakt z czarnuszki przekształca budulec komórek
Widma pochodzące z komórek traktowanych ekstraktem i z komórek kontrolnych rozdzieliły się na całkowicie odrębne grupy, co oznacza, że ekstrakt spowodował rozległe zmiany molekularne. Badacze stwierdzili, że nienasycone kwasy tłuszczowe w błonach komórkowych zmniejszyły się, podczas gdy wzrosły poziomy tłuszczów nasyconych oraz cząsteczek magazynujących tłuszcz, zwanych trójglicerydami. Łańcuchy tłuszczowe w błonach stały się krótsze, bardziej elastyczne i bardziej nieuporządkowane — wzorzec zgodny z uszkodzeniem oksydacyjnym, w istocie chemicznym „rdzewieniem” wywołanym przez reaktywne formy tlenu (ROS). Jednocześnie całkowita zawartość białka w komórkach spadła, a pozostałe białka wykazywały znamiona stresu: więcej form „skoniugowanych” wskazujących na niepoprawne fałdowanie i denaturację oraz wyższy poziom grup karbonylowych, markera nieodwracalnego uszkodzenia oksydacyjnego.
Zakłócanie sygnałów, paliwa i materiału genetycznego
Ekstrakt wydawał się również zakłócać sposób, w jaki komórki nowotworowe się komunikują i pozyskują energię. Poziomy fosforylacji białek — powszechnego włącznika/wyłącznika wykorzystywanego w szlakach wzrostu i przetrwania — spadły po leczeniu, co sugeruje tłumienie kluczowych obwodów sygnalizacyjnych. Wskaźniki związane z metabolizmem glukozy sugerowały, że komórki miały ograniczony dostęp do preferowanego paliwa i że przetwarzanie cukru było zaburzone. Sygnatury związane z DNA w widmach także wyraźnie zmalały, co jest zgodne ze zmniejszoną zawartością DNA lub zwiększoną ilością uszkodzeń DNA. Razem te zmiany tworzą obraz komórek pod silnym stresem oksydacyjnym i metabolicznym: ich błony stają się nieszczelne i nieuporządkowane, białka tracą właściwy kształt i funkcję, a materiał genetyczny zostaje uszkodzony na tyle, że uruchamiane są ścieżki prowadzące do śmierci komórki.
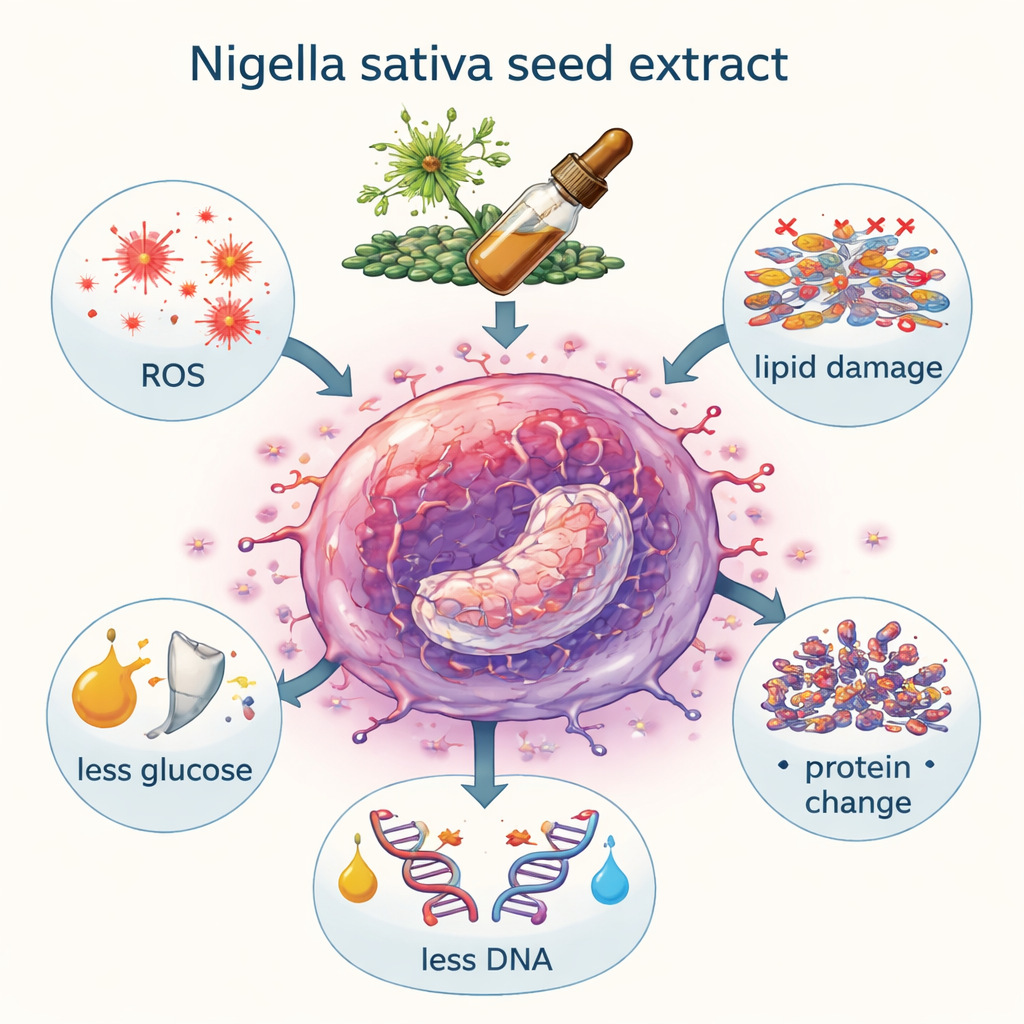
Co to może znaczyć dla przyszłych terapii
Dla osób niebędących specjalistami kluczowy przekaz jest taki, że ekstrakt z nasion czarnuszki robi znacznie więcej niż tylko hamuje wzrost komórek raka jelita grubego w warunkach laboratoryjnych. Wywołuje skoordynowany atak na podstawowe struktury i procesy komórkowe — lipidy, białka, gospodarkę energetyczną i DNA — w dużej mierze poprzez zwiększenie ROS i uszkodzeń oksydacyjnych. Nie oznacza to, że ludzie powinni samoleczyć się nasionami czy olejami; dawki, czystość i sposób podania w badaniach laboratoryjnych różnią się znacznie od codziennego stosowania, a takie silne efekty oksydacyjne mogłyby uszkadzać zdrowe komórki, jeśli nie byłyby starannie kontrolowane. Jednak praca dostarcza szczegółowej mapy molekularnej wyjaśniającej, dlaczego Nigella sativa zasługuje na dalsze badania jako starannie sformułowany partner konwencjonalnych terapii raka jelita grubego, i pokazuje spektroskopię w podczerwieni jako potężne, szybkie narzędzie do śledzenia działania złożonych mieszanin naturalnych wewnątrz komórek nowotworowych.
Cytowanie: Ozek, N.S., Ozyurt, I., Kucukcankurt, F. et al. ATR-FTIR spectroscopy combined with chemometrics reveals molecular alterations and anticancer effects of Nigella sativa extract in human colon cancer cells. Sci Rep 16, 5458 (2026). https://doi.org/10.1038/s41598-026-34994-9
Słowa kluczowe: rak jelita grubego, Nigella sativa, czarnuszka, naturalne środki przeciwnowotworowe, spektroskopia ATR‑FTIR