Clear Sky Science · pl
System ubikwityny–proteasomalny jest ważnym motorem postępu raka nosogardzieli związanego z EBV: metaanaliza danych transkryptomicznych
Rak w ukrytym zakątku gardła
Rak nosogardzieli rozwija się w niewielkiej, trudno dostępnej przestrzeni za nosem i nad tylną częścią gardła. Na świecie występuje stosunkowo rzadko, ale jest częstszy w niektórych rejonach Azji Południowo‑Wschodniej i Chin, często ze śmiertelnymi konsekwencjami. Niemal wszystkie te guzy noszą przewlekłą infekcję wirusem Epsteina–Barra (EBV), tym samym wirusem, który może wywoływać mononukleozę. W tym badaniu stawiane jest pilne pytanie dla pacjentów i lekarzy: w jaki sposób ten wirus po cichu przekształca komórki i ich otoczenie, aby nowotwór mógł rosnąć, ukrywać się przed układem odpornościowym i opierać się leczeniu?
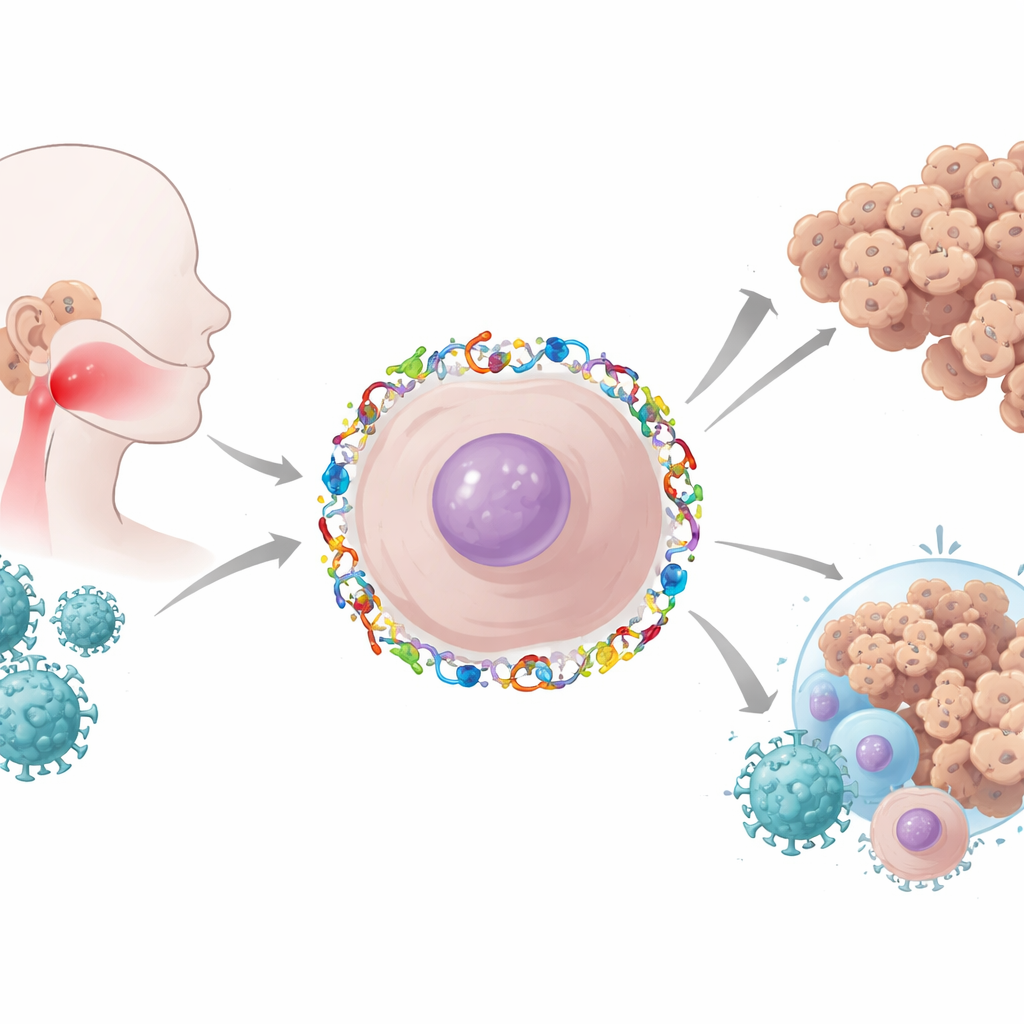
Wirusowy intruz i zatłoczone pole bitwy immunologicznej
Guzy nosogardzieli związane z EBV są pełne komórek odpornościowych, w tym limfocytów T, komórek NK i makrofagów. W wielu nowotworach tak liczne występowanie komórek odpornościowych jest dobrym znakiem, sugerującym, że organizm się broni. Tutaj jednak komórki odpornościowe są dziwnie nieskuteczne. EBV przyczynia się do tego paradoksu, wydzielając białka wirusowe i małe RNA, które przesuwają otaczającą tkankę w kierunku supresji zamiast ataku. Wirus skłania komórki do wydzielania uspokajających sygnałów, do ekspresji „hamulców” wywołujących wyczerpanie limfocytów T oraz do zmiany sposobu prezentacji fragmentów wirusowych i nowotworowych na powierzchni komórek. Efekt to ruchliwa, lecz stłumiona okolica immunologiczna, w której guz może spokojnie prosperować.
Komórkowy system utylizacji staje się zdrajcą
Autorzy skupiają się na komórkowym systemie recyklingu białek, znanym jako system ubikwityna–proteasom. W normalnych warunkach system ten znakuję zużyte lub uszkodzone białka i kieruje je do molekularnej „shredderki”. Produkuje też krótkie fragmenty, które pomagają komórkom odpornościowym rozpoznawać zakażone lub złośliwe komórki. Łącząc sześć dużych zestawów danych genetycznych z guzów i tkanek zdrowych, badacze zidentyfikowali tysiące genów zmienionych w raku nosogardzieli. Wśród nich 85 ludzkich genów fizycznie oddziałuje z białkami EBV, a ściśle powiązany klaster dotyczy właśnie tego systemu recyklingu białek. Wiele z tych genów gospodarza jest kontrolowanych przez białka EBV aktywne podczas fazy „litycznej” wirusa, gdy chwilowo się budzi, by się replikować. Sugeruje to, że okresowa reaktywacja wirusa może dostrajać wewnętrzny system utylizacji komórki rakowej w sposób sprzyjający guzowi.
Pojedyncze komórki ujawniają dwie twarze guza
Aby zobaczyć, gdzie te geny są aktywne, zespół sięgnął po sekwencjonowanie RNA pojedynczych komórek, metodę odczytującą aktywność genów w tysiącach indywidualnych komórek pobranych z guzów. Porównali nowotwory nosogardzieli dodatnie na EBV z nowotworami migdałków i części gardła ujemnymi na wirusa. Komórki nowotworowe w guzach nosogardzieli wykazywały konsekwentnie wyższą aktywność genów systemu recyklingu białek niż ich odpowiedniki, a niektóre komórki odpornościowe również pokazywały podwyższoną aktywność. Kiedy badacze pogrupowali komórki guza według tego sygnaturowego wzorca, wyłoniły się dwa główne stany. Komórki „UPS‑High” miały bardzo aktywny aparat recyklingowy, niższe oznaki podziału komórkowego oraz silniejsze powiązania z zachowaniami przypominającymi komórki macierzyste i sygnałami tłumiącymi odporność. Komórki „UPS‑Low” dzieliły się szybciej i były związane z klasycznymi szlakami napędzającymi wzrost, takimi jak te aktywowane przez czynniki wzrostu fibroblastów i białka Wnt.
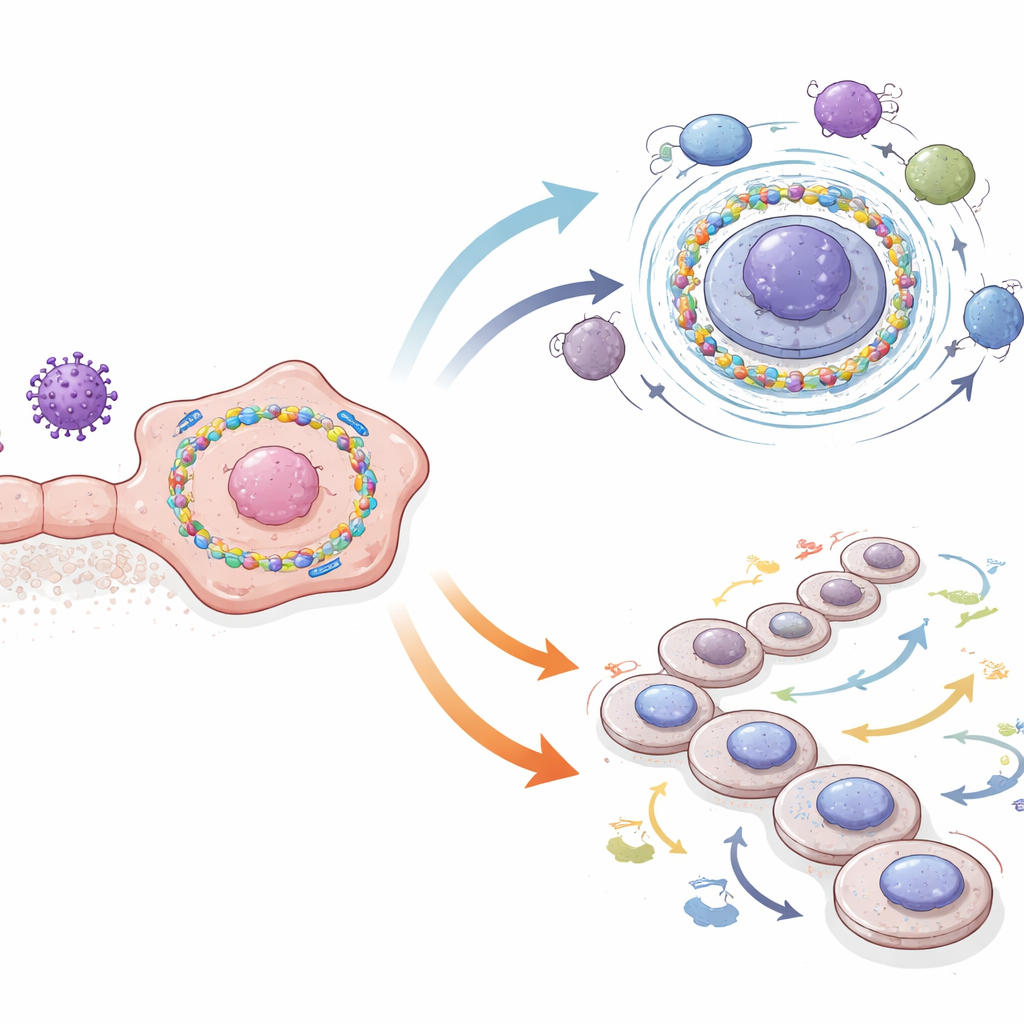
Jak komórki guza komunikują się z sąsiadami
Zespół wykorzystał następnie narzędzia obliczeniowe do przewidzenia, jak te dwa stany komórek guza komunikują się z pobliskimi komórkami odpornościowymi. Komórki w stanie UPS‑High wydawały się nadawać komunikaty sprzyjające tolerancji immunologicznej zamiast ataku. Wykazywały zmniejszoną aktywność sygnałów, które zwykle eksponują wewnętrzne białka przed „strażnikami” układu odpornościowego, przez co trudniej je „dostrzec”. Jednocześnie angażowały szlaki powiązane z supresją immunologiczną, w tym sygnały wynikające z takich cząsteczek jak czynnik hamujący migrację makrofagów (MIF) oraz niektóre komponenty błony podstawnej. Dla porównania komórki UPS‑Low wysyłały i odbierały więcej sygnałów związanych z wzrostem i przebudową tkanki, zgodnie z bardziej szybko rosnącą, ale mniej skrytą populacją.
Co to oznacza dla pacjentów i przyszłych terapii
Analizując zbiory danych pacjentów w różnych typach nowotworów, w tym w guzach głowy i szyi oraz mniejszej kohorcie raka nosogardzieli, badacze stwierdzili, że wyższa ekspresja tej 12‑genowej sygnatury recyklingu białek zwykle wiąże się z gorszym przeżyciem. Proponują, że EBV kieruje część komórek nowotworowych w stan UPS‑High, który rośnie wolniej, ale lepiej się ukrywa i zachowuje cechy rezerwuaru komórek podobnych do macierzystych, zdolnych przetrwać terapię i zasiewać nawroty. Inne komórki pozostają w stanie UPS‑Low, napędzając szybkie powiększanie guza. Chociaż te wnioski pochodzą głównie z pomiarów RNA i wymagają potwierdzenia w laboratorium, wskazują na maszynerię recyklingu białek zarówno jako marker agresywnej choroby, jak i obiecujący cel terapeutyczny. Precyzyjne modulowanie tego systemu — szczególnie w połączeniu z terapiami układu odpornościowego — mogłoby pewnego dnia pomóc „zdemaskować” komórki nowotworowe napędzane przez EBV i poprawić rokowania osób z rakiem nosogardzieli.
Cytowanie: Ratnawati, H., Sanjaya, A., Christiandy, A. et al. The ubiquitin–proteasome system is an important driver of EBV-associated nasopharyngeal carcinoma progression: a meta-analysis of transcriptomic data. Sci Rep 16, 8892 (2026). https://doi.org/10.1038/s41598-025-34808-4
Słowa kluczowe: rak nosogardzieli, wirus Epsteina–Barra, system ubikwityna–proteasom, mikrośrodowisko immunologiczne guza, unikanie odpowiedzi immunologicznej