Clear Sky Science · pl
W pełni zautomatyzowany przepływ pracy do cyfrowej analizy obrazów w teście przeżywalności mikrokolonii jelitowych
Dlaczego szybsze i bardziej obiektywne odczyty tkankowe mają znaczenie
Gdy lekarze i naukowcy badają wpływ promieniowania na jelita, często polegają na żmudnej inspekcji obrazów mikroskopowych. Eksperci muszą wizualnie policzyć maleńkie skupiska regenerujących się komórek w jelicie cienkim — zadanie wolne, męczące i zaskakująco subiektywne. Artykuł przedstawia sposób, by powierzyć większość tej pracy komputerowi, wykorzystując nowoczesną analizę obrazów i sztuczną inteligencję (AI) do automatycznego zliczania tych struktur. Cel jest prosty, lecz istotny: uczynić badania nad promieniowaniem bardziej spójnymi, szybszymi i mniej zależnymi od ograniczonego czasu ekspertów.
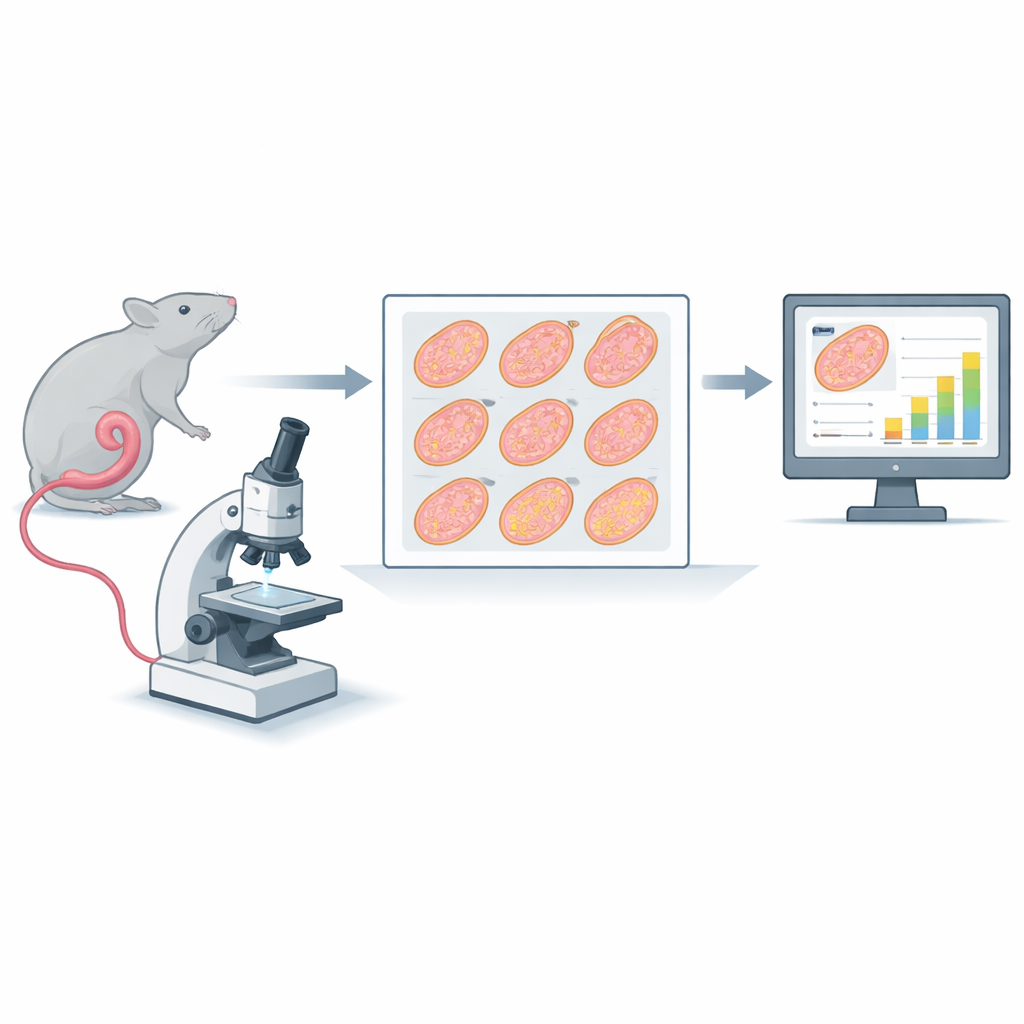
Od jelita myszy do slajdów cyfrowych
Badania koncentrują się na klasycznym teście zwanym testem przeżywalności mikrokolonii jelitowych. W tym teście myszy otrzymują napromieniowanie brzucha. Około trzy i pół dnia później fragment jelita cienkiego (jelito czcze) jest wycinany, dzielony na dziewięć krótkich segmentów, zatapiany w wosku, krojony na niezwykle cienkie przekroje, barwiony i skanowany w wysokiej rozdzielczości. Każde skanowanie daje ogromny obraz cyfrowy zawierający dziewięć okrągłych przekrojów tkanki jelitowej. Tradycyjnie wyszkoleni obserwatorzy przybliżają każdy okrąg i liczą krypty — małe, gruczołopodobne zagłębienia przy wewnętrznej krawędzi, gdzie odnawiają się komórki. Mniej przeżywających krypt oznacza poważniejsze uszkodzenie spowodowane promieniowaniem lub leczeniem łączonym, takim jak chemioterapia.
Problem z ręcznym liczeniem
Ręczne zliczanie może wydawać się proste, ale artykuł pokazuje, że wcale takie nie jest. Piętnaście osób, zarówno doświadczonych, jak i początkujących liczników, zostało przeszkolonych zgodnie ze standardowymi zasadami określającymi, co kwalifikuje się jako krypta. Mimo to ich zliczenia tych samych obrazów często znacząco się różniły. Na ponad 300 przekrojach średnia różnica względem średniej grupy wynosiła około jednej trzeciej, a niezgodność była największa w przypadkach z bardzo niewielką liczbą krypt. Nawet wśród trzech ekspertów z wieloletnim doświadczeniem pozostawały różnice rzędu około dziesięciu procent. Taka zmienność może osiągać skalę efektów leczenia, które naukowcy próbują zmierzyć, co zwiększa ryzyko, że istotne wyniki zostaną rozmyte przez ludzki szum.
Jak działa zautomatyzowany przepływ pracy
Autorzy zaprojektowali czterostopniowy zautomatyzowany przepływ pracy, który naśladuje działania uważnego człowieka, dodając przy tym nowe możliwości. Po pierwsze, skrypt komputerowy pobiera każdy duży obraz slajdu i automatycznie wycina dziewięć okrągłych fragmentów tkanki, korygując różnice w rozmiarze obrazu i kolorze barwienia. Po drugie, model głębokiego uczenia o nazwie nnU-Net oznacza piksele należące do krypt w każdym okręgu, tworząc czarno-białą „maskę” prawdopodobnych obszarów krypt. Po trzecie, autorski algorytm wyznacza krawędzie każdego regionu, filtruje malutkie kropki zbyt małe, by być prawdziwymi kryptami, i — co kluczowe — próbuje rozdzielić zlepione regiony, które w rzeczywistości zawierają kilka sąsiadujących krypt. Wreszcie, graficzny interfejs pozwala recenzentowi zobaczyć obrysy nałożone na oryginalne obrazy, poprawić błędy kilkoma kliknięciami i automatycznie zapisać ostateczne zliczenia oraz pomiary.
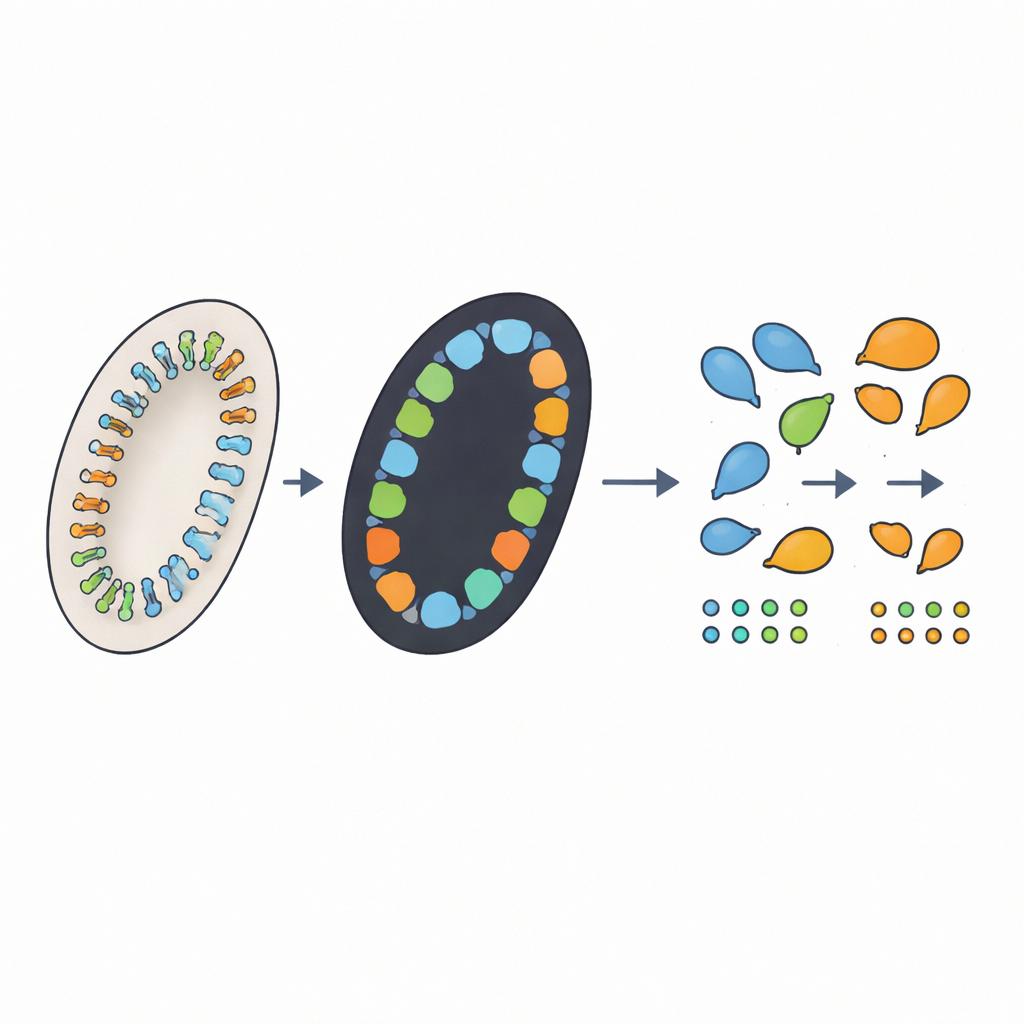
Wyniki zbliżone do ekspertów, ale w godzinach zamiast tygodni
Aby ocenić skuteczność zautomatyzowanego przepływu pracy, zespół porównał jego zliczenia z ocenami ekspertów na kilku zbiorach danych. Dla obrazów użytych do trenowania systemu krok głębokiego uczenia bardzo dokładnie oznaczał obszary krypt, a algorytm zliczający zbliżał się do konsensusu ekspertów o kilka krypt, szczególnie po dodaniu etapu rozdzielania zlepionych krypt. Dla nowych obrazów niewidzianych podczas treningu zautomatyzowane zliczenia różniły się od średniej trzech ekspertów o około dziesięć procent — podobnie lub nieco lepiej niż różnice występujące między samymi ekspertami. Gdy eksperci później przeglądali i korygowali wyniki automatyczne przez interfejs, zwykle potrzebowali poniżej minuty na obraz. W sumie pełne eksperymenty obejmujące 60 myszy można było przetworzyć w zaledwie kilka godzin czasu komputerowego i w kilka minut pracy ludzkiej.
Nowe sposoby opisu uszkodzeń jelit
Ponieważ przepływ pracy analizuje całe obrazy cyfrowe, może łatwo mierzyć cechy trudne do śledzenia ręcznie, takie jak długość obwodu jelita czy powierzchnia każdej krypt. Autorzy zbadali, czy uwzględnienie tych cech w zliczeniach krypt — zasadniczo pytanie, czy „krypty na jednostkę długości jelita” lub „krypty skorygowane o ich rozmiar” lepiej odzwierciedlają uszkodzenie po promieniowaniu — dałoby czystszy sygnał. W tym badaniu żadne z alternatywnych miar nie przewyższyło konsekwentnie surowych zliczeń krypt, ale podejście pokazuje, że automatyczna analiza obrazów może otworzyć drogę do bogatszych, bardziej zniuansowanych wskaźników uszkodzeń tkankowych.
Co to oznacza dla przyszłych badań
Dla osób spoza tej dziedziny kluczowy wniosek jest taki, że badacze zbudowali praktycznego cyfrowego asystenta, który potrafi odczytywać skomplikowane slajdy tkankowe niemal tak niezawodnie jak doświadczeni eksperci, lecz znacznie szybciej i bardziej spójnie. Ograniczając żmudną pracę ręczną i wygładzając różnice między ludźmi, ten zautomatyzowany system może uczynić badania nad promieniowaniem jelit bardziej solidnymi i łatwiejszymi do porównania między laboratoriami. Autorzy wskazują też oczywiste ścieżki dalszych ulepszeń, takie jak wykorzystanie modeli, które bezpośrednio rozdzielają sąsiadujące krypty. Poza tym jednym testem ich ramy stanowią wzór do automatyzacji innych ocen mikroskopowych, przesuwając patologię w stronę przyszłości, w której staranna ludzka ocena jest wspierana — a nie zastępowana — przez przejrzyste, godne zaufania narzędzia AI.
Cytowanie: Baikalov, A., Wang, E., Neill, D. et al. A fully automated workflow for the digital image analysis of the intestinal microcolony survival assay. Sci Rep 16, 9633 (2026). https://doi.org/10.1038/s41598-025-34719-4
Słowa kluczowe: test przeżywalności mikrokolonii jelitowych, zautomatyzowana histopatologia, analiza obrazów z użyciem głębokiego uczenia, uszkodzenie jelit wywołane promieniowaniem, przepływ pracy zliczania krypt