Clear Sky Science · pl
Pan-centromerowy FISH zwiększa precyzję w biodosymetrii radiacyjnej
Dlaczego ważne jest mierzenie niewidzialnego promieniowania
Promieniowanie pochodzące z zabiegów medycznych, przemysłu lub wypadków może cicho uszkadzać nasz DNA bez żadnych natychmiastowych widocznych objawów. W sytuacji awaryjnej lub w przypadku pracowników rutynowo narażonych na promieniowanie lekarze i służby bezpieczeństwa muszą szybko i dokładnie wiedzieć, jaką dawkę otrzymała dana osoba. Artykuł opisuje udoskonaloną technikę laboratoryjną, która ułatwia wykrywanie ukrytych uszkodzeń w chromosomach, potencjalnie przekształcając niepewne szacunki narażenia w bardziej wiarygodne, istotne dla decyzji medycznych wartości.
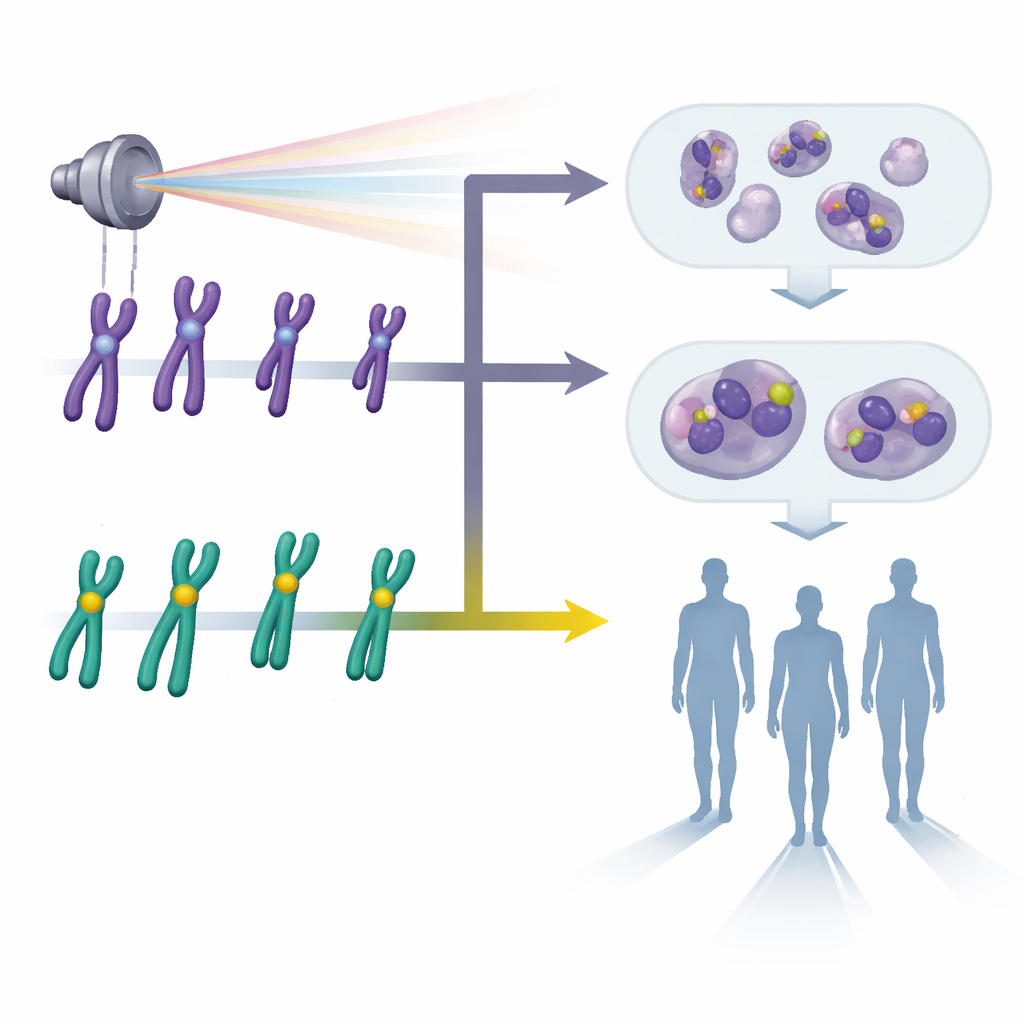
Szukając uszkodzeń w instrukcji obsługi organizmu
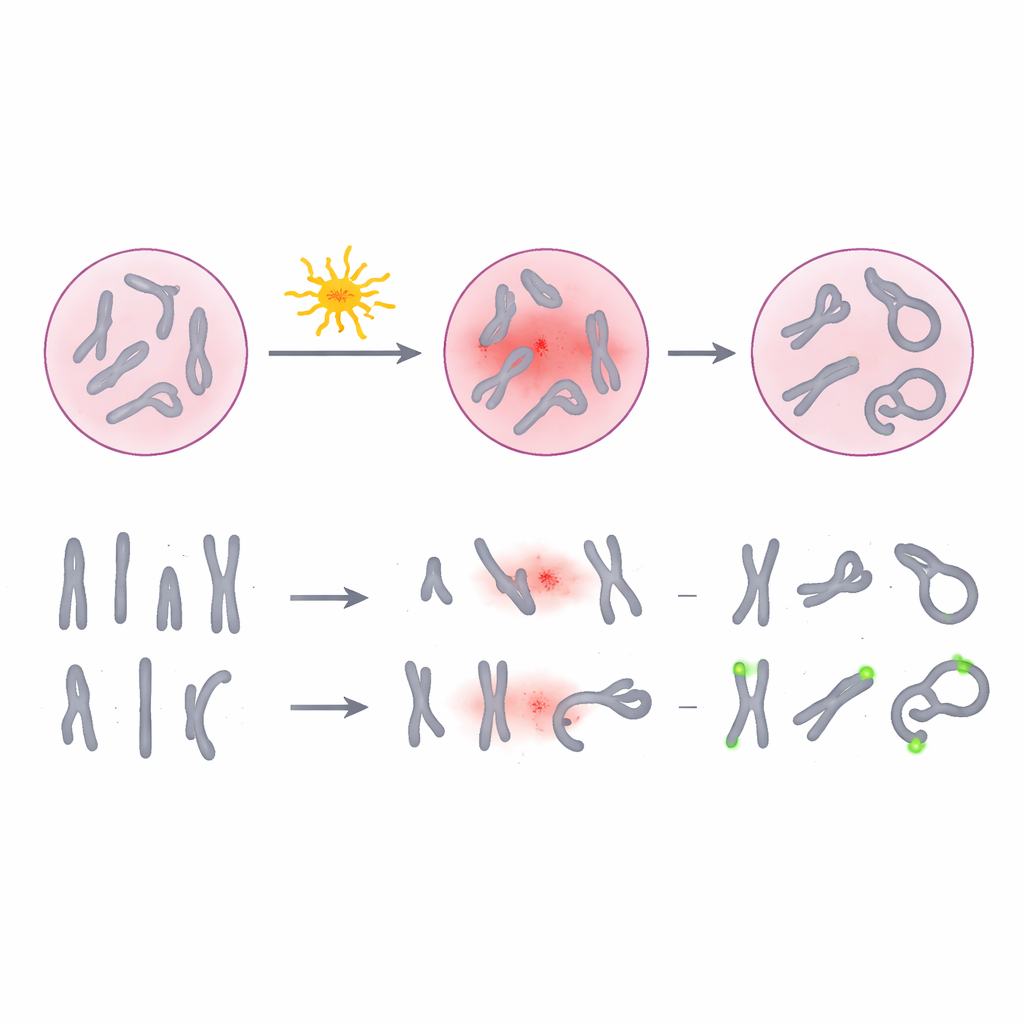
Promieniowanie może łamać i przestawiać fragmenty naszych chromosomów — włóknistych struktur przenoszących instrukcje genetyczne. Pewne niestandardowe kształty chromosomów, zwane dicytrami i pierścieniami, są szczególnie dobrymi „odciskami palców” narażenia, ponieważ powstają głównie po ekspozycji na promieniowanie i występują częściej przy wyższych dawkach. Przez dekady laboratoria stosowały fioletowy barwnik znany jako Giemsa do barwienia chromosomów w komórkach krwi i liczenia tych charakterystycznych zmian pod mikroskopem. Chociaż metoda ta jest szeroko akceptowana i stosunkowo tania, zależy od umiejętności osoby oceniającej w interpretacji subtelnych kształtów, szczególnie gdy chromosomy nachodzą na siebie, są słabo rozłożone lub są słabo widoczne. Przy niskich dawkach — właśnie tam, gdzie najtrudniej, lecz najważniej jest ustalić, czy ktoś był narażony — uszkodzenia mogą być rzadkie i łatwe do przeoczenia.
Oświetlenie środka każdego chromosomu
Badacze przetestowali alternatywne podejście zwane pan-centromerową fluorescencyjną hybrydyzacją in situ, w skrócie pan-cent-FISH. Zamiast barwić całe chromosomy, technika ta przyłącza znakowane fluorescencyjnie sondy do centromeru, niewielkiego centralnego regionu każdego chromosomu. Przy obserwacji w specjalnym mikroskopie każdy centromer promienieje intensywnym światłem, co znacznie ułatwia rozpoznanie, gdy chromosom ma dwa centra (dicytr) lub tworzy pierścień. Zespół pobrał krew od ochotników, wystawił próbki na kontrolowane dawki promieniowania gamma od zera do trzech jednostek dawki, a następnie przygotował tysiące rozmazów komórkowych zarówno metodą tradycyjnego barwienia Giemsa, jak i pan-cent-FISH. Następnie starannie policzyli uszkodzone chromosomy, by skonstruować krzywe odpowiedzi dawka–efekt, które łączą ilość zaobserwowanych uszkodzeń z podaną dawką promieniowania.
Dokładniejsze oszacowania dawki dzięki jaśniejszym sygnałom
Wśród ponad 30 000 analizowanych komórek pan-cent-FISH konsekwentnie wykrywał więcej powstałych w wyniku promieniowania dicytrów i pierścieni niż barwienie Giemsa. Wzrost był najbardziej wyraźny przy niskich dawkach poniżej pół jednostki, gdzie konwencjonalne barwienie łatwo może przeoczyć rzadkie zdarzenia. Gdy badacze dopasowali do danych funkcje matematyczne, krzywa pan-cent-FISH rosła stromo, co oznacza większą czułość na zmiany dawki. Aby przetestować praktyczną skuteczność, wykorzystali obie metody do oszacowania dawki w ukrytych próbkach krwi, których rzeczywiste narażenie znał tylko zespół eksperymentatorów. Średnio pan-cent-FISH zmniejszył błąd w oszacowaniach dawki mniej więcej o połowę w porównaniu z Giemsą. Przy bardzo niskiej testowej dawce nowa metoda utrzymała się w powszechnie akceptowanych granicach błędu, podczas gdy tradycyjne podejście wychodziło poza nie.
Balans między szybkością, nakładem pracy a zastosowaniami praktycznymi
Chociaż metoda fluorescencyjna wymaga specjalnych sond, mikroskopu fluorescencyjnego i nieco dłuższych przygotowań, rekompensuje to podczas analizy. Ponieważ świecące centromery ułatwiają rozpoznawanie nieprawidłowych chromosomów, osoby liczące mogą pracować szybciej z mniejszą liczbą przypadków niejednoznacznych i konieczności ponownych kontroli. Technika ta zmniejsza też ryzyko rozbieżności między obserwatorami, co jest istotne, gdy wiele laboratoriów musi porównywać wyniki. Autorzy zauważają, że barwienie Giemsa pozostaje atrakcyjne w warunkach ograniczonych zasobów ze względu na niższe koszty, ale argumentują, że pan-cent-FISH oferuje wyraźne zalety tam, gdzie precyzja ma największe znaczenie, na przykład przy monitoringu regulacyjnym blisko dopuszczalnych limitów narażenia lub podczas triage po dużym zdarzeniu radiologicznym.
Wyraźniejsze obrazy chromosomów dla bezpieczniejszych decyzji
Mówiąc prosto, badanie pokazuje, że oświetlenie centralnej części każdego chromosomu daje naukowcom czytelniejszy obraz uszkodzeń spowodowanych promieniowaniem niż tradycyjne metody barwienia. Dzięki ujawnianiu większej liczby subtelnych zmian w strukturze DNA, szczególnie przy niskich dawkach, pan-cent-FISH pozwala na oszacowania dawki bliższe prawdzie i bardziej spójne między próbkami. Dla pracowników narażonych na promieniowanie oraz osób dotkniętych zdarzeniami jądrowymi lub radiologicznymi ta poprawa czytelności może przełożyć się na lepszą opiekę medyczną, bardziej odpowiedni follow-up i pewniejsze decyzje dotyczące bezpieczeństwa.
Cytowanie: Chaurasia, R.K., Notnani, A., Vaz, D.F. et al. Pan centromeric FISH enhances precision in radiation biodosimetry. Sci Rep 16, 8020 (2026). https://doi.org/10.1038/s41598-025-34407-3
Słowa kluczowe: narażenie na promieniowanie, biodosymetria, uszkodzenia chromosomów, fluorescencyjna hybrydyzacja in situ, zdarzenia radiologiczne