Clear Sky Science · pl
Celowana stabilizacja czynnika indukowanego niedotlenieniem 1‑alfa (HIF1A) podczas in vitro dojrzewania bydlęcych kompleksów komórka‑osocyt zwiększa wskaźniki blastocyst
Dlaczego modyfikacja wykrywania tlenu w jajach ma znaczenie
Współczesne hodowle bydła w dużej mierze opierają się na zarodkach wytwarzanych w laboratorium, ale powodzenie jest dalekie od gwarantowanego: tylko około jednej trzeciej komórek jajowych osiąga kluczowy etap blastocysty, kiedy można je przenieść do krowy. To badanie stawia pozornie proste pytanie o szerokim znaczeniu dla hodowli zwierząt i wspomaganego rozrodu: czy bardziej wierne naśladowanie niskotlenowych warunków, jakich doświadczają jajeczka naturalnie w jajniku — poprzez łagodne wzmocnienie kluczowego białka wykrywającego tlen — może pomóc większej liczbie zarodków w prawidłowym rozwoju?
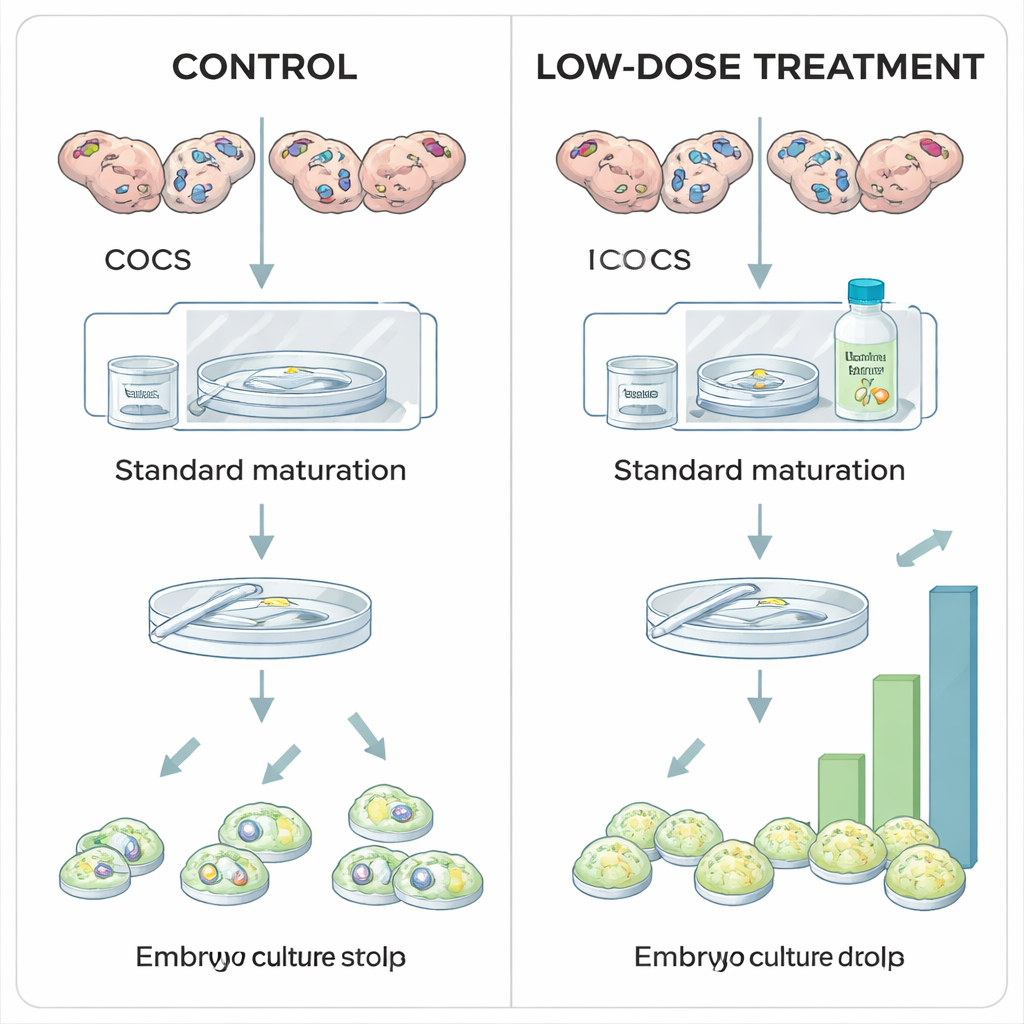
Życie zaczyna się w niszy o niskiej zawartości tlenu
W jajniku każde rozwijające się jajeczko otoczone jest wspierającym skupiskiem komórek zwanych komórkami kumulusowymi, razem tworząc kompleks kumulus‑oocyt. Chociaż unaczynienie jajnika zwiększa się w miarę wzrostu pęcherzyków, naczynia krwionośne nie sięgają bezpośredniego otoczenia oocytu. Tlen musi dyfundować, tworząc wokół dojrzewającego oocytu lekko obniżoną, czyli hipoksyczną, strefę. W tej niszy wewnątrzkomórkowy sensor zwany HIF1A pomaga komórkom przystosować się poprzez regulację metabolizmu i produkcji hormonów. Wcześniejsze prace wykazały, że zahamowanie HIF1A szkodzi dojrzewaniu oocytu i drastycznie redukuje tworzenie zarodków, co wskazuje na to białko jako centralnego koordynatora kompetencji oocytu — zdolności oocytu do zapłodnienia i rozwoju w zdrowy zarodek.
Użycie leku do precyzyjnego dostrojenia sensora tlenu w jajku
Naukowcy badali, czy umiarkowana stabilizacja HIF1A podczas laboratoryjnego dojrzewania bydlęcych oocytów może zwiększyć plony zarodków. W standardowych protokołach in vitro kompleksy kumulus‑oocyt dojrzewają w warunkach powietrza atmosferycznego, głównie z powodów praktycznych, a nie biologicznych. W tym eksperymencie oocyty pobrane z jajników rzeźnych podzielono na grupy i przez 24‑godzinny okres dojrzewania wystawiono na działanie różnych dawek Roxadustatu — leku stosowanego już w medycynie ludzkiej w leczeniu niedokrwistości. Roxadustat działa przez blokowanie rodziny enzymów zwanych prolinowymi hydroksylazami (PHD), które normalnie oznaczają HIF1A do degradacji, gdy tlenu jest dużo. Hamując PHD, Roxadustat pozwala na gromadzenie się białka HIF1A nawet przy wyższych poziomach tlenu, częściowo odtwarzając sygnał hipoksji, jaki oocyt odbierałby in vivo.
Więcej blastocyst przy właściwej dawce, szkoda przy wyższych poziomach
Po ocenie losów oocytów i zarodków po leczeniu wyłonił się wyraźny wzorzec. Niska dawka Roxadustatu (25 mikromolowa) nie zmieniała odsetka oocytów, które ukończyły dojrzewanie, ani odsetka zapłodnionych oocytów, które zaczęły się dzielić, lecz istotnie zwiększała proporcję osiągającą etap blastocysty. Innymi słowy, wczesne etapy pozostawały bez zmian, a mimo to więcej zarodków pomyślnie ukończyło wymagającą drogę do blastocysty — co sugeruje, że umiarkowana stabilizacja HIF1A poprawia wewnętrzną jakość oocytu. W przeciwieństwie do tego najwyższa dawka (100 mikromolowa) zmniejszyła odsetek oocytów, które w ogóle dojrzały, a gdy ten sam inhibitor zastosowano później, podczas ośmiodniowej hodowli zarodków, wysokie dawki ostro obniżyły tworzenie blastocyst bez zmiany wczesnego podziału komórek. Wyniki te wskazują, że „właściwy” poziom aktywności HIF1A podczas dojrzewania jest korzystny, natomiast zbyt duża lub przedłużona aktywacja szkodzi.
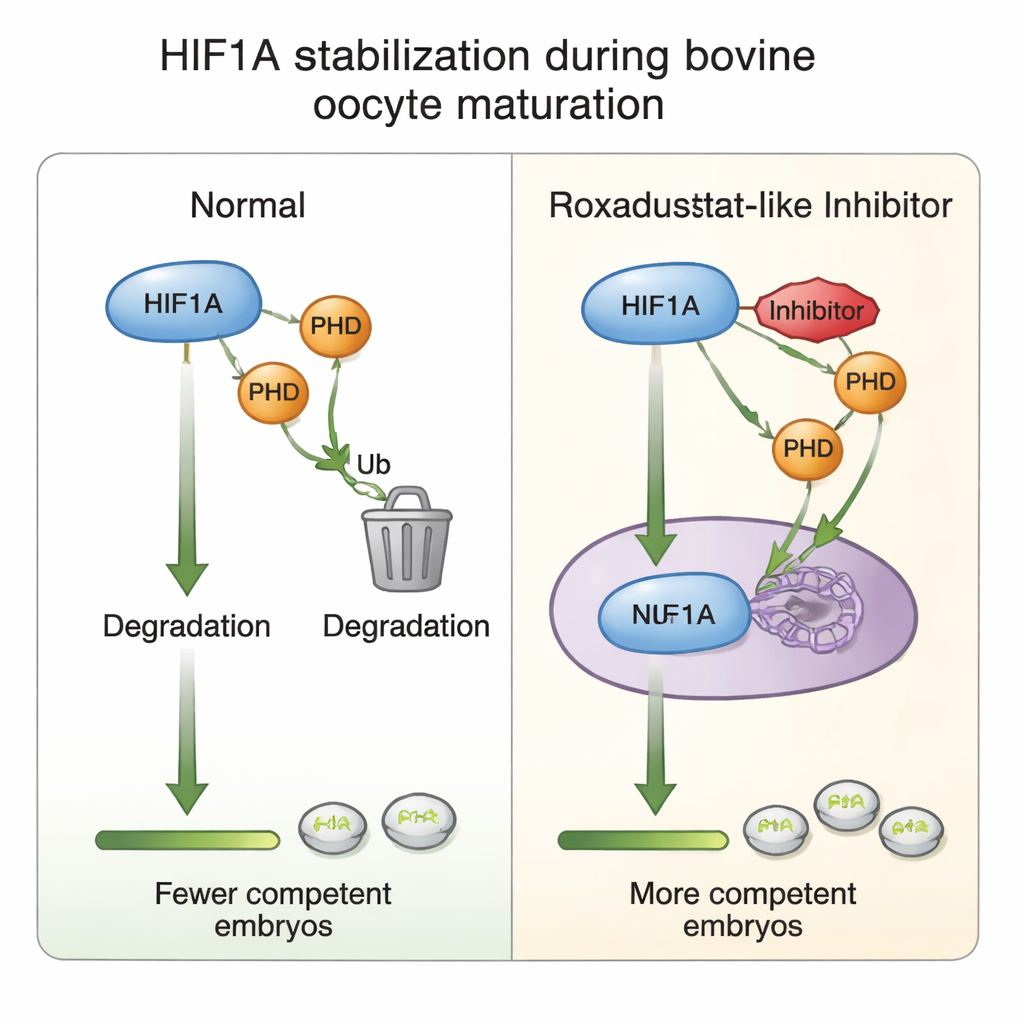
Co dzieje się wewnątrz komórek wspierających oocyt
Aby zrozumieć mechanizm chemicznego dostrajania, autorzy przeanalizowali komórki kumulusowe otaczające każdy oocyt. Stwierdzili, że samo dojrzewanie ogólnie podnosi aktywność genu HIF1A, ale dodanie Roxadustatu paradoksalnie obniżało mRNA HIF1A przy jednoczesnym utrzymaniu poziomów białka HIF1A — to wskazówka, że komórki mogą tłumić ekspresję genową, gdy białko jest wystarczająco ustabilizowane, swego rodzaju wbudowany hamulec przed nadaktywacją. Poziomy PHD2, najbardziej wrażliwej na tlen z enzymów PHD, wzrosły w odpowiedzi na lek, podkreślając jej rolę w pętli wykrywania tlenu. Przy wyższych dawkach leku zmniejszyły się markery proliferacji komórek oraz składniki lepkiej macierzy, która pomaga komórkom kumulusowym rozprzestrzeniać się wokół oocytu, co koreluje z obserwowanym spadkiem dojrzewania i tworzenia zarodków. Wszystko to wspiera ideę, że starannie zbalansowana aktywność HIF1A precyzyjnie dostraja dialog między oocytem a komórkami kumulusowymi, leżący u podstaw późniejszego sukcesu rozwojowego.
Implikacje dla hodowli zwierząt i dalej
Ta praca pokazuje, że łagodne ustabilizowanie sensora tlenu oocytu w krótkim oknie dojrzewania in vitro może istotnie zwiększyć i ustabilizować plony blastocyst u bydła, bez zmiany zapłodnienia czy wczesnego dzielenia. W praktyce może to przełożyć się na bardziej niezawodną produkcję zarodków dla programów hodowlanych, wykorzystując ukierunkowany lek zamiast grubych zmian w poziomie tlenu czy bardziej toksycznych chemikaliów. Badanie podkreśla także szerszą lekcję ważną dla zabiegów płodności u ludzi: naśladowanie subtelnego, niskotlenowego środowiska jajnika nie polega jedynie na zwiększaniu lub zmniejszaniu tlenu, ale na poszanowaniu delikatnej równowagi sygnałów takich jak HIF1A. Precyzyjne dostrojenie tej równowagi, zamiast forsowania jej do skrajności, może być kluczową drogą do zdrowszych zarodków.
Cytowanie: Gübeli, M., Bleul, U. & Kowalewski, M.P. Targeted hypoxia-inducible factor 1-alpha (HIF1A) stabilization during in vitro maturation of bovine cumulus-oocyte complexes increases blastocyst rates. Sci Rep 16, 7554 (2026). https://doi.org/10.1038/s41598-025-33894-8
Słowa kluczowe: produkcja zarodków in vitro, dojrzewanie oocytów, sygnalizacja niedotlenienia, stabilizacja HIF1A, rozród bydła