Clear Sky Science · pl
CMAF-Net: fuzja uwagi międzymodalnej z regularyzacją informacyjną dla niezrównoważonej histopatologii raka piersi
Dlaczego to badanie ma znaczenie dla opieki nad pacjentkami z rakiem piersi
Patolodzy diagnozują raka piersi, analizując cienkie przekroje tkanki pod mikroskopem, lecz wyodrębnienie rzadkich, nowotworowych obszarów spośród morza zdrowych komórek jest pracochłonne i obarczone błędem. W tym badaniu przedstawiono CMAF-Net — nowy typ systemu komputerowego zaprojektowanego tak, by wykrywać więcej przypadków raka na tych obrazach przy jednoczesnym utrzymaniu niskiego poziomu fałszywych alarmów, nawet gdy próbki złośliwe są zdecydowanie mniej liczne niż zdrowe. Postępy te mogą zwiększyć niezawodność automatycznego przesiewu, wspierać przeciążonych klinicystów i stanowić wzorzec do wykrywania wielu innych rzadkich chorób.
Znajdowanie igły w stogu siana obrazów tkankowych
W rzeczywistych danych szpitalnych większość próbek tkanki piersi jest nieszkodliwa, a tylko mniejszość zawiera inwazyjny rak przewodowy — najczęstszą postać raka piersi. Taka nierównowaga sprawia, że wiele systemów sztucznej inteligencji „uczy się” po cichu, że przewidywanie tkanki zdrowej jest niemal zawsze bezpieczne, przez co przeocza groźne guzy. Jednocześnie wskazówki sugerujące złośliwość pojawiają się na bardzo różnych poziomach powiększenia — od zdeformowanych jąder pojedynczych komórek po zaburzenia struktury obejmującej całe obszary tkanki. Tradycyjne sieci do analizy obrazów dobrze radzą sobie albo ze szczegółami, albo z dużymi wzorcami, rzadko jednak łączą obie perspektywy w sposób, który wyraźnie uwypukla rzadkie, zagrażające życiu przypadki.
Mieszanie detali z szerszym kontekstem
Aby sprostać tym dwóm problemom, autorzy zaprojektowali CMAF-Net z dwoma komplementarnymi „oczami” na każdy obraz. Jedna gałąź działa jak klasyczny silnik rozpoznawania wzorców wyspecjalizowany w drobnych teksturach — kształtach i układach komórek. Druga gałąź przypomina czytelnika map, obejmując szerszą organizację tkanki za pomocą nowoczesnej architektury transformera. Zamiast jedynie nakładać te dwa widoki, system przepuszcza je przez dedykowany blok fuzji, który pozwala gałęziom wymieniać się informacjami poprzez wielokanałowe mechanizmy uwagi. Blok ten selektywnie zachowuje cechy wnoszące nowe informacje, jednocześnie tłumiąc zduplikowane lub rozpraszające sygnały, tak że ostateczna złączeniowa reprezentacja pozostaje zarówno bogata, jak i zwarta. 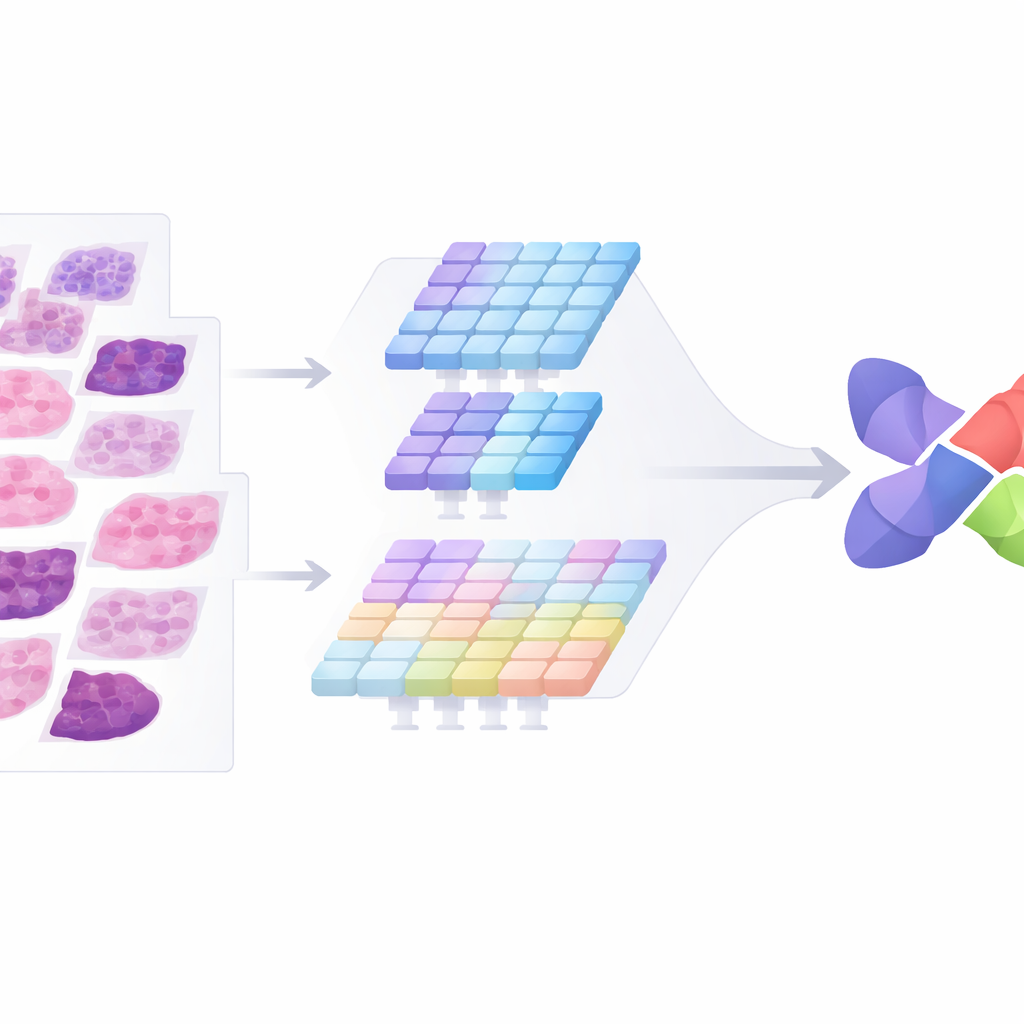
Nauczanie systemu, by zwracał uwagę na rzadkie nowotwory
Nawet sprytna architektura może faworyzować klasę większościową, dlatego badacze przeprojektowali sposób, w jaki system uczy się na podstawie popełnianych błędów. Opierając się na ideach z teorii informacji i uczenia z marginesem, opracowali regułę treningową, która wprost wymusza na modelu tworzenie szerszych „marginesów bezpieczeństwa” wokół przypadków należących do mniejszości — nowotworowych. W praktyce CMAF-Net jest bardziej karany za przeoczenie złośliwej płytki niż za błędne oznaczenie płytki jako łagodnej, a ta kara jest dostosowywana w czasie, w miarę jak przestrzeń cech dojrzewa. Sam mechanizm uwagi jest również regulowany przez swego rodzaju kontrolę „temperatury”: ostrzejsza uwaga zachowuje więcej informacji, gdy jest to potrzebne, podczas gdy łagodniejsza uwaga filtruje szum, dając modelowi zasadniczy sposób kompresji danych bez utraty sygnałów rozróżniających raka od tkanki zdrowej. 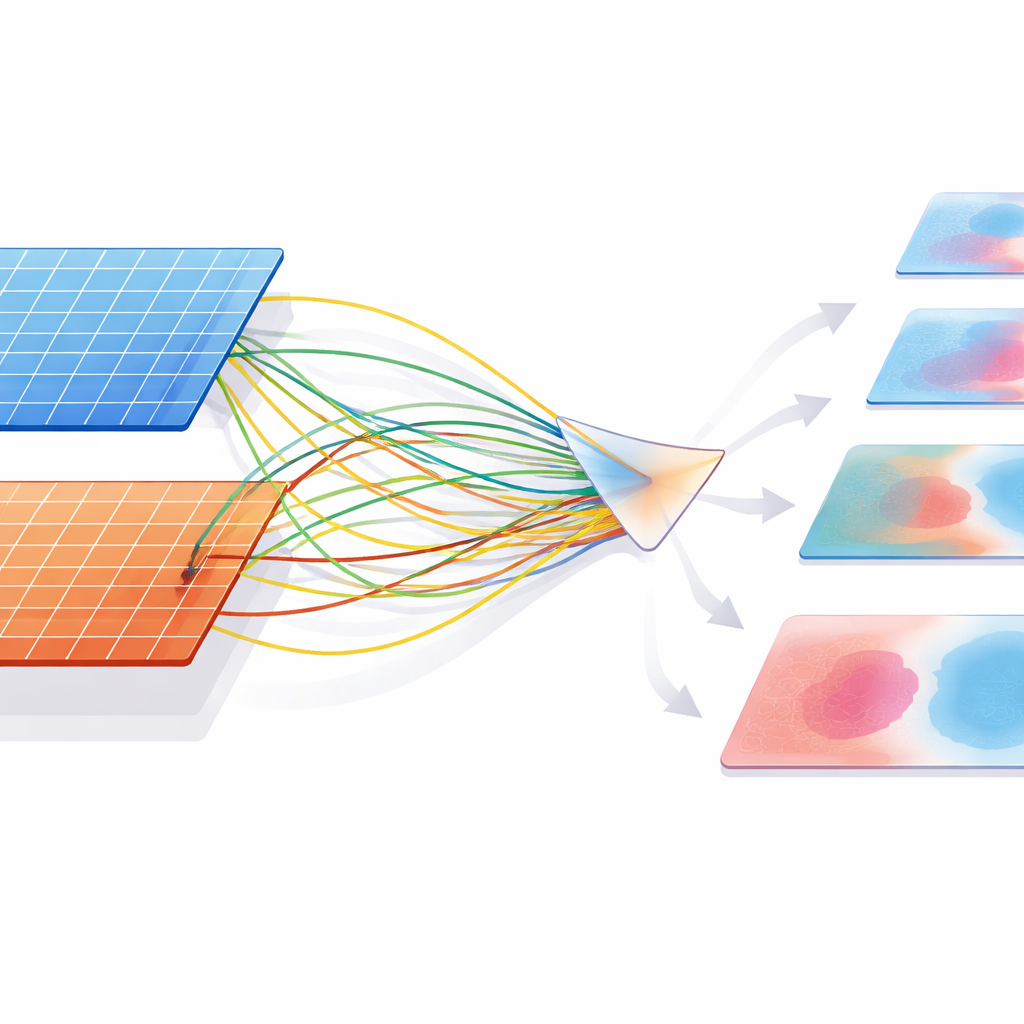
Testy metody
Zespół ocenił CMAF-Net na dużym, naturalnie niezrównoważonym zbiorze łatek tkanki piersi, gdzie około trzy czwarte było łagodnych, a reszta złośliwa. W porównaniu z szeregiem silnych systemów bazowych — w tym głębokimi sieciami splotowymi, vision transformerami i wcześniejszymi modelami fuzji dostosowanymi do nierównowagi — nowa metoda wyróżniła się. Poprawnie zidentyfikowała około 95% próbek złośliwych przy utrzymaniu podobnie wysokiej swoistości, i zrobiła to przy mniejszej liczbie parametrów niż wiele konkurencyjnych sieci fuzji. Gdy autorzy jeszcze bardziej zaburzyli proporcje danych, do poziomu jednej płytki z rakiem na dziewięćdziesiąt dziewięć łagodnych, wydajność CMAF-Net spadała stopniowo, ale pozostawała klinicznie użyteczna. Inne metody, przeciwnie, traciły większość zdolności rozpoznawania raka w tych skrajnych warunkach.
Uogólnianie między mikroskopami i typami guzów
Aby sprawdzić, czy CMAF-Net jedynie zapamiętuje jeden zbiór danych, czy uczy się bardziej uniwersalnych wzorców choroby, autorzy przetestowali go na oddzielnej kolekcji obrazów guzów piersi pochodzących od różnych pacjentów i wykonanych w czterech poziomach powiększenia. Bez żadnego ponownego trenowania model utrzymał wysoką czułość na wszystkich poziomach powiększenia i przewyższył wcześniejsze podejścia zarówno w prostych zadaniach klasyfikacji łagodne–złośliwe, jak i w trudniejszym zadaniu ośmioklasowym obejmującym różne podtypy guzów. Co istotne, CMAF-Net wykazał największe zyski w rzadkich kategoriach nowotworów, co sugeruje, że jego nacisk na efektywną informacyjnie fuzję i uczenie uwzględniające klasy pomaga wyróżniać subtelne, nietypowe wzorce, a nie tylko najbardziej typowe przypadki.
Znaczenie na przyszłość
Dla laików kluczowe przesłanie jest takie, że CMAF-Net oferuje inteligentniejszy sposób, w jaki komputery „czytają” preparaty patologiczne: jednocześnie patrzy blisko i szeroko, uczy się zwracać dodatkową uwagę na rzadkie, lecz niebezpieczne znaki raka i działa nawet wtedy, gdy przykładów złośliwych jest niewiele. Poza rakiem piersi te same zasady projektowe mogą kierować tworzeniem narzędzi do wykrywania rzadkich chorób w różnych typach obrazów medycznych, dostarczając lekarzom bardziej godną zaufania drugą opinię i potencjalnie umożliwiając wcześniejsze, dokładniejsze diagnozy pacjentkom, które najbardziej tego potrzebują.
Cytowanie: Ativi, W.X., Chen, W., Kwao, L. et al. CMAF-Net: cross-modal attention fusion with information-theoretic regularization for imbalanced breast cancer histopathology. Sci Rep 16, 9607 (2026). https://doi.org/10.1038/s41598-025-32794-1
Słowa kluczowe: rak piersi, histopatologia AI, nierównowaga klas, uczenie głębokie, analiza obrazów medycznych