Clear Sky Science · pl
Wielofunkcyjne pochodne pektyny jako środki przeciwnowotworowe w raku jelita grubego: synteza, wnioski obliczeniowe i modulacja szlaków sygnałowych NRF2/HO-1, HIF-1α oraz VEGF/PDGF-D
Od włókna owocowego do cząsteczek walczących z rakiem
Pektyna to naturalne włókno najbardziej znane z zagęszczania dżemów i galaretek, lecz ten codzienny składnik kuchenny może także być cichym sojusznikiem w walce z rakiem. W badaniu tym zbadano, jak naukowcy mogą precyzyjnie modyfikować strukturę pektyny, aby otrzymać nowe związki, które w laboratorium hamują wzrost komórek raka jelita grubego, jednocześnie osłabiając szkodliwy stres oksydacyjny i odcinając dopływ krwi niezbędny do wzrostu guza.
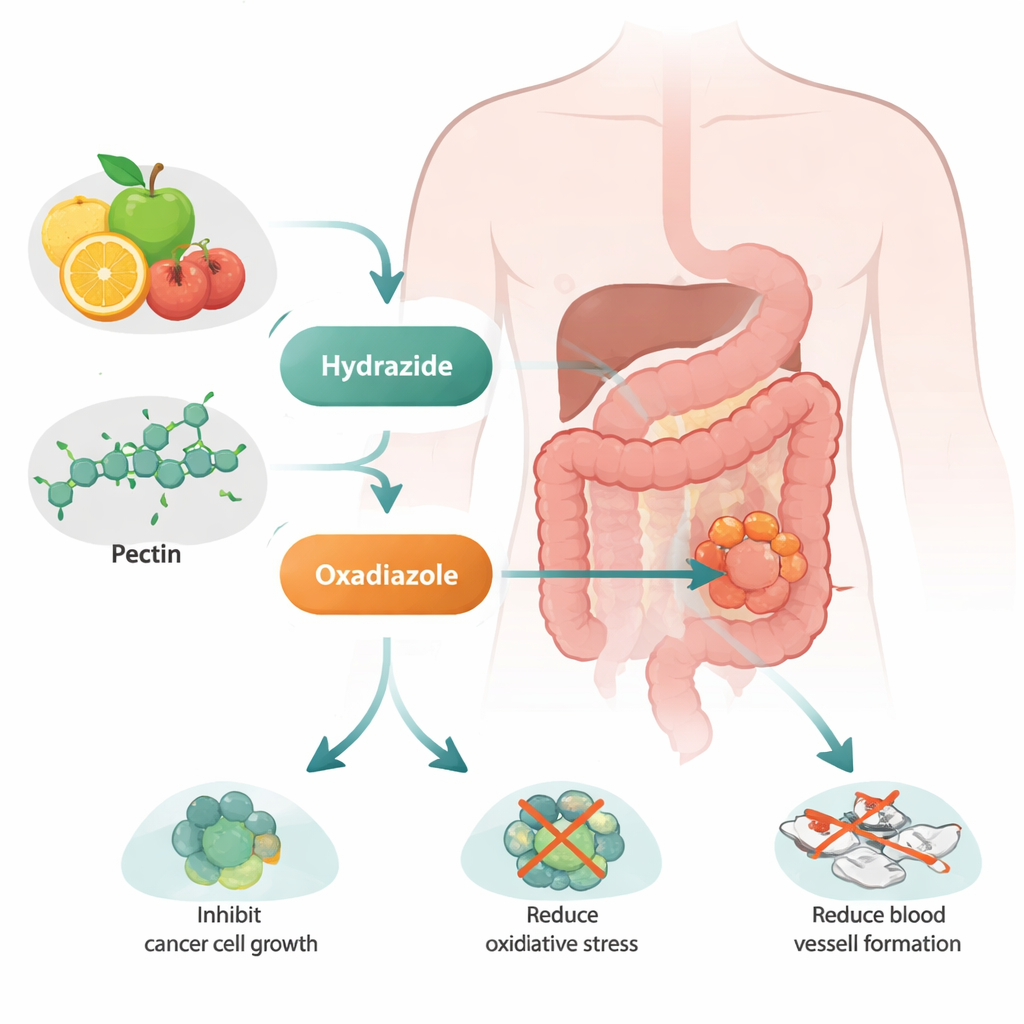
Przekształcanie powszechnego włókna w inteligentnego kandydata na lek
Naukowcy zaczęli od zwykłej pektyny, łańcucha cukrowego pochodzenia roślinnego występującego w wielu owocach. Przy użyciu serii kontrolowanych reakcji chemicznych przekształcili pektynę w dwie nowe formy nazwane „pektyna hydrazydowa” i „pektyna oksadiazolowa”. Choć nazwy brzmią technicznie, pomysł jest prosty: przez przyłączenie niewielkich grup zawierających azot i siarkę do pektyny nadano cząsteczce nowe właściwości elektroniczne i strukturalne, które mogłyby zwiększyć jej aktywność przeciwnowotworową. Zaawansowane narzędzia, takie jak spektroskopia w podczerwieni, magnetyczny rezonans jądrowy, mikroskopia elektronowa i testy odporności termicznej potwierdziły, że reakcje przebiegły prawidłowo, a nowe materiały są bardziej termicznie stabilne niż pierwotna pektyna.
Testowanie nowych związków na komórkach nowotworowych
Aby sprawdzić, czy zmodyfikowane włókna mogą zaszkodzić komórkom nowotworowym, zespół poddał dwie ludzkie linie komórkowe — jedną pochodzącą z raka wątroby i jedną z raka jelita grubego — działaniu różnych dawek nowych związków. Zastosowano test barwnikowy mierzący, ile komórek pozostaje żywych po leczeniu. Zarówno pektyna hydrazydowa, jak i pektyna oksadiazolowa były skuteczniejsze niż niemodyfikowana pektyna w zmniejszaniu przeżywalności komórek raka jelita grubego (Caco2), przy czym najsilniejszy efekt wykazywała pektyna oksadiazolowa. W stosunku do komórek raka wątroby związki te były mniej aktywne, ale nadal wykazywały mierzalne działanie, co sugeruje, że nowe struktury są szczególnie obiecujące w kierunku guzów jelita grubego.
Obniżanie stresu oksydacyjnego i odcięcie dopływu krwi do guza
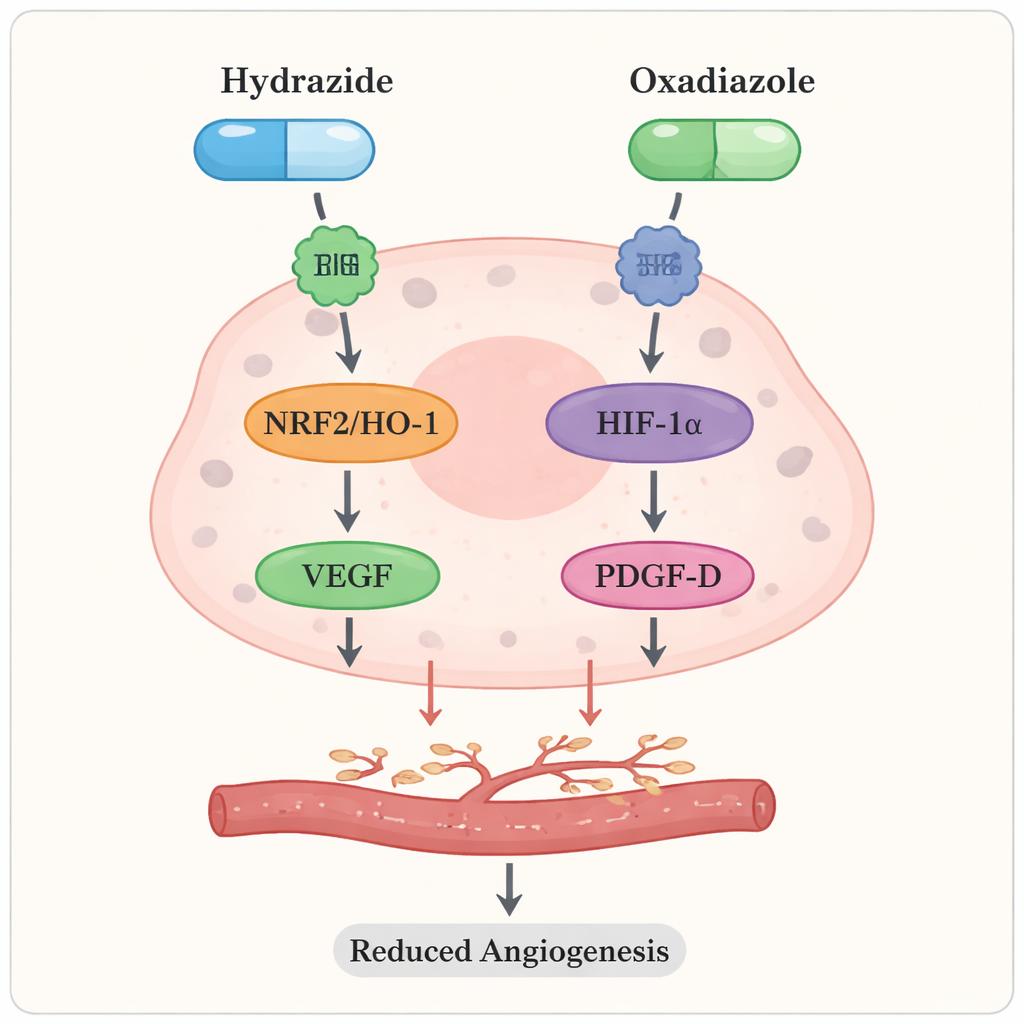
Nowotwór nie rozwija się w izolacji; napędzają go stres chemiczny i nieprawidłowe sygnalizowanie wewnątrzkomórkowe. Badacze skupili się na reaktywnych formach tlenu (ROS) — wysoce reaktywnych cząsteczkach mogących uszkadzać DNA i napędzać wzrost guza — oraz na białkach pomagających nowotworom adaptować się do stresu i tworzyć nowe naczynia krwionośne. Gdy komórki Caco2 leczono nowymi pochodnymi pektyny w dawkach aktywnych, poziomy ROS spadły, a ilość enzymu przeciwutleniającego HO‑1 również zmniejszyła się. Na poziomie genetycznym kluczowe „główne przełączniki” takie jak NRF2 i HIF‑1α, wraz z czynnikami promującymi tworzenie naczyń VEGF i PDGF‑D, zostały stłumione. Prościej mówiąc, zmodyfikowane pektyny nie tylko bezpośrednio uszkadzały komórki nowotworowe, lecz także łagodziły wewnętrzne sygnały stresowe i ograniczały instrukcje nakazujące guzom tworzyć nowe naczynia krwionośne.
Wykorzystanie modeli komputerowych, by zrozumieć mechanizm działania
Aby głębiej zbadać, jak i dlaczego te cząsteczki są tak aktywne, zespół sięgnął po symulacje komputerowe. Wirtualnie „zadokowali” pektynę, pektynę hydrazydową i pektynę oksadiazolową do kilku struktur białkowych powiązanych z wzrostem nowotworu, odpowiedzią na stres i tworzeniem naczyń. We wszystkich tych celach pektyna oksadiazolowa miała tendencję do najlepszego dopasowania, tworząc najsilniejsze i najstabilniejsze interakcje. Długie symulacje komputerowe śledzące ruch atomów przez 100 nanosekund potwierdziły ten obraz: forma oksadiazolowa mocniej wiązała się ze swoimi celami i stabilizowała ich struktury bardziej niż hydrazyd lub niemodyfikowana pektyna. Obliczenia kwantowo‑chemiczne dodatkowo wykazały, że dodanie pierścieni zawierających azot i siarkę zmienia rozkład elektronów w cząsteczce, czyniąc ją bardziej reaktywną w sposób sprzyjający silnemu wiązaniu z partnerami biologicznymi.
Co to może oznaczać dla przyszłych terapii przeciwnowotworowych
Podsumowując, badanie pokazuje, że znane włókno pokarmowe można przekształcić w coś znacznie więcej niż składnik przyjazny jelitom. Poprzez staranne przeprojektowanie struktury pektyny badacze stworzyli nowe związki, które atakują komórki raka jelita grubego na kilku frontach jednocześnie: spowalniają wzrost komórek, zmniejszają szkodliwy stres oksydacyjny i osłabiają sygnały napędzające tworzenie nowych naczyń krwionośnych. Choć ustalenia te pochodzą wciąż z badań na hodowlach komórkowych i modelach komputerowych — i muszą zostać przetestowane na komórkach prawidłowych oraz w modelach zwierzęcych przed zastosowaniem u ludzi — wskazują one na pektynę hydrazydową, a szczególnie pektynę oksadiazolową, jako obiecujące punkty wyjścia do opracowania bezpieczniejszych, wielofunkcyjnych leków przeciw rakowi jelita grubego.
Cytowanie: Elsayed, G.H., Fahim, A.M. Multifunctional pectin derivatives as anticancer agents in colorectal cancer via synthesis, computational insights, and modulation of NRF2/HO-1, HIF-1α, and VEGF/PDGF-D signaling pathways. Sci Rep 16, 6542 (2026). https://doi.org/10.1038/s41598-025-32107-6
Słowa kluczowe: pektyna, rak jelita grubego, stres oksydacyjny, angiogeneza, projektowanie leków