Clear Sky Science · pl
Pośrednie struktury G-quadrupleksów telomerowych ujawnione przez złożoną analizę sieci Markowa
Ukryte supły na końcach naszego DNA
Na końcach naszych chromosomów znajdują się ochronne nasadki zwane telomerami, często porównywane do plastikowych końcówek sznurówek. W tych regionach DNA może zawiązywać się w nietypowe, czteroniciowe supły zwane G-quadrupleksami. Te drobne struktury wpływają na zachowanie genów oraz na starzenie się komórek lub ich przemianę nowotworową. W badaniu zaprezentowano mechanizm stopniowego rozpadu jednego z takich supłów, wykorzystując szczegółowe symulacje komputerowe i zaawansowaną analizę danych, aby wydobyć efemeryczne kształty niemal niemożliwe do uchwycenia eksperymentalnie.
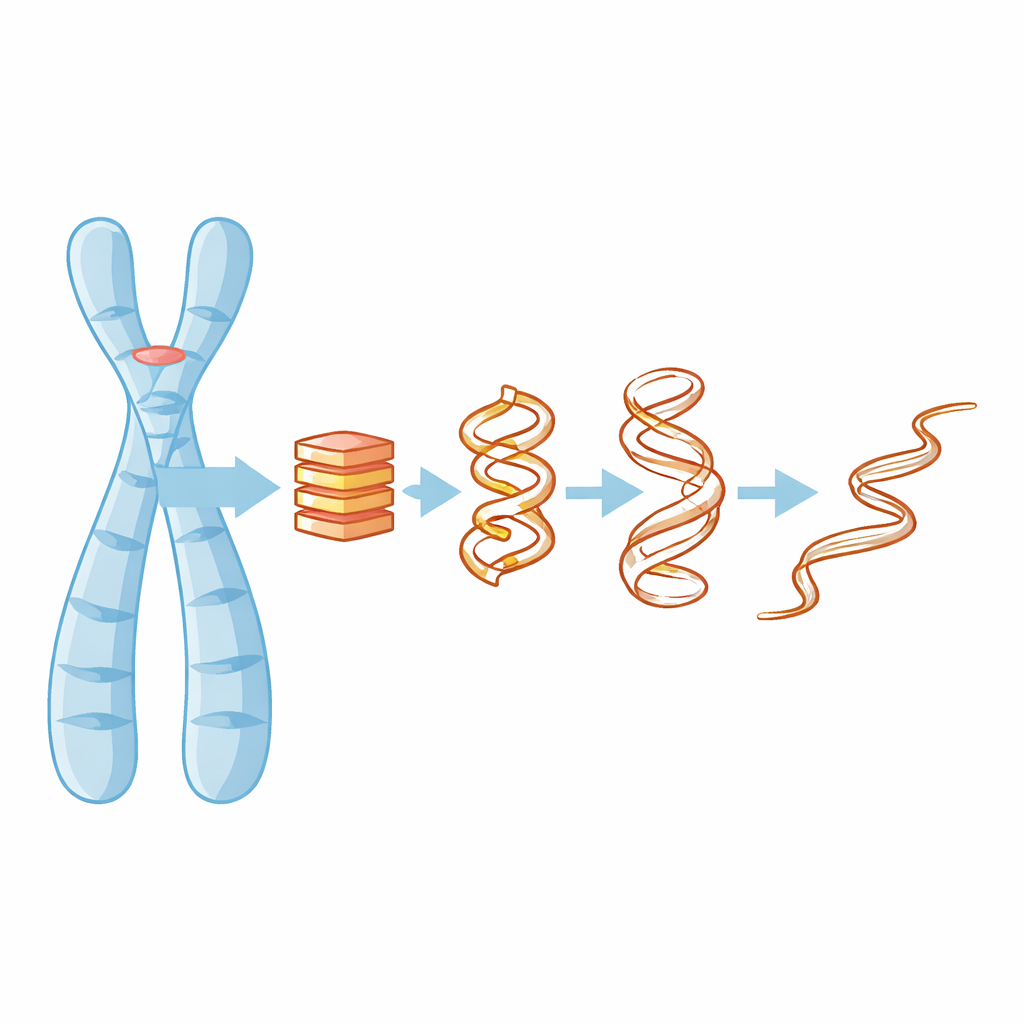
Dlaczego czteroniciowe supły DNA mają znaczenie
Większość z nas uczy się, że DNA to podwójna helisa, ale w odcinkach bogatych w guaninę — takich jak telomery — cząsteczka może składać się w zwarte, czteroniciowe układy zwane G-quadrupleksami. Układy te są utrzymywane przez płaskie warstwy zasad guaninowych oraz niewielkie, dodatnio naładowane jony, np. potasu, które zajmują środkowy kanał i stabilizują strukturę. Powstawanie lub rozpad G-quadrupleksu może blokować lub odsłaniać fragmenty genomu, wpływając na aktywność genów, replikację DNA, a nawet na sposób, w jaki komórki nowotworowe utrzymują telomery. Zrozumienie, jak te struktury tracą swoją formę, jest zatem kluczowe dla opracowania leków je celujących lub przewidywania momentów ich destabilizacji.
Obserwowanie, jak molekularny supł się rozplątuje
Naukowcy skupili się na ludzkim telomerowym G-quadrupleksie, w którym cztery segmenty jednej nici DNA układają się równolegle i stapiają w zwartą kolumnę. Zastosowali symulacje dynamiki molekularnej w pełnym składzie atomowym — wirtualne eksperymenty śledzące ruch każdego atomu — podnosząc temperaturę ośmiu kopii tej struktury do wartości bliskich punktowi topnienia. Aby pomóc układowi w eksploracji różnych kształtów, użyli strategii zwanej wymianą replik (replica exchange), gdzie symulacje przy różnych temperaturach okazjonalnie zamieniają konfiguracje. W siedmiu z ośmiu przypadków G-quadrupleks pozostał złożony; w jednym wypadku całkowicie się rozwinął. To rzadkie zdarzenie rozpadu stało się przedmiotem szczegółowego studium, pokazując nie tylko stan początkowy i końcowy, lecz cały ciąg pośrednich kształtów.
Kluczowa rola maleńkich jonów
Centralnym odkryciem jest to, że małe jony wewnątrz G-quadrupleksu działają jak zawiasy bezpieczeństwa. Dopóki przynajmniej jeden jon pozostaje osadzony między warstwami guanin, struktura pozostaje w dużej mierze nienaruszona — może nieco poluzowana, ale wciąż rozpoznawalna. Gdy jednak oba jony opuszczają centralny kanał, stos szybko się destabilizuje. Warstwy guanin ulegają odkształceniu, pojedyncze nici odchodzą, a całość DNA staje się bardziej wydłużona i elastyczna. Inne symulowane molekuły, które straciły tylko jeden jon, weszły w chwiejne, lecz częściowo uporządkowane stany, co sugeruje, że pełny rozpad wymaga utraty obu jonów stabilizujących — wskazówka, dlaczego niektóre G-quadrupleksy są w komórce wyjątkowo trwałe.
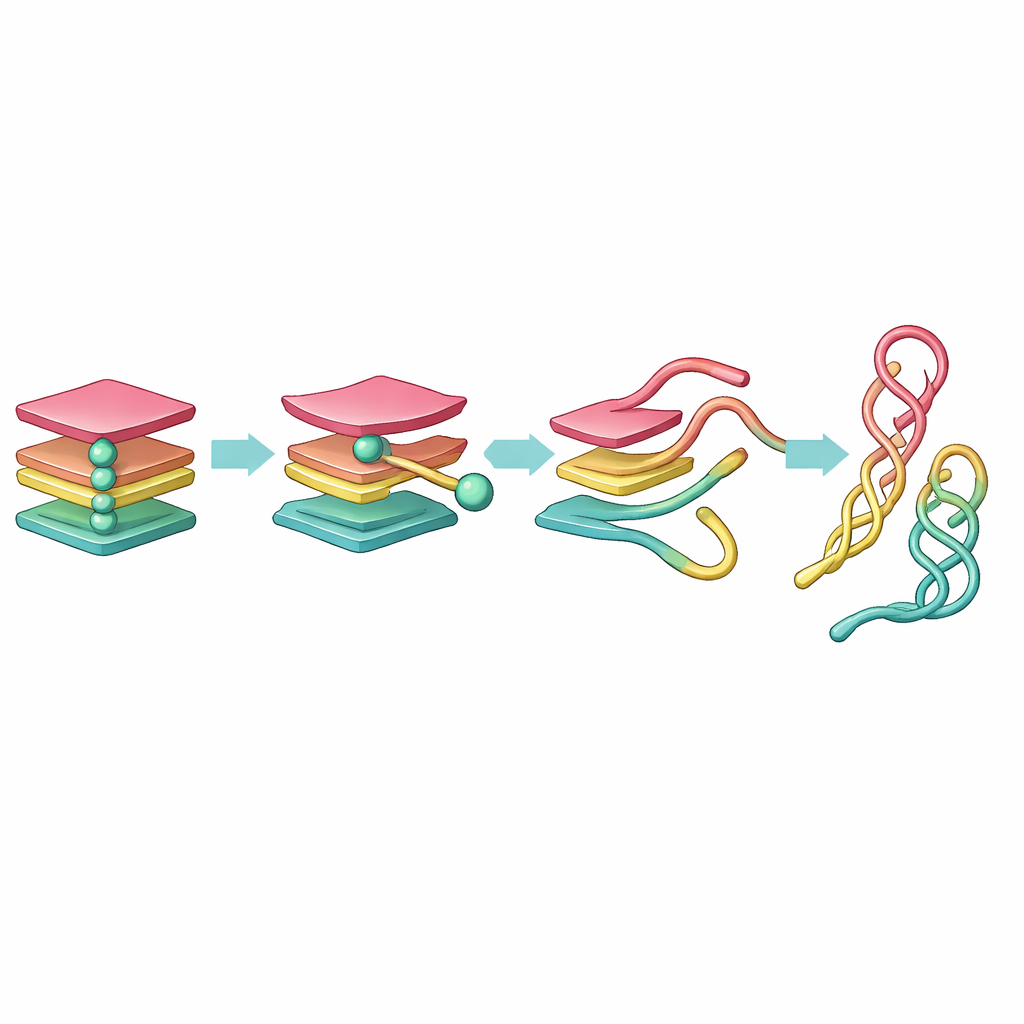
Odkrywanie ukrytych punktów pośrednich w tym procesie
Surowe dane z symulacji były ogromne i zbyt złożone, by interpretować je wzrokiem. Aby je okiełznać, zespół najpierw uprościł DNA, reprezentując każdą zasadę jako pojedynczy punkt, a następnie zastosował narzędzia matematyczne do sprowadzenia ruchu do kilku kluczowych współrzędnych. Wykorzystali dwie metody: analizę głównych składowych (PCA), która uwypukla kierunki największego ruchu, oraz analizę składowych niezależnych w czasie (tICA), która filtruje wolne, długotrwałe zmiany oznaczające rzeczywiste przesunięcia strukturalne. Z tych zredukowanych współrzędnych zbudowali tak zwane konformacyjne sieci Markowa, w których każdy węzeł reprezentuje typowy kształt DNA, a łącza pokazują, jak cząsteczka przeskakuje między kolejnymi formami.
Preferowana trasa od supła do luźnej nici
Widok sieci ujawnił wyraźną ścieżkę rozpadu. Z pełni złożonego G-quadrupleksu najpierw odłącza się jedna nić, tworząc trójniciowy stan „triplex”. Ten triplex reorganizuje się następnie w dwuniciowy „hairpin” (zamknięcie) oraz zestaw okolicznych luźnych nici. Hairpin i pokrewny układ „cross-hairpin” okazują się zaskakująco długowieczne, pełniąc rolę stabilnych punktów na trasie od ciasnego supła do bardziej rozluźnionej konfiguracji DNA. Podczas gdy PCA rozdzieliła ten postęp na wiele podobnych stanów, tICA sprowadziła go do niewielkiego zestawu odrębnych, kinetycznie istotnych kroków, pokazując, że kształty przypominające triplex są krótkotrwałe, natomiast formy przypominające hairpin utrzymują się znacznie dłużej.
Znaczenie dla biologii i medycyny
Dla nietechnicznego odbiorcy kluczowy wniosek jest taki, że telomerowe G-quadrupleksy nie przełączają się po prostu nagle z postaci złożonej na rozwiniętą. Zamiast tego „topnieją” przez serię krótkotrwałych i dłużej trwających kształtów, przy czym drobne jony pełnią rolę strażników stabilności. Symulacje sugerują, że trójniciowe pośrednie formy są ulotne, natomiast dwuniciowe hairpiny i formy krzyżowe stanowią bardziej stabilne punkty spoczynkowe. Ponieważ stany pośrednie mogą pojawiać się także w odwrotnym kierunku, podczas składania, prawdopodobnie odgrywają kluczową rolę w formowaniu, przemianach i interakcjach G-quadrupleksów z potencjalnymi lekami. Mapowanie tego ukrytego krajobrazu kształtów przybliża naukowców do projektowania molekuł, które selektywnie stabilizują lub destabilizują te supły DNA w walce z rakiem i innymi chorobami.
Cytowanie: Sáinz-Agost, A., Falo, F. & Fiasconaro, A. Telomeric G-quadruplex intermediates unveiled by complex Markov network analysis. Sci Rep 16, 8308 (2026). https://doi.org/10.1038/s41598-025-29993-1
Słowa kluczowe: G-quadruplex, DNA telomerowe, dynamika molekularna, składanie DNA bez białek, terapie przeciwnowotworowe