Clear Sky Science · pl
HMI-LUSC: Zestaw danych obrazowania hiperspektralnego histologii raka płaskonabłonkowego płuca
Widząc raka w nowych barwach
Rak płuca pozostaje jedną z najbardziej śmiertelnych chorób na świecie, częściowo dlatego, że wykrycie każdej ostatniej komórki nowotworowej na szkiełku mikroskopowym jest trudne i czasochłonne. Patolodzy zwykle polegają na tkance wybarwionej na różowo i fioletowo oglądanej pod mikroskopem — metoda ta oddaje strukturę, ale pomija subtelne wskazówki chemiczne. W artykule przedstawiono HMI-LUSC, pierwszą publicznie dostępną kolekcję obrazów mikroskopowych raka płaskonabłonkowego płuca zarejestrowanych nie tylko w trzech barwach, lecz w kilkudziesięciu wąskich pasmach spektralnych, dając komputerom i klinicystom znacznie bogatszy wgląd w to, co odróżnia komórki nowotworowe od ich zdrowych sąsiadów.
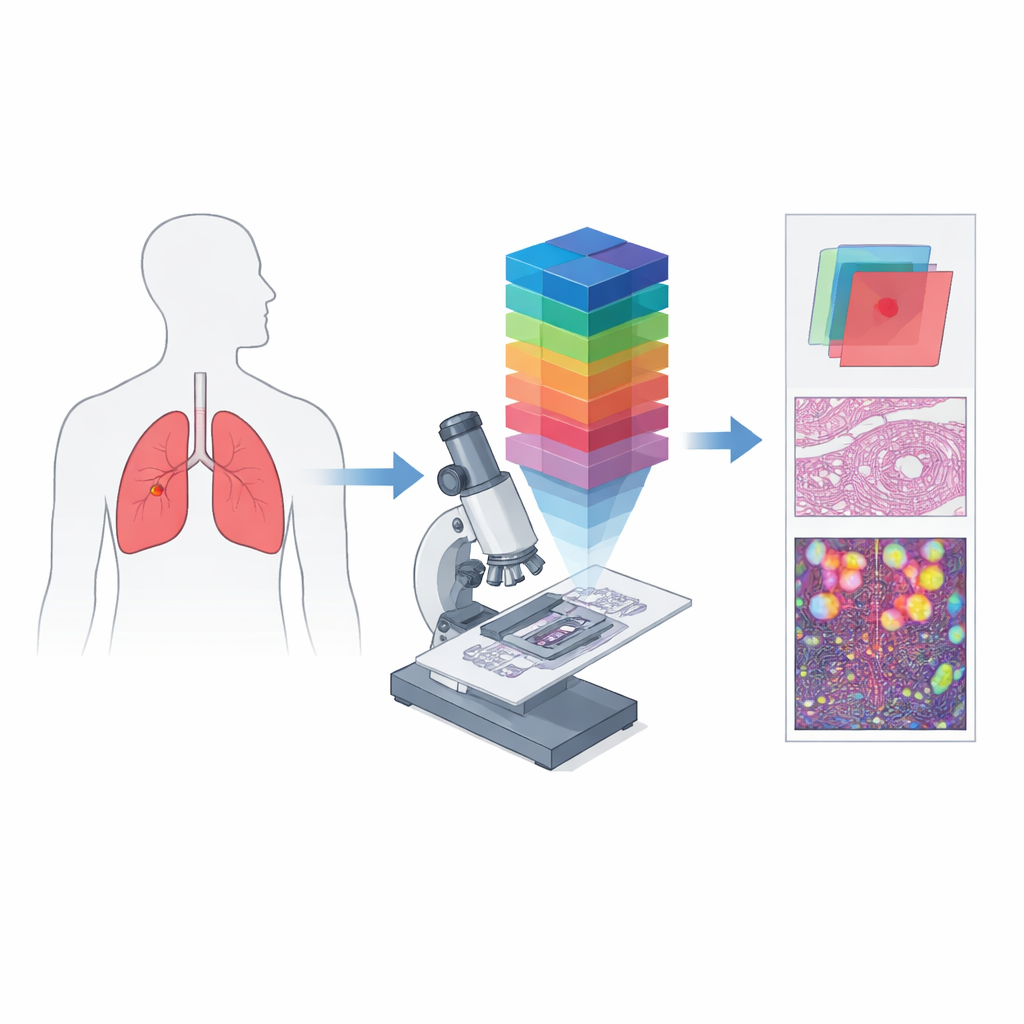
Od prostych zdjęć kolorowych do spektralnych odcisków palców
Konwencjonalna patologia cyfrowa działa podobnie jak aparat w telefonie: rejestruje kanały czerwony, zielony i niebieski, by przybliżyć to, co widzi oko. Obrazowanie hiperspektralne idzie kilka kroków dalej, rozdzielając światło na wiele blisko położonych długości fal i tworząc trójwymiarową „kostkę danych”, w której każde maleńkie miejsce tkanki ma własne szczegółowe widmo kolorów. Połączenie tej idei z mikroskopem daje hiperspektralne obrazowanie mikroskopowe, zdolne uchwycić zarówno drobne struktury, jak i bogate informacje spektralne na poziomie pojedynczych komórek. Takie dane mogą ujawnić różnice w tym, jak tkanki absorbują i odbijają światło — niewidoczne na standardowych obrazach — tworząc unikatowe spektralne „sygnatury” dla obszarów nowotworowych i nienowotworowych.
Budowanie nowej biblioteki do badań nad rakiem płuca
Autorzy stworzyli HMI-LUSC, aby wypełnić wyraźną lukę: przed tym projektem nie istniał publiczny zestaw hiperspektralnych obrazów preparatów raka płuca, co utrudniało testowanie i porównywanie metod diagnostycznych opartych na komputerach. Zebrali tkanki od dziesięciu pacjentów poddawanych operacji usunięcia guza płuca, przygotowali standardowe szkiełka wybarwione hematoksyliną i eozyną i zeskanowali je w wysokiej rozdzielczości. Doświadczeni patolodzy oznaczyli obszary nowotworowe i prawidłowe, a reprezentatywne regiony zostały ponownie zarejestrowane za pomocą niestandardowego mikroskopu hiperspektralnego. Każdy uzyskany obraz obejmuje niewielki fragment tkanki, ale rozciąga się na 61 długości fal w zakresie 450–750 nanometrów, przy rozdzielczości 3088 na 2064 pikseli. Dla każdego regionu zestaw danych zawiera surową kostkę spektralną, konwencjonalne odwzorowanie RGB oraz maski wyznaczające obecność tkanki nowotworowej.
Przekształcanie zgrubnych obrysów w mapy na poziomie komórek
Chociaż oznaczenia na poziomie preparatu są użyteczne, trenowanie nowoczesnych algorytmów często wymaga informacji na poziomie pojedynczych komórek. Ręczne obrysowywanie każdej komórki jest niepraktyczne, więc zespół opracował półautomatyczny przepływ pracy. Najpierw pogrupowano piksele w klastry na podstawie podobieństwa ich widm przy użyciu standardowej metody widzenia komputerowego. Następnie patolodzy sprawdzali te klastry nałożone na obraz tkanki i przypisywali je do czterech kategorii: komórki nowotworowe, komórki nienowotworowe, tkanka niekomórkowa taka jak zrąb czy krew oraz puste tło. Drugi patolog dokonał przeglądu i korekt, a niezgodności rozstrzygano konsensusem. Wynikiem jest zestaw szczegółowych masek piksel-piksel, które uchwytują subtelne mieszanki typów komórek i mylące strefy brzegowe, dostarczając znacznie bogatszych materiałów szkoleniowych dla systemów uczących się.
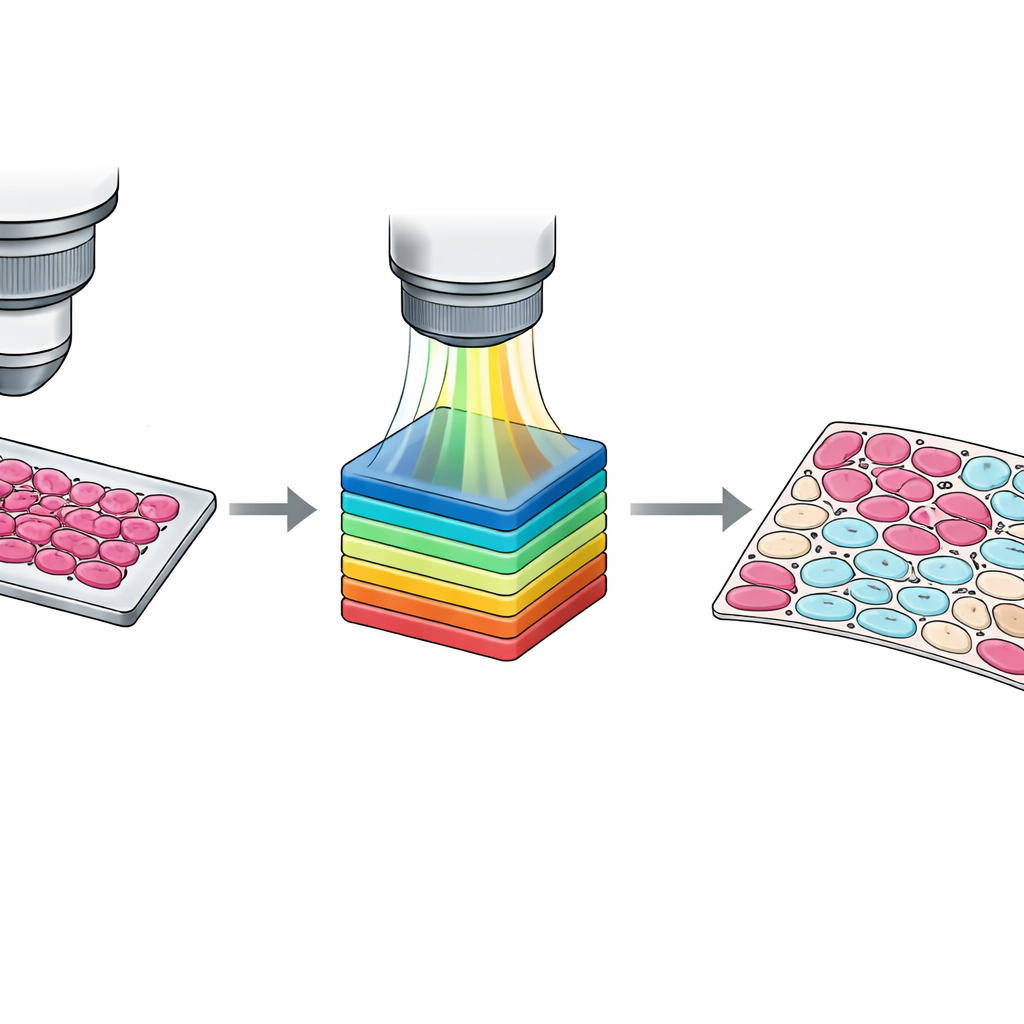
Zapewnienie ostrości i wiarygodności danych
Aby zestaw danych był godny zaufania, autorzy dokładnie przetestowali swój system obrazowania. Zweryfikowali, że mikroskop może rozróżniać drobne struktury osiągające około jednego mikrometra — wystarczająco mało, by odróżnić pojedyncze komórki — oraz że szumy obrazowe są niskie w większości długości fal. Porównali także zmierzone widmo standardowego źródła światła z krzywymi referencyjnymi i z komercyjną kamerą hiperspektralną, znajdując doskonałą zgodność. Wreszcie pokazali, jak dane można wykorzystać, uruchamiając bazowe modele komputerowe — od klasycznych metod uczenia maszynowego po proste sieci głębokiego uczenia — do segmentacji obszarów nowotworowych. Nawet bez intensywnej optymalizacji modele te osiągnęły solidną dokładność, co pokazuje, że zestaw danych nadaje się na punkt odniesienia dla przyszłych metod.
Co to oznacza dla przyszłej opieki nad rakiem płuca
HMI-LUSC nie zastępuje dużych kolekcji standardowych preparatów ani nie jest jeszcze samodzielnym narzędziem klinicznym. Zamiast tego oferuje badaczom starannie wyselekcjonowane okno na to, jak komórki guza płuca różnią się od sąsiedniej tkanki w wielu długościach fal. Udostępniając te dane, etykiety i kod otwarcie, autorzy zapewniają wspólne pole testowe do rozwijania i porównywania algorytmów wykorzystujących informacje spektralne — od prostych klasyfikatorów po zaawansowane sieci neuronowe. W dłuższej perspektywie taka praca może pomóc komputerom wspierać patologów w dokładniejszym i szybszym wykrywaniu guzów oraz odsłonić wzorce spektralne związane z typem guza lub odpowiedzią na leczenie, których zwykłe obrazy nie potrafią ukazać.
Cytowanie: Yan, Z., Huang, H., Guo, Y. et al. HMI-LUSC: A Histological Hyperspectral Imaging Dataset for Lung Squamous Cell Carcinoma. Sci Data 13, 415 (2026). https://doi.org/10.1038/s41597-026-06766-7
Słowa kluczowe: obrazowanie hiperspektralne, rak płuca, patologia cyfrowa, segmentacja guza, zestaw danych obrazów medycznych