Clear Sky Science · pl
Mapowanie chimerycznych elementów transpozon–gen, ich powstawanie i rola w zwiększaniu plastyczności transkryptomu
Ukryci pasażerowie w naszym DNA
Dużą część naszego DNA stanowią starożytni wirusowi pasażerowie zwani elementami transpozonowymi — fragmenty kodu genetycznego, które kiedyś przeskakiwały po genomach niczym pasożytniczy autostopowicze. To badanie pokazuje, że te dawne wirusowe odłamki nie są jedynie cichym śmieciem: mogą łączyć się z naszymi genami, tworząc hybrydowe komunikaty, pomagać komórkom przystosowywać się do zmieniających się warunków, a czasem napędzać choroby. Mapując te chimery w przebiegu rozwoju, starzenia się i raka, autorzy ujawniają zaskakujący sposób, w jaki wirusowe DNA nadal kształtuje ludzką biologię dziś.
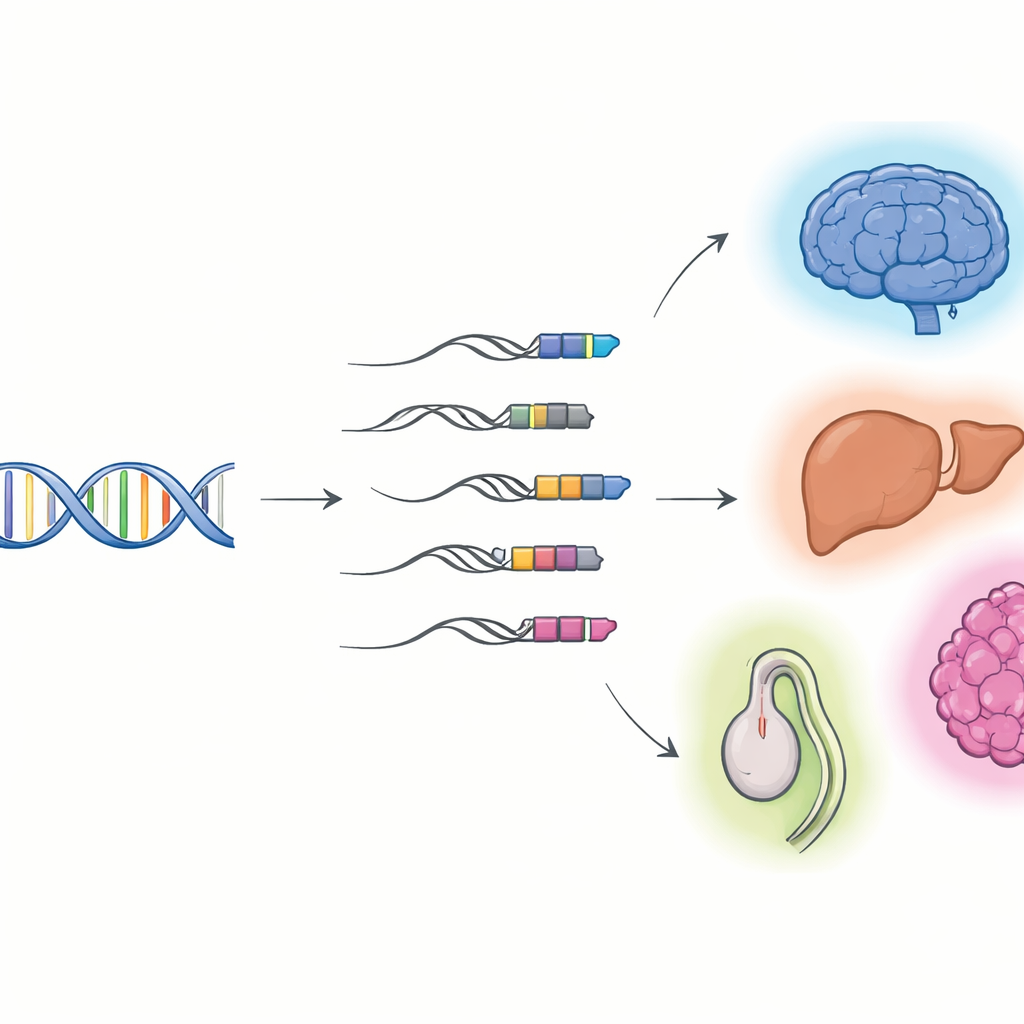
Kiedy wirusowe DNA staje się częścią naszych genów
Naukowcy skupili się na „chimera–TE–gen”: cząstkach RNA, które zaczynają się w elemencie transpozonowym, a następnie ciągną się w obrębie genu gospodarza. Wykorzystując sekwencjonowanie długich odczytów, które może uchwycić całe cząsteczki RNA od końca do końca, w połączeniu ze standardowym sekwencjonowaniem krótkich odczytów, zbudowali szczegółowe katalogi tych hybryd w komórkach i narządach myszy oraz człowieka. Odkryli tysiące wcześniej nieznanych transkryptów chimerycznych, z których większość to RNA niekodujące, a nie plany białek. Wiele zaczyna się w klasie wirusowych pozostałości zwanych długimi powtórzeniami końcowymi (LTR), które często znajdują się na początku genów i mogą działać jak alternatywne przełączniki włącz/wyłącz. Różne tkanki i narządy używają różnych zestawów tych chimer, szczególnie intensywnie w mózgu, wątrobie i jądrach, a ich wykorzystanie zmienia się w miarę rozwoju tkanek od fazy płodowej do dorosłej.
Chimery w starzeniu i raku
Aby sprawdzić zachowanie tych wirusowo–gospodarczych hybryd w populacjach, zespół przeanalizował duże ludzkie zbiory danych obejmujące dziesiątki tkanek od setek osób oraz próbki nowotworowe. Zidentyfikowali kilkaset chimerycznych transkryptów o wysokim poziomie ufności, które powtarzają się między osobnikami. Ich ekspresja różni się nie tylko między narządami, ale także z wiekiem: w tkankach takich jak krew i mózg niektóre chimery napędzane przez LTR maleją u starszych dorosłych, podczas gdy w pewnych tkankach obwodowych wzrastają. W wielu typach raka te LTR-zależne hybrydy są powszechnie podwyższone w guzach w porównaniu z pobliską tkanką normalną, a pacjenci, których guzy wyrażają ich więcej, zwykle mają gorsze rokowania. W zbiorach danych od osób opornych na chemioterapię lub immunoterapię, geny dotknięte nowymi eksonami napędzanymi przez LTR często biorą udział w ścieżkach związanych z mechanizmem działania tych leków, co sugeruje, że chimery TE mogą pomagać guzom przeorganizować się pod presją terapii.
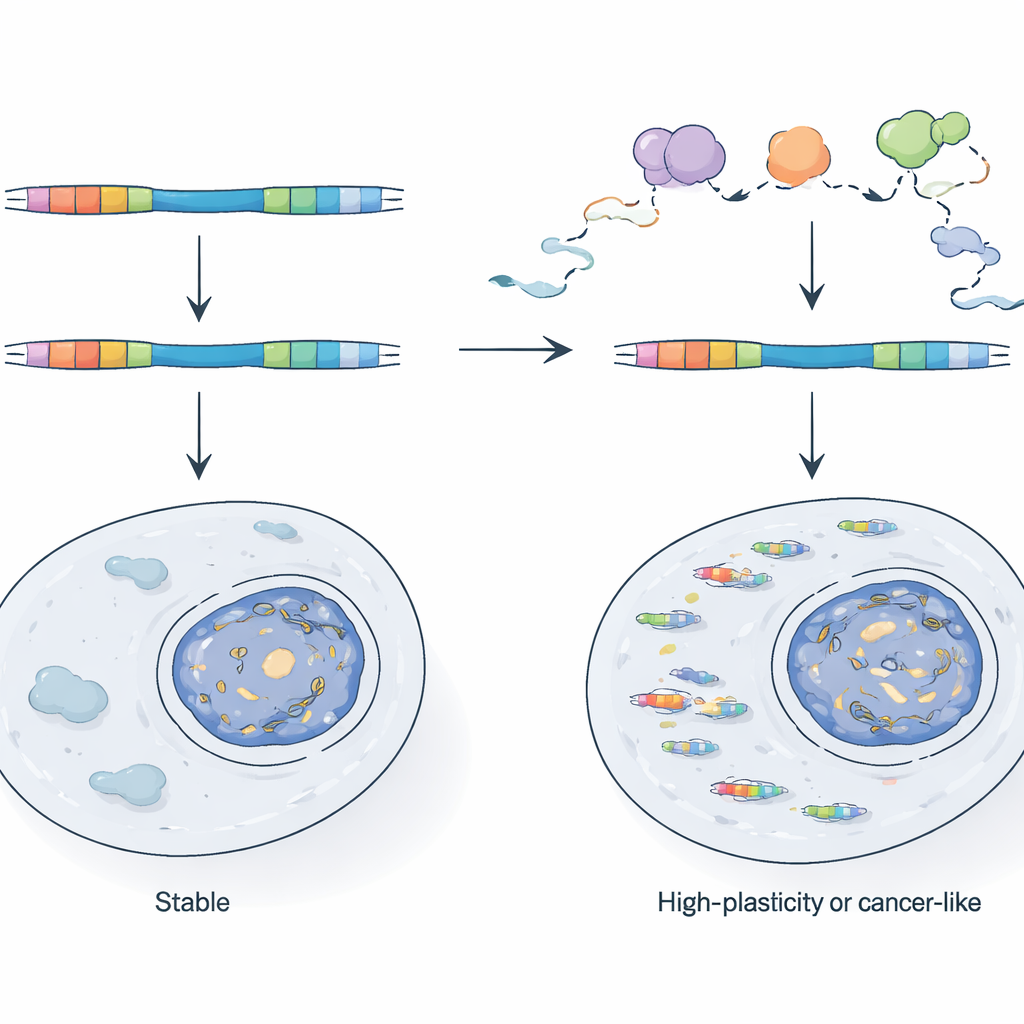
Jak komórki powstrzymują wirusowe hybrydy
Biorąc pod uwagę ich potencjał, dlaczego chimery TE nie zalewają normalnych komórek? Autorzy pokazują, że komórki polegają na systemie kontroli jakości RNA, koncentrującym się na kompleksie egzosomu jądrowego, by patrolować i niszczyć wiele z tych transkryptów w trakcie ich powstawania. Gdy genetycznie uszkadzają kluczowy składnik egzosomu w komórkach macierzystych myszy, promotory napędzane przez LTR stają się znacznie bardziej aktywne, a chimeryczne RNA lawinowo rosną. Porównując świeżo syntetyzowane RNA z trwałym RNA, pokazują, że niektóre LTR są normalnie tłumione, ponieważ ich transkrypty są szybko degradowane, podczas gdy inne są kontrolowane na poziomie częstości inicjacji transkrypcji. Aktywne LTR mają tendencję do lokalizowania się w regionach genomu już dostępnych i często transkrybowanych, co wskazuje, że samo znajdowanie się blisko aktywnego genu lub transkryptu antysensowego może pomóc wirusowemu fragmentowi uwolnić się od tradycyjnego wyciszenia epigenetycznego.
Splicing, plastyczność komórek macierzystych i wirusowy „główny wyłącznik”
Obraz staje się bardziej złożony, gdy zaburzona zostaje machineria splicingowa komórki. Autorzy wyciszają kilka podstawowych czynników splicingowych lub chemicznie hamują spliceosom i obserwują wspólny skutek z utratą egzosomu: silne zwiększenie chimerycznych transkryptów napędzanych przez LTR oraz krótkich genów ubogich w introny. Wśród wyraźnych aktywowanych jest MERVL, endogenny retrowirus aktywny we wczesnych zarodkach myszy. Gdy wewnętrzna sekwencja MERVL i powiązane czynniki transkrypcyjne są nadmiernie aktywowane, komórki macierzyste przesuwają się w kierunku bardziej „totipotentnego” stanu, przypominającego wczesne komórki embrionalne zdolne do tworzenia wszystkich tkanek. Odwrotnie, degradacja RNA MERVL za pomocą antysensownych oligonukleotydów tłumi ten przesuw i redukuje aktywność promotorów LTR, co wskazuje, że MERVL działa jak główny wyłącznik uruchamiający szerszą sieć chimerycznych TE i plastyczności stanów komórkowych.
Wirusowa innowacja w toku ewolucji
Analizując wiele genomów ssaków, zespół odtwarza, kiedy różne rodziny TE zaczęły dostarczać eksony do genów gospodarza. Zarówno u ludzi, jak i u myszy relatywnie młode rodziny LTR są szczególnie skłonne tworzyć chimery w orientacji „sensownej”, które mogą być czytane jako część transkryptów gospodarza. Ten wzorzec sugeruje, że nowe fale insercji TE wielokrotnie dostarczały surowego materiału do sieci regulacyjnych genów w czasie ewolucji. Zamiast być wyłącznie szkodliwymi, te insercje mogą być testowane przez maszynerię transkrypcyjną i degradacyjną komórki: większość jest wyciszana lub degradowana, ale mniejszość trafia w odpowiednie miejsce i kontekst, by zostać przejęta jako użyteczne elementy regulacyjne lub nowe początki genów.
Dlaczego te wirusowe pozostałości mają znaczenie
Dla osoby niebędącej specjalistą ta praca pokazuje, że duża i niegdyś lekceważona część naszego genomu aktywnie kształtuje, jak odczytywane są geny, jak komórki zmieniają tożsamość i jak postępują choroby. Starożytne sekwencje wirusowe mogą zostać przekształcone w alternatywne „frontowe drzwi” genów, produkując hybrydowe RNA, które zwykle są kontrolowane przez komórkowe systemy porządkowe. Gdy ta kontrola lub normalny splicing zawodzi, te hybrydy mogą się nasilić, skłaniając komórki macierzyste ku większej elastyczności lub pomagając guzom przystosować się i opierać terapii. Przez miliony lat ewolucja wielokrotnie majstrowała przy tych wirusowych fragmentach, przekształcając wiele z nich z genomowych pasożytów w elementy budujące złożoność regulacyjną — pozostawiając nas z transkryptomem znacznie bardziej plastycznym i dynamicznym niż prosta lista genów mogłaby sugerować.
Cytowanie: Cheon, Y., Alvstad, E.G., Torre, D. et al. Transposable element–gene chimera cartography, origination and role in enhancing transcriptome plasticity. Nat Struct Mol Biol 33, 448–463 (2026). https://doi.org/10.1038/s41594-026-01757-z
Słowa kluczowe: elementy transpozonowe, transkrypty chimeryczne, nadzór RNA, plastyczność komórek macierzystych, ewolucja nowotworów