Clear Sky Science · pl
Dostosowanie importu białek mitochondrialnych do stresu przez degradację DNAJC15 zależną od OMA1
Jak nasze komórki radzą sobie, gdy ich elektrownie są pod stresem
Każda komórka w twoim ciele polega na drobnych strukturach zwanych mitochondriami, które przekształcają pokarm w użyteczną energię. Jak miniaturowe fabryki, mitochondria nieustannie importują nowe części — białka zsyntetyzowane w innych rejonach komórki — aby utrzymać swój sprzęt w ruchu. W pracy tej pokazano, że gdy mitochondria są zestresowane lub uszkodzone, komórka celowo ogranicza ten strumień importu białek. Dzięki temu chroni się przed przeciążeniem i koordynuje szerszą reakcję na stres, obejmującą nie tylko mitochondria, lecz także inny kluczowy przedział komórkowy — retikulum endoplazmatyczne.
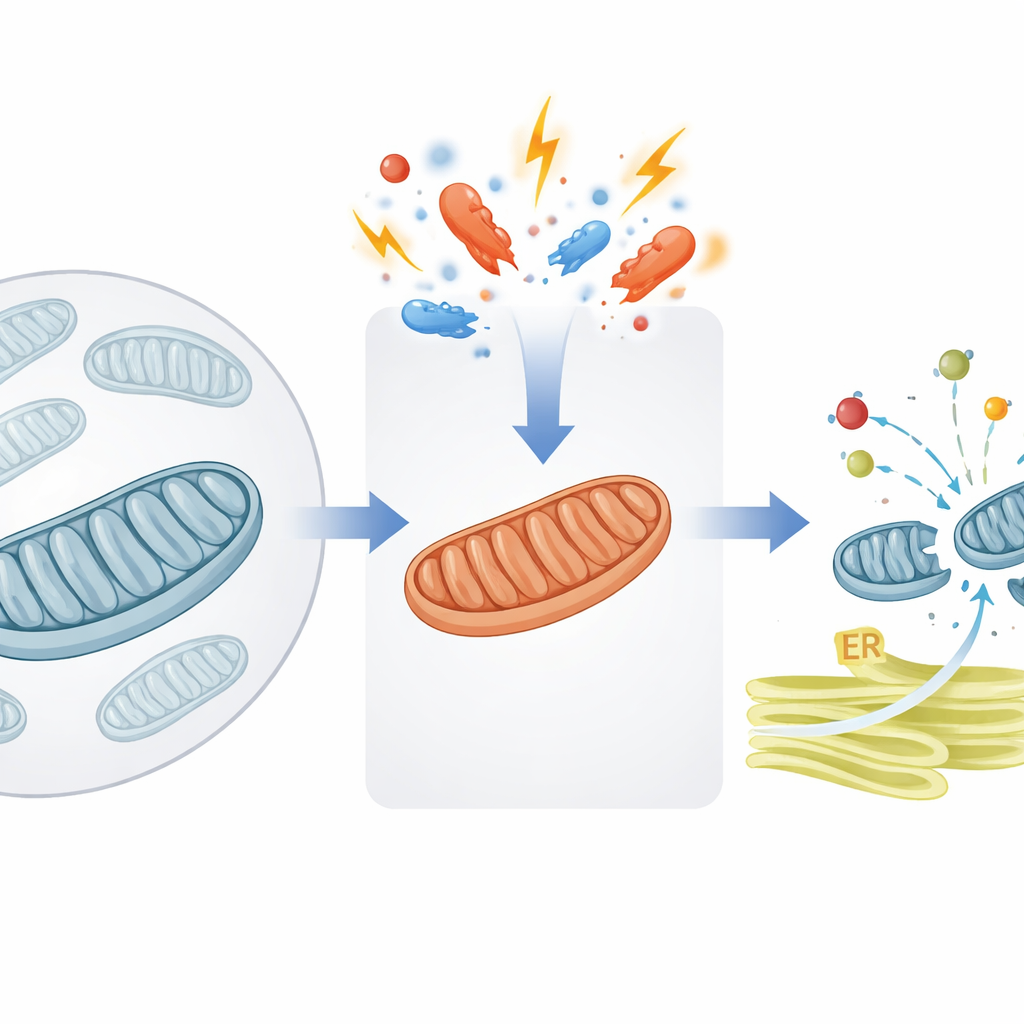
Zawór bezpieczeństwa dla ruchu białek do mitochondriów
Mitochondria potrzebują tysięcy białek, które są najpierw zbudowane w głównym przedziale komórkowym, a następnie transportowane do nich. Autorzy skupiają się na kluczowej bramie w błonie wewnętrznej mitochondrium, wspieranej przez białko pomocnicze o nazwie DNAJC15. W normalnych warunkach DNAJC15 pomaga przeciągać nowe „paczki” białkowe przez kanał importowy do wnętrza mitochondrium, gdzie wiele z nich staje się częścią mechanizmu wytwarzania energii znanego jako fosforylacja oksydacyjna (OXPHOS). Badanie wykazuje, że gdy mitochondria doświadczają stresu — na przykład zaburzonej produkcji energii lub zmian właściwości błony — komórka przełącza molekularny mechanizm, który zmienia ilość białek, jakie organellum jest skłonne zaimportować.
OMA1: nożyk aktywowany przez stres
W centrum tego przełącznika znajduje się enzym wrażliwy na stres o nazwie OMA1, osadzony w błonie wewnętrznej mitochondrium. Gdy mitochondria napotykają problemy, OMA1 ulega aktywacji i przecina DNAJC15 w określonym miejscu blisko jego początku. To cięcie generuje krótszą formę DNAJC15, która jest szybko rozkładana przez inny kompleks enzymatyczny mitochondrium, zwany proteazą m-AAA. W efekcie ginie formą pełnej długości DNAJC15 zdolna do wspierania importu. Autorzy wykazują, że komórki pozbawione DNAJC15 lub w których DNAJC15 jest szybko niszczone po aktywacji OMA1, mają zmniejszoną zdolność wprowadzania nowych białek do mitochondriów, szczególnie tych potrzebnych do budowy i utrzymania kompleksów OXPHOS.
Hamowanie montażu energetycznego dopasowane do kondycji mitochondrium
Wykorzystując szeroko zakrojone pomiary białek i testy importu, zespół odkrył, że DNAJC15 jest szczególnie ważne dla dostarczania do wnętrza mitochondrium białek zaangażowanych w ekspresję genów i montaż łańcucha oddechowego. Gdy DNAJC15 brakuje, te białka gromadzą się wolniej wewnątrz mitochondriów, a zdolność organelli do zużywania tlenu i napędzania produkcji energii — mierzona w izolowanych mitochondriach — maleje, zwłaszcza w odniesieniu do kompleksu I łańcucha oddechowego. Inny składnik kanału importowego, TIMM17A, współdziała z DNAJC15: utrata obu powoduje szczególnie silne defekty w poziomach białek rybosomalnych mitochondriów i komponentów OXPHOS. Te ustalenia sugerują, że degradacja DNAJC15 zależna od OMA1 jest sposobem na tymczasowe ograniczenie budowy nowego aparatu energetycznego, dopóki organellum się nie zregeneruje.
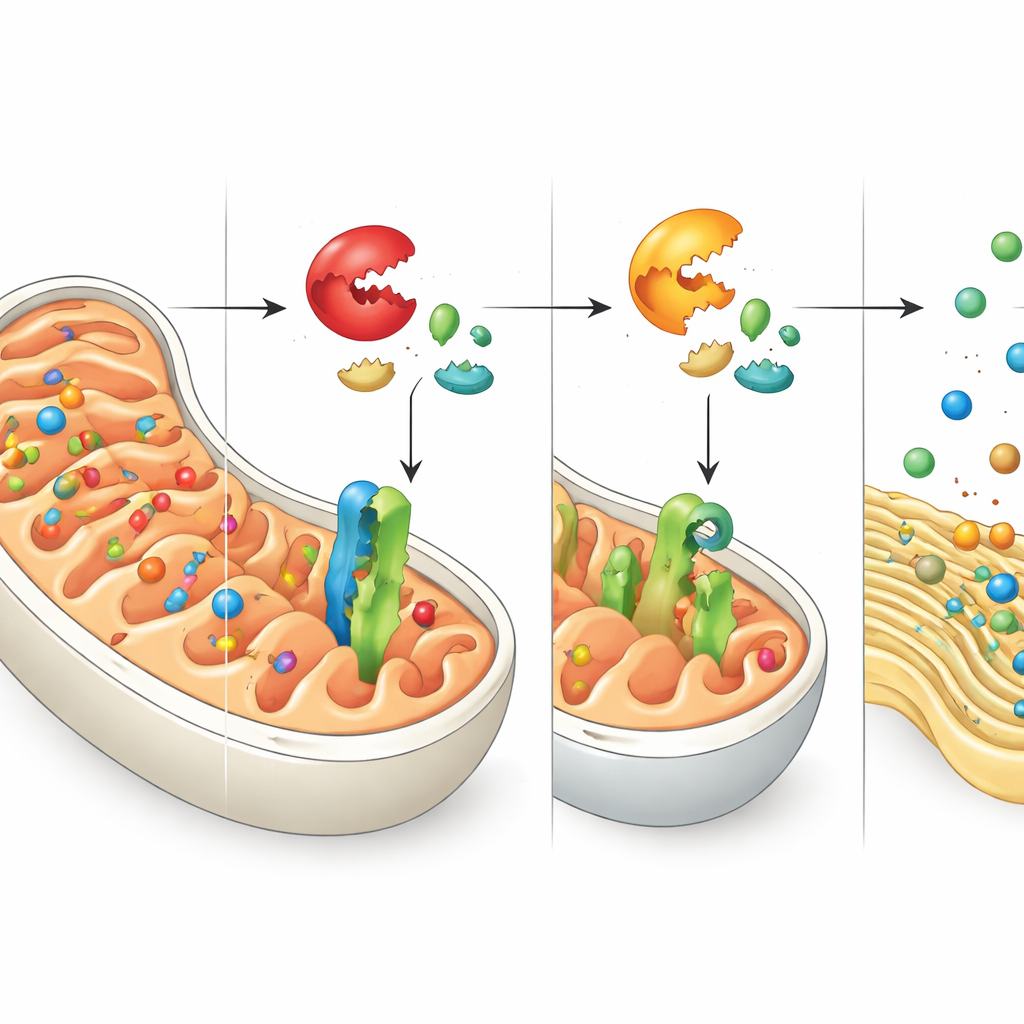
Paczki skierowane omyłkowo i prośba o pomoc do ER
Wyłączenie DNAJC15 nie zatrzymuje produkcji białek mitochondrialnych przez komórkę — głównie uniemożliwia im dotarcie do przewidzianego miejsca. Autorzy śledzili, gdzie trafiają te porzucone białka i odkryli, że wiele z nich kończy w retikulum endoplazmatycznym (ER), sieci błon, która na co dzień pomaga fałdować i przetwarzać różne zestawy białek. Te zbłąkane białka mitochondrialne osadzają się w błonach ER, zaburzając równowagę systemów kontroli jakości ER. W odpowiedzi komórka aktywuje ochronny program znany jako odpowiedź na nieprawidłowo pofałdowane białka, konkretnie przez gałąź kontrolowaną przez czujnik ATF6. Ta reakcja zwiększa zdolność ER do radzenia sobie z nieprawidłowo sfałdowanymi lub niewłaściwie umieszczonymi białkami, ujawniając ścisłą koordynację między systemami stresu mitochondriów i ER.
Zsynchronizowane spowolnienie chroniące komórkę
Podsumowując, badanie ukazuje wbudowany system hamowania biogenezy mitochondriów. Gdy mitochondria są zestresowane, OMA1 przycina i pośrednio doprowadza do zniszczenia DNAJC15, ograniczając napływ nowych białek związanych z energią do uszkodzonych organelli. Część z tych białek jest tymczasowo buforowana w ER, które uruchamia własną odpowiedź ochronną. Dzięki połączeniu zdolności importu mitochondriów ze stanem ich zdrowia oraz wykorzystaniu ER jako miejsca zapasowego dla nadmiaru białek, komórki mogą uniknąć zapchania uszkodzonych mitochondriów i zyskać czas na ich naprawę lub usunięcie. Dla obserwatora niebędącego specjalistą ta praca pokazuje, jak głęboko zintegrowane są nasze komórkowe systemy kontroli jakości: nawet najmniejsze potknięcia w jednym przedziale są wykrywane i kompensowane przez inne, aby utrzymać produkcję energii — a tym samym życie — na właściwym torze.
Cytowanie: Kroczek, L., Nolte, H., Lasarzewski, Y. et al. Stress adaptation of mitochondrial protein import by OMA1-mediated degradation of DNAJC15. Nat Struct Mol Biol 33, 499–511 (2026). https://doi.org/10.1038/s41594-026-01756-0
Słowa kluczowe: stres mitochondriów, import białek, komórkowa kontrola jakości, fosforylacja oksydacyjna, reticulum endoplazmatyczne