Clear Sky Science · pl
Struktura i mechanizm antyfagowego retronu Eco2
Jak bakterie używają wbudowanego „samozniszczenia”, by walczyć z wirusami
Wirusy infekujące bakterie, zwane fagami, występują wszędzie — od oceanów po nasze jelita. To badanie wyjaśnia, jak maleńkie genetyczne urządzenie wewnątrz niektórych bakterii, znane jako retron Eco2, pomaga im przetrwać atak faga. Ukazując trójwymiarową strukturę Eco2 i mechanizm jego aktywacji, praca objaśnia nowy rodzaj awaryjnej obrony: po wykryciu infekcji komórka celowo wyłącza własną produkcję białek, by powstrzymać rozprzestrzenianie się wirusa.
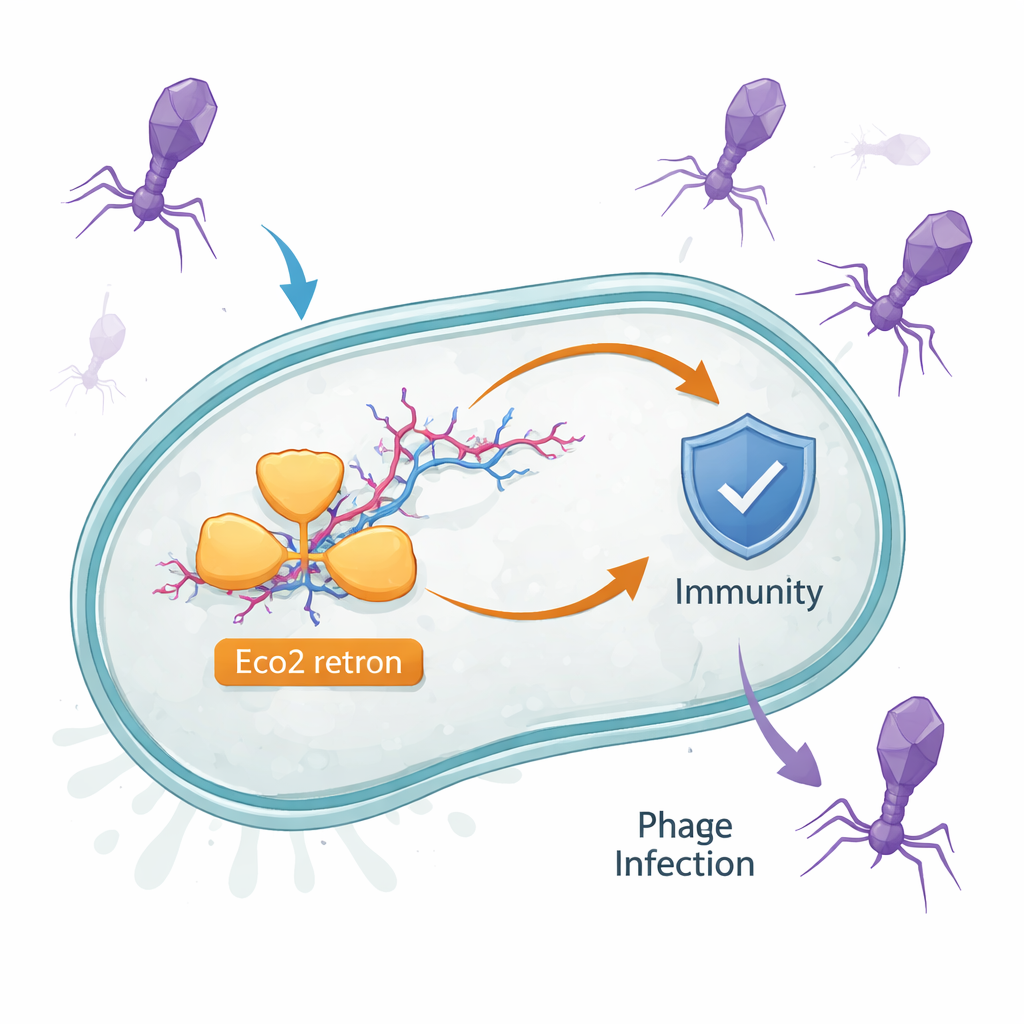
Ukryte DNA–RNA urządzenie w komórkach bakteryjnych
Bakterie posiadają liczne małe systemy obronne, które uruchamiają się dopiero podczas infekcji. Eco2 jest jednym z nich. Występuje w Escherichia coli i składa się z pojedynczego białka, które jednocześnie przepisywuje RNA na DNA i może przecinać kwasy nukleinowe. To białko współdziała z osobliwą cząsteczką zwaną msDNA — hybrydą RNA i jednoniciowego DNA o rozgałęzionej budowie przypominającej małą widłowatą gałązkę. Wcześniejsze wskazówki sugerowały, że retrony takie jak Eco2 bronią przed fagami, ale nie wiadomo było, jak jedno białko i jego partner msDNA wykrywają infekcję i reagują.
Szeroka ochrona przed wieloma wirusami
Naukowcy najpierw sprawdzili, jak dobrze Eco2 chroni bakterie przed różnorodnymi fagami. Atakując komórki z Eco2 dużą, zróżnicowaną kolekcją wirusów, odkryli, że Eco2 blokuje wiele rodzin fagów, choć nie wszystkie. Kiedy niektórym fagom udało się uciec, ich genom wykazywał mutacje w genach kodujących wirusowe enzymy tnące DNA, zwłaszcza w genie odpowiadającym DenB. Ten wzorzec sugerował, że Eco2 jest aktywowany przez specyficzne wirusowe nukleazy: gdy te enzymy zostaną unieruchomione przez mutację, wirus może prześlizgnąć się obronie.
Trójramienna molekularna tarcza
Aby zobaczyć, jak zbudowany jest Eco2, zespół użył krioelektronowej mikroskopii, by zobrazować kompleks z niemal atomową rozdzielczością. Eco2 nie działa samotnie: trzy kopie białka Eco2 łączą się w trójramienną, przypominającą shuriken strukturę. Rozgałęzione msDNA przewleka się przez te trzy białka i oplata je, łącząc w całość. W ten sposób msDNA tworzy trójdzielne złącze w centrum i fizycznie „zamknie” część nukleazową Eco2, blokując jej miejsce cięcia. Eksperymenty wymiany wodoru na deuter wykazały, które regiony są bardziej elastyczne, i pokazały, że związanie msDNA usztywnia i stabilizuje kompleks. W tym stanie spoczynkowym Eco2 jest efektywnie zablokowany w pozycji WYŁ.
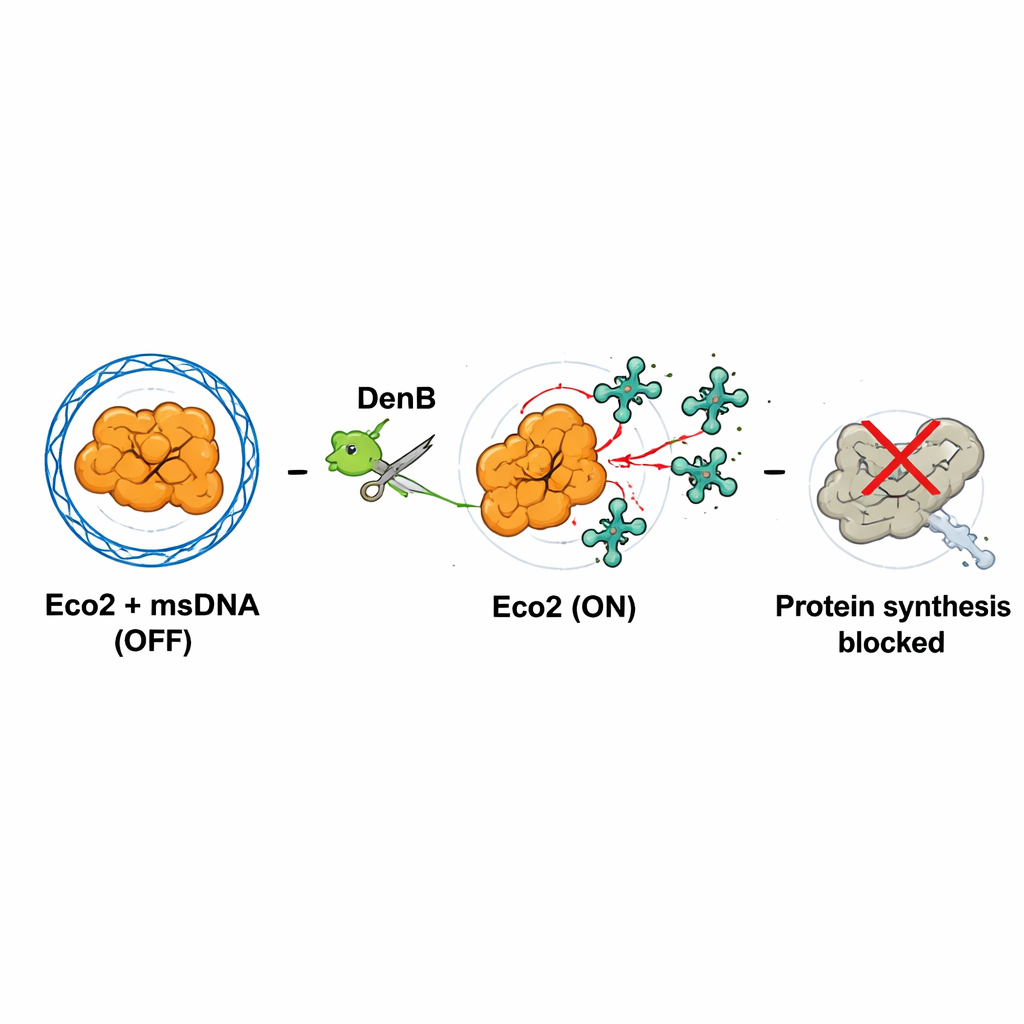
Atak wirusa włącza system
Kluczem aktywacji jest zniszczenie msDNA. Wirusowy enzym DenB, który normalnie pomaga fagowi przetwarzać DNA, również tnie wewnątrz msDNA, które więzi Eco2. Autorzy zasymulowali ten proces, używając zarówno oczyszczonego DenB, jak i standardowego enzymu tnącego DNA, i zaobserwowali, że po przecięciu msDNA miejsce nukleazy Eco2 zostaje odsłonięte i przeorganizowuje się w konfigurację aktywną. Struktury o wysokiej rozdzielczości tego „stanu WŁ.” pokazały, że kluczowy aminokwas w kieszeni nukleazy przesuwa się na pozycję, w której może prawidłowo utrzymać jon magnezu, niezbędny do cięcia RNA. W ten sposób aktywność wirusowej nukleazy, mająca na celu przebudowę DNA gospodarza, mimowolnie wyciąga zawleczkę Eco2.
Cięcie własnych tRNA przez komórkę, by zatrzymać wirusa
Co tnie aktywowany Eco2? Korzystając z systemów pozakomórkowych, znakowania radioaktywnego i sekwencjonowania RNA podczas rzeczywistych infekcji, zespół odkrył, że Eco2 głównie naciną cząsteczki transportowego RNA (tRNA), czyli adaptery dostarczające aminokwasy do rybosomu. Eco2 przecina te tRNA blisko ich końców ogonowych, szczególnie w miejscach bogatych w zasadę cytozynę. Gdy wiele tRNA zostaje uszkodzonych, rybosomy komórkowe nie potrafią już efektywnie syntetyzować białek. W obecności DenB i aktywnego Eco2 produkcja zielonego białka fluorescencyjnego gwałtownie spadała, a zarówno bakteryjne, jak i fagowe RNA były rozkładane. To zatrzymanie prawdopodobnie stanowi „przerwaną infekcję”: zakażona komórka bakteryjna poświęca własny wzrost, by wirus nie mógł się pomnożyć i rozprzestrzenić.
Dlaczego to ma znaczenie poza bakteriami
Praca pokazuje, jak minimalny retron potrafi wykryć enzym wirusowy, przełączyć się z formy nieaktywnej do aktywnej, a następnie sparaliżować syntezę białek przez atak na tRNA. Dla czytelnika niebędącego specjalistą kluczowe jest to, że bakterie czasem pokonują wirusy nie dzięki precyzyjnemu celowaniu, lecz przez odcięcie własnych procesów komórkowych we właściwym momencie. Poza pogłębieniem wiedzy o odporności mikroorganizmów, szczegółowe struktury Eco2 i jego rusztowania msDNA dostarczają planu dla inżynierów, którzy chcieliby zaadaptować retrony jako narzędzia do edycji genomu i biologii syntetycznej.
Cytowanie: Jasnauskaitė, M., Juozapaitis, J., Liegutė, T. et al. Structure and mechanism of antiphage retron Eco2. Nat Struct Mol Biol 33, 330–340 (2026). https://doi.org/10.1038/s41594-026-01754-2
Słowa kluczowe: odporność na bakteriofagi, retron Eco2, bakteryjna obrona przeciwwirusowa, cięcie tRNA, msDNA