Clear Sky Science · pl
Struktura i funkcja drożdżowego superkompleksu wykrywającego aminokwasy SEAC–EGOC
Jak komórki decydują, kiedy rosnąć
Każda komórka musi nieustannie oceniać, czy może sobie pozwolić na wzrost, czy powinna oszczędzać zasoby. Ta decyzja zależy w dużej mierze od aminokwasów — budulca białek i istotnego źródła azotu. Artykuł ujawnia z niezwykłą precyzją strukturalną, jak komórki drożdżowe wykrywają dostępność aminokwasów za pomocą olbrzymiego zespołu molekularnego i wykorzystują tę informację do włączania lub wyłączania głównego regulatora wzrostu, zwanego TORC1. Ponieważ analogiczne układy są zachowane u ludzi i powiązane z rakiem oraz metabolizmem, wnioski z badań na drożdżach dają wgląd w to, jak nasze własne komórki oceniają, kiedy warunki sprzyjają wzrostowi.
Skomplikowany węzeł na centrum recyklingu komórki
U drożdży centralny kompleks decyzyjny zwany SEAC umiejscowiony jest na błonie wakuoli — organelli pełniącej funkcję centrum recyklingu komórkowego. Tam spotyka inny kompleks, EGOC, który przekazuje informacje o poziomach aminokwasów. Razem przesyłają sygnały do TORC1, głównego przełącznika wzrostu. SEAC składa się z dwóch funkcjonalnych połówek: SEACIT, które może wyłączyć TORC1, oraz SEACAT, dawniej uważanego za element hamujący SEACIT. Autorzy zastosowali wysokorozdzielczą kriomikroskopię elektronową, aby zobrazować pełny SEAC związany z EGOC, rejestrując migawkę tego molekularnego węzła dokładnie tam, gdzie zachodzi sygnalizacja — na powierzchni wakuoli. 
Ujęcie architektury molekularnej z bliska
Struktura ukazuje SEAC jako duże jądro złożone z podjednostek SEACAT, od którego odchodzą dwa elastyczne „skrzydła” SEACIT. Każde skrzydło może wiązać jeden kompleks EGOC, co oznacza, że pojedynczy SEAC może odbierać dwa sygnały jednocześnie. Co istotne, EGOC przyłącza się wyłącznie do skrzydeł, a nie do jądra, a ogólny kształt SEAC zmienia się nieznacznie po przyłączeniu EGOC. To pokazuje, że SEACAT nie blokuje fizycznie miejsca aktywnego SEACIT i nie uniemożliwia wiązania EGOC. Orientacja kompleksu na błonie wakuoli ustawia jądro SEAC w stronę cytozolu, gdzie może oddziaływać z dodatkowymi regulatorami, podczas gdy skrzydła leżą blisko błony, idealnie położone, by kontaktować się z EGOC i innymi białkami zakotwiczonymi w błonie.
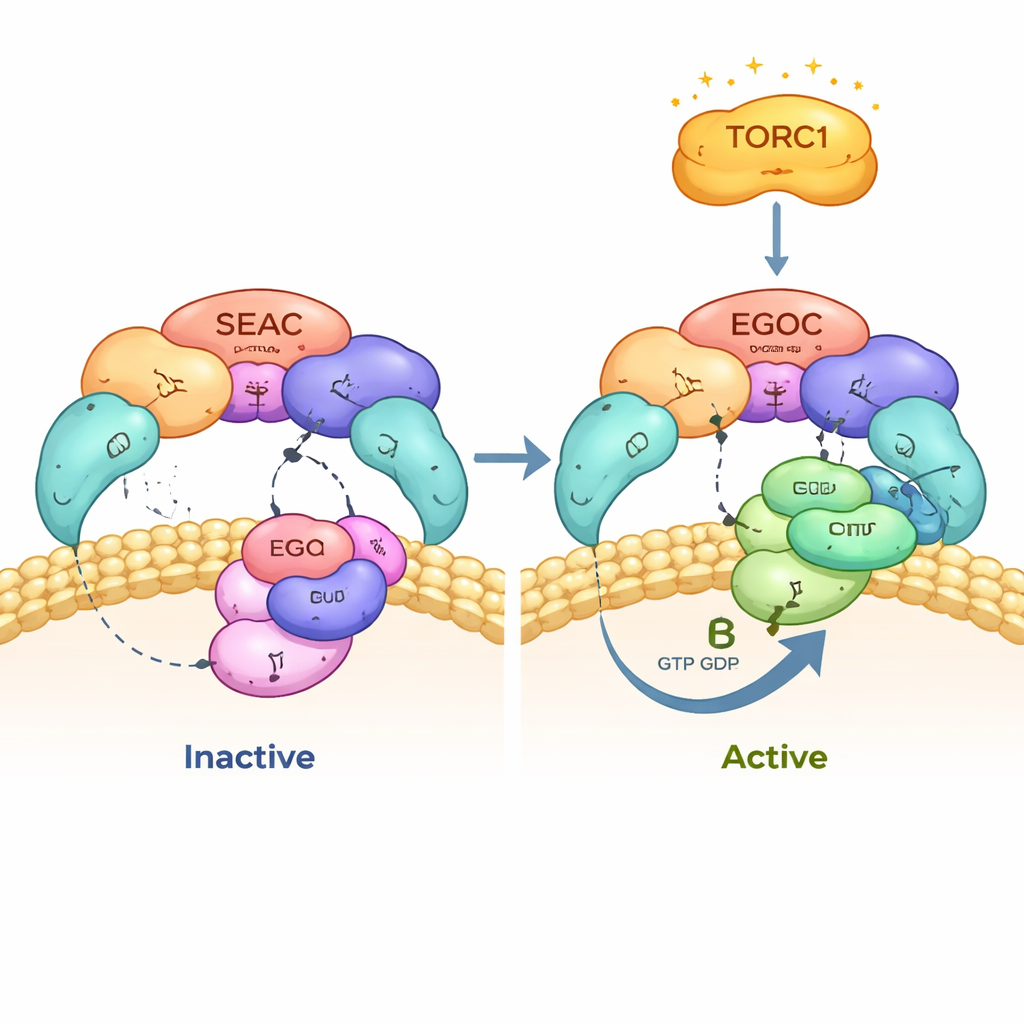
Jak SEAC wybiera właściwy sygnał
Autorzy przyjrzeli się kontaktom między SEAC i EGOC i odkryli, że SEAC rozpoznaje wyłącznie „aktywną” formę EGOC, w której jeden z małych GTPaz, Gtr1, nosi nukleotyd podobny do GTP, a jego partner Gtr2 ma GDP. SEACIT dostarcza katalityczny „palec”, który sięga do kieszeni nukleotydowej Gtr1 i przyspiesza rozkład GTP, przełączając EGOC z formy aktywnej do nieaktywnej. Szczegółowe mapy kriom i eksperymenty mutacyjne pokazują, że ten katalityczny palec oraz przyległy resztor pomocniczy są niezbędne do interakcji i poprawnego odczytu stanu nukleotydu. Gdy autorzy zmienili te kluczowe reszty, SEAC przestał prawidłowo lokować się do wakuoli, a EGOC nie mógł efektywnie wchodzić w interakcję.
Szybka kontra wolna kontrola przełącznika wzrostu
Aby zrozumieć, co to oznacza dla żywej komórki, badacze śledzili aktywność TORC1 w czasie po usunięciu, a potem ponownym dodaniu aminokwasów. W komórkach normalnych TORC1 szybko wyłącza się w ciągu kilku minut po głodzeniu azotowym, a następnie równie szybko włącza, gdy aminokwasy wracają. Gdy katalityczny palec w SEACIT został unieruchomiony albo podjednostki SEACIT usunięto, TORC1 prawie nie reagował w tym wczesnym przedziale czasowym. Podobnie było po usunięciu zarówno Gtr1, jak i Gtr2, co pokazuje, że para SEAC–EGOC jest dominującą, szybką drogą kontroli TORC1 zależnej od aminokwasów. Jednak w późniejszych chwilach — około pół godziny — aktywność TORC1 stopniowo się regulowała nawet w tych mutantach, co wskazuje, że w komórkach działa równoległa, wolniejsza ścieżka prowadząca do TORC1, niezależna od tego systemu GTPaz.
Zaskakująca rola odległej podjednostki
Szczególnie intrygujące jest odkrycie dotyczące Sea2, składnika SEACAT z elastyczną domeną „śmigła” wystającą z jądra. Usunięcie Sea2, lub samego jego śmigła, wywołało defekty sygnalizacji niemal identyczne z tymi obserwowanymi po utracie aktywności katalitycznej SEAC — TORC1 reagował powoli zarówno na odcięcie aminokwasów, jak i na ich ponowne podanie. Jednocześnie Sea2 znajduje się daleko od miejsca katalitycznego i nie styka się bezpośrednio ze skrzydłem SEACIT, co czyni prosty mechanizm blokujący mało prawdopodobnym. Eksperymenty genetyczne łączące utratę Sea2 z katalitycznie martwą wersją SEAC sugerują, że całkowite zablokowanie lub całkowite odblokowanie aktywności GAP zaburza szybką odpowiedź, podczas gdy potrzebna jest regulacja pośrednia. Autorzy proponują, że śmigło Sea2 działa jako platforma dokująca dla nieznanego czynnika, który łagodzi aktywność SEACIT, pozwalając komórkom precyzyjnie dostroić TORC1 zamiast trwale go wyłączać.
Co to oznacza dla decyzji o wzroście komórek
Podsumowując, badanie przekształca obraz SEAC z dwóch przeciwnych zespołów w jedną, zintegrowaną maszynę, której katalityczne skrzydło (SEACIT) i strukturalne jądro (SEACAT) współpracują, by wykrywać aminokwasy i szybko regulować przełącznik wzrostu TORC1. Działanie enzymatyczne SEACIT na EGOC zapewnia szybką, precyzyjną kontrolę, podczas gdy śmigło Sea2 najpewniej rekrutuje regulatorów modulujących tę aktywność. Równocześnie wolniejsze, równoległe ścieżki sprawiają, że TORC1 ostatecznie odzwierciedla stan odżywienia nawet jeśli główny czujnik jest zaburzony. Ponieważ pokrewne kompleksy pełnią tę samą funkcję w komórkach ludzkich, odkrycia te wyjaśniają, jak nasze komórki równoważą wzrost z dostawą składników odżywczych, co ma implikacje dla zrozumienia chorób związanych z nieprawidłową sygnalizacją TORC1.
Cytowanie: Tafur, L., Bonadei, L., Zheng, Y. et al. Structure and function of the yeast amino acid-sensing SEAC–EGOC supercomplex. Nat Struct Mol Biol 33, 488–498 (2026). https://doi.org/10.1038/s41594-026-01746-2
Słowa kluczowe: wykrywanie aminokwasów, sygnalizacja TORC1, kompleks SEAC GATOR, kontrola wzrostu komórek, kriomikroskopia elektronowa