Clear Sky Science · pl
Mechanizm i rekonstrukcja okołodobowej transkrypcji w sinicach
Dlaczego zegary biologiczne mają znaczenie, nawet dla bakterii
Wszystkie organizmy żywe, od ludzi po maleńkie mikroby, odmierzają czas. Wewnętrzne zegary pozwalają przewidywać wschód i zachód słońca, planując czynności takie jak pobieranie pokarmu, naprawa i wzrost. W tym artykule badano, jak prosta bakteria fotosyntetyczna, Synechococcus elongatus, wykorzystuje białkowy układ zegarowy do włączania i wyłączania genów z zaskakującą precyzją w cyklu 24‑godzinnym. Odtwarzając ten system czasowy w probówce, autorzy ujawniają zredukowaną wersję biologicznego zegara, która może zainspirować nowe narzędzia w biotechnologii i biologii syntetycznej.
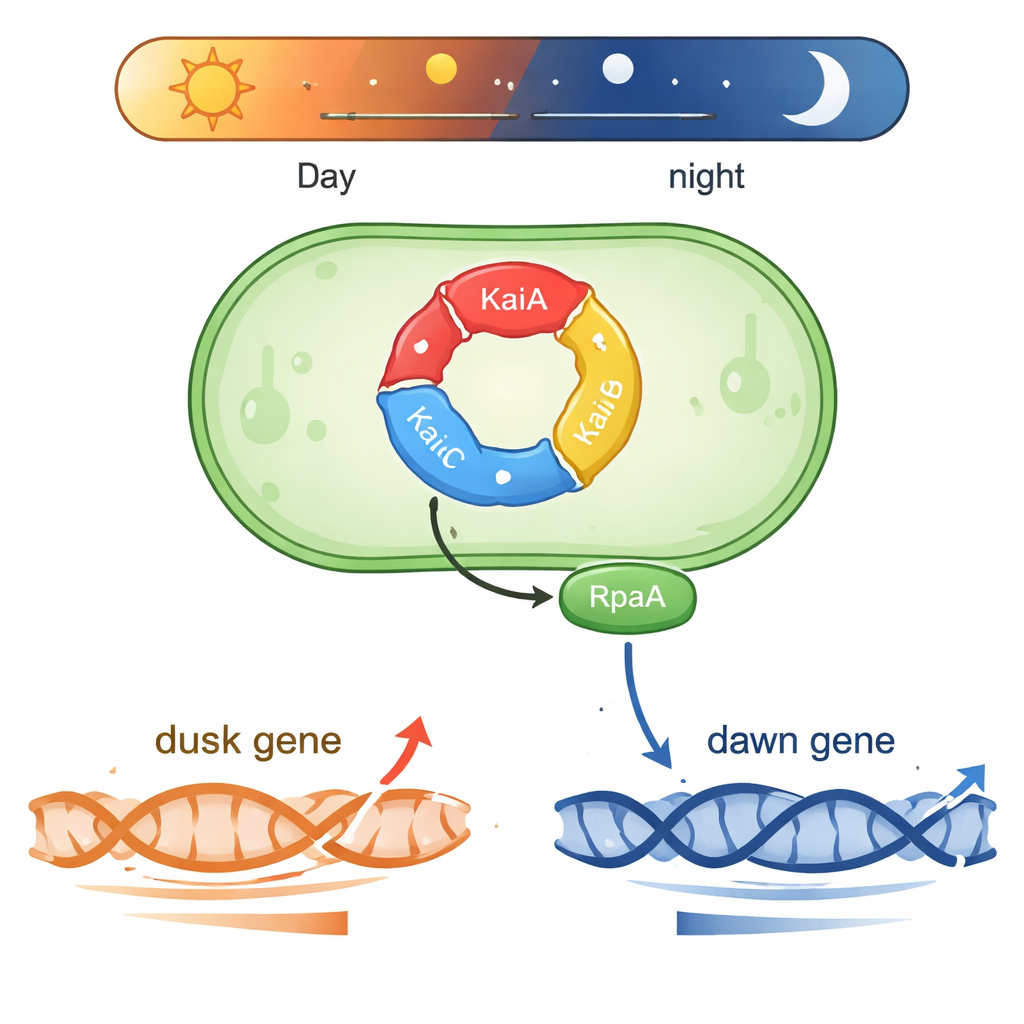
Mały zegar napędzany chemią
Synechococcus żyje w dobrze oświetlonych wodach i musi przewidywać dzienne zmiany natężenia światła. W jego centrum znajduje się trójskładnikowa maszyna białkowa składająca się z KaiA, KaiB i KaiC. Te białka przekazują grupy fosforanowe w powtarzalnym cyklu trwającym około 24 godzin, tworząc biochemiczny „zegarnik”, który odmierza czas nawet poza komórką. Dwa inne białka, SasA i CikA, odczytują stan fosforylacji KaiC i wykorzystują go do kontroli kolejnego białka, RpaA. Gdy RpaA jest fosforylowane, wiąże się z DNA i działa jako główny przełącznik dla setek genów, których aktywność wzrasta i opada albo blisko subiektywnego „świtu”, albo „zmierzchu” w warunkach ciągłego światła.
Jedno białko, dwa przeciwstawne rozkłady genów
Zagadką w biologii okołodobowej było, w jaki sposób jeden czynnik wyjściowy, RpaA, może koordynować geny osiągające szczyt aktywności o bardzo odmiennych porach dnia. Autorzy skupili się na dwóch reprezentatywnych regionach kontrolnych DNA (promotorach): kaiBC, który jest najbardziej aktywny o zmierzchu, oraz purF, który osiąga szczyt o świcie. W kontrolowanych reakcjach z oczyszczoną bakteryjną polimerazą RNA i RpaA wykazali, że fosforylowane RpaA zwiększa transkrypcję z promotora kaiBC, jednocześnie zmniejszając transkrypcję z promotora purF. Szczegółowe eksperymenty typu footprinting dokładnie zmapowały miejsca wiązania RpaA na każdym fragmencie DNA, ujawniając, że jego pozycja względem standardowych elementów promotora decyduje o tym, czy działa jak przyspieszacz, czy jak hamulec.
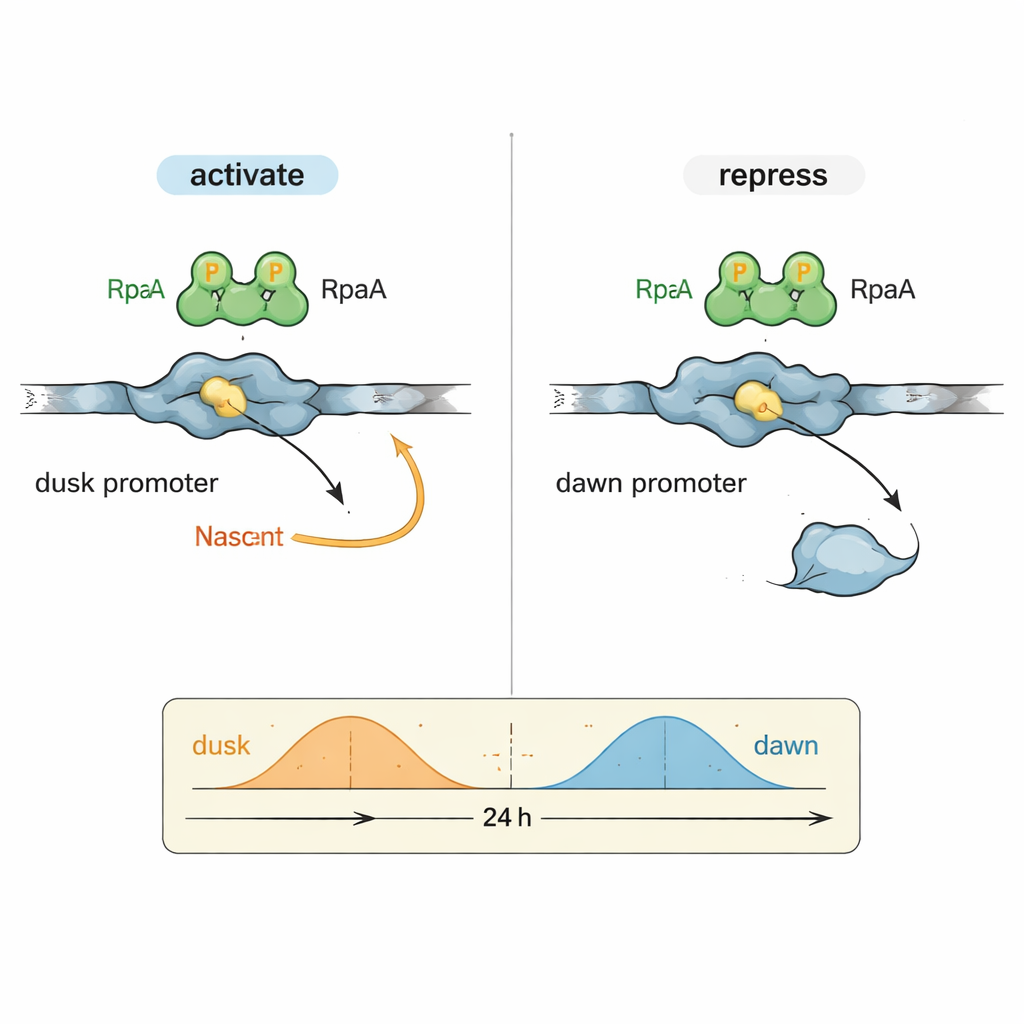
Obserwowanie przełącznika zegara w skali atomowej
Aby zrozumieć to dwoiste działanie na poziomie molekularnym, zespół użył wysokorozdzielczej krioelektronowej mikroskopii, aby uchwycić strukturę RpaA związanej z promotorem kaiBC razem z polimerazą RNA. Obrazy pokazują RpaA chwytające DNA jako asymetryczną parę i nawiązujące kontakty z dwoma kluczowymi częściami enzymu: ogonem podjednostki alfa oraz regionem czynnika sigma, który normalnie rozpoznaje sekwencje promotorowe. Te kontakty wyginają DNA i pomagają ustawić polimerazę RNA w nieco zmienionym miejscu startu transkrypcji. Starannie dobrane mutacje osłabiające którykolwiek z tych punktów kontaktu zmniejszają lub znoszą aktywację kaiBC zarówno in vitro, jak i w żywych komórkach, co potwierdza, że fizyczne rekrutowanie polimerazy RNA leży u podstaw aktywacji genów fazy zmierzchu.
Budowanie genów sterowanych przez zegar od podstaw
Ponieważ natywna bakteryjna polimeraza RNA jest złożona i trudno utrzymać ją aktywną przez wiele dni, badacze zwrócili się do znacznie prostszej polimerazy bakteriofaga T7, powszechnie używanej w laboratoriach. RpaA nie potrafi rekrutować tego niespokrewnionego enzymu, ale nadal może go blokować przez zajęcie miejsca na DNA. Zespół zaprojektował syntetyczny szablon DNA, w którym promotor T7 napędza fluorescencyjny reporter RNA „Broccoli”, z miejscem wiązania RpaA umieszczonym poniżej. Gdy połączyli ten szablon z zegarem KaiA–KaiB–KaiC, kinazą/fosfatazą CikA, RpaA i polimerazą T7 w jednym zoptymalizowanym buforze, zaobserwowali narastające i malejące tempo transkrypcji z okresem około 24 godzin. Rytm dało się zresetować przez zmianę stosunku ATP do ADP i przebiegał z niemal tym samym okresem w szerokim zakresie temperatur — klasyczne cechy prawdziwego zegara okołodobowego.
Od prostych zegarów do inżynieryjnego pomiaru czasu
Badanie pokazuje, że zaledwie sześć białek wystarcza do połączenia chemicznego pacemakera z rytmicznym odczytem genów: trzy białka Kai, CikA, RpaA i polimeraza RNA. Zmieniając pozycję RpaA na DNA, ten sam cząsteczka może sprawić, że niektóre geny osiągają szczyt o zmierzchu, a inne o świcie, co pomaga wyjaśnić złożone fale aktywności genów obserwowane u sinic. Ponieważ projekt oparty na represji działa nawet z obcą polimerazą taką jak T7, możliwe powinno być przeszczepienie tego minimalnego modułu zegara do innych mikroorganizmów lub systemów bezkomórkowych, co pozwoli naukowcom programować włączanie i wyłączanie genów w rytmie dobowym do zastosowań badawczych, przemysłowych lub przyszłych terapii.
Cytowanie: Fang, M., Gu, Y., Leanca, M. et al. Mechanism and reconstitution of circadian transcription in cyanobacteria. Nat Struct Mol Biol 33, 275–281 (2026). https://doi.org/10.1038/s41594-025-01740-0
Słowa kluczowe: zegar okołodobowy, sinice, regulacja transkrypcji, RpaA, biologia syntetyczna