Clear Sky Science · pl
Cereblon wywołuje degradację neosubstratu G3BP2, wykorzystując naśladownictwo powierzchni molekularnej
Przekształcanie komórkowego sprzątania w inteligentny system celowania
Współczesne leki coraz częściej starają się leczyć choroby nie tylko przez blokowanie problematycznych białek, lecz przez ich trwałe usuwanie. Artykuł opisuje sprytny sposób przeprogramowania jednego z wewnętrznych „systemów sprzątających” komórki, tak aby w połączeniu z małą cząsteczką potrafił rozpoznać i zniszczyć białko powiązane z rakiem i innymi zaburzeniami. Praca ujawnia nieoczekiwany trik: maszyneria degradowania zmienia kształt części swojej powierzchni, udając jednego z naturalnych partnerów białka, co umożliwia jej przyczepienie się i skierowanie białka do komórkowego kosza na śmieci.
Komórkowy zbieracz odpadów o ukrytej elastyczności
Nasze komórki nieustannie znakują zużyte lub niechciane białka do zniszczenia, korzystając z systemu opartego na ligazach E3 — dużych kompleksach białkowych, które decydują, co powinno zostać wyrzucone. Jeden z takich kompleksów opiera się na komponencie zwanym cereblonem, pełniącym rolę sensora rozpoznającego określone cechy („degrony”) na innych białkach. Pewne zatwierdzone leki już wykorzystują cereblon jako „klej molekularny”: wiążą się z cereblonem i tworzą nową powierzchnię dokującą, która przyciąga białka związane z chorobą, które następnie są znakowane i degradowane. Do tej pory większość znanych celów miała określony wzorzec strukturalny, co sugerowało ograniczony zakres białek możliwych do usunięcia tą drogą.
Odkrycie nowego celu poza dotychczasowymi regułami
W nowym badaniu autorzy przeskanowali kolekcję molekularnych klejów skierowanych na cereblon w komórkach ludzkich i zidentyfikowali związek nazwany MRT-5702. Ta mała cząsteczka spowodowała szybki zanik białka o nazwie G3BP2, które pomaga w zarządzaniu RNA i wchodzi w skład ziarnistości stresowych — struktur powiązanych z rakiem, schorzeniami serca i chorobami neurodegeneracyjnymi. Co istotne, G3BP2 nie ma typowego motywu degronowego rozpoznawanego przez cereblon. Późniejsze eksperymenty komórkowe, w tym czułe testy oparte na świetle mierzące bliskość białek, potwierdziły, że MRT-5702 łączy cereblon i G3BP2 w trójelementowy kompleks prowadzący do degradacji G3BP2, oszczędzając jednocześnie jego blisko spokrewnione białko G3BP1, chyba że zostanie wymieniona jego kluczowa domena.
Naśladownictwo jako strategia wiązania
Zgłębiając temat, badacze zapytali, jak G3BP2 może wiązać cereblon bez standardowego motywu rozpoznawczego. Zamiast szukać podobieństw między G3BP2 a znanymi celami cereblonu, odwrócili pytanie: czy cereblon może przypominać jednego z naturalnych partnerów G3BP2? Białka G3BP często wchodzą w interakcje z innymi cząsteczkami przez gorące punkty na rejonie zwanym domeną typu NTF2-like, która zwykle rozpoznaje krótkie sekwencje. Korzystając z modeli strukturalnych naturalnego partnera G3BP2, USP10, zespół komputerowo przeskanował powierzchnię cereblonu i znalazł fragment na słabiej poznanym rejonie, domenie LON, który ściśle naśladuje kształt i chemię motywu wiążącego USP10. Zmiany zaledwie kilku kluczowych aminokwasów w tym fragmencie lub w hotspotcie G3BP2 osłabiły trójelementowy kompleks, co sugeruje, że cereblon skutecznie podszywa się pod USP10, aby zadokować do G3BP2.
Uchwycenie nowego interfejsu w atomowych szczegółach
Aby zwizualizować tę nietypową interakcję, zespół użył wysokorozdzielczej krioelektronowej mikroskopii elektronowej, aby rozwiązać strukturę kompleksu zawierającego cereblon, inny rdzeniowy komponent ligazy, MRT-5702 oraz domenę typu NTF2-like G3BP2. Obrazy ujawniły, że elastyczna pętla w domenie LON cereblonu zgina się i przekształca, tworząc niemal połowę powierzchni kontaktu z G3BP2. Aktywna enancjomeryczna forma MRT-5702 siedzi w zwykłej kieszeni wiążącej lek w cereblonie, ale razem z pętlą pomaga stworzyć szeroką platformę, która obejmuje jedną połowę dimeru G3BP2. Co uderzające, to ułożenie niemal nie korzysta z kanonicznego miejsca cereblonu obsługującego wcześniejsze cele klejów, pokazując, że cereblon może angażować bardzo różne regiony swojej powierzchni w zależności od kleju i białka. Jednocześnie niezmieniona połowa dimeru G3BP2 pozostaje dostępna do wiązania innych partnerów, co daje wiarygodną drogę do „kolateralnej” degradacji białek, które przypadkowo są z nim związane.
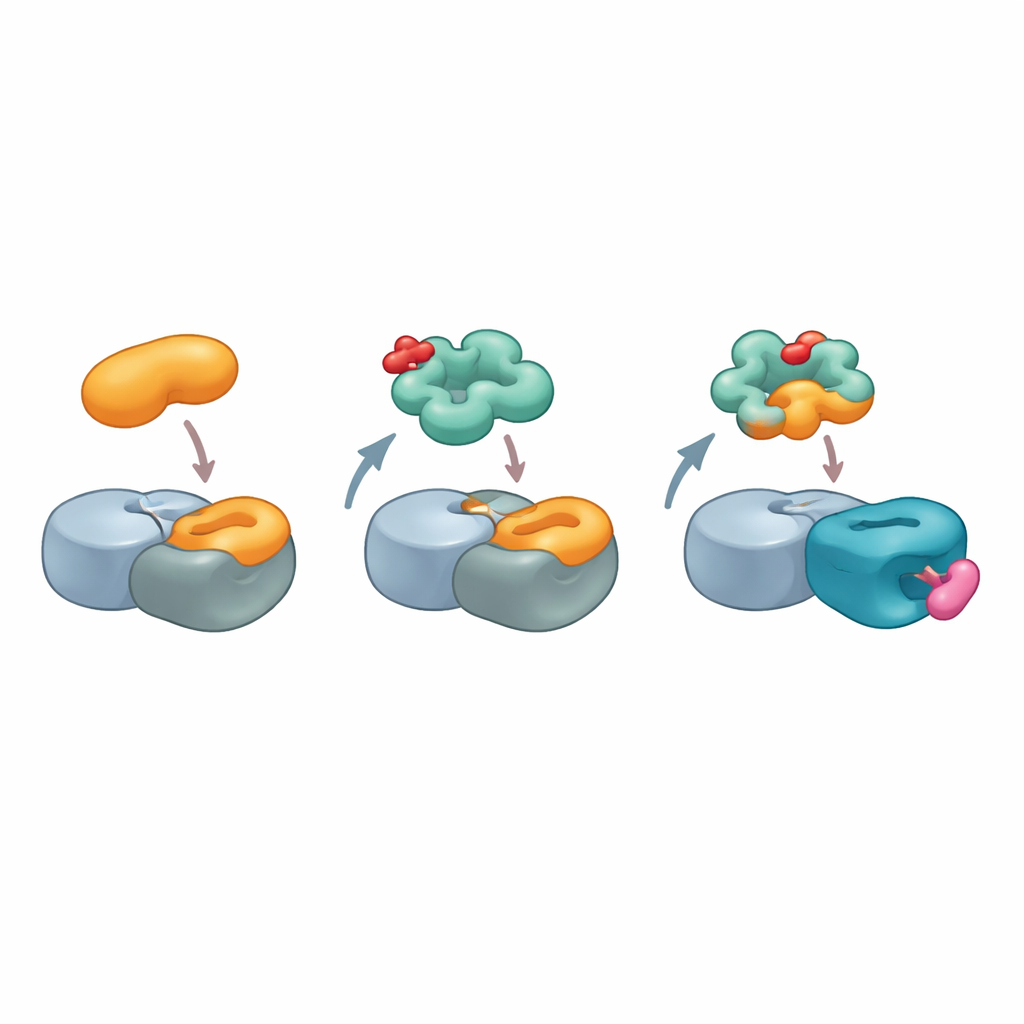
Glueprinty dla przyszłego projektowania leków
W sumie wyniki ukazują cereblon jako znacznie bardziej wszechstronnego łącznika niż dotąd sądzono. Zamiast wymagać, by cele miały jeden rodzaj degronu, cereblon może, uzbrojony w odpowiedni klej molekularny, uformować kompozytową powierzchnię naśladującą naturalne kontakty białko–białko występujące w komórce. Autorzy proponują, że takie złożone powierzchnie białko-plus-klej, które nazywają „glueprintami”, można mapować i projektować tak, by imitowały istniejące gorące punkty interakcji wielu białek związanych z chorobami. Dla czytelnika niezaawansowanego kluczowy przekaz jest taki, że twórcy leków mogą nie musieć odkrywać zupełnie nowych kieszeni wiążących na problematycznych białkach; zamiast tego mogą nauczyć komórkową maszynerię recyklingu rozpoznawać te białka przez sprytne kopiowanie kształtów ich zwykłych partnerów, znacznie poszerzając katalog celów możliwych do bezpiecznego i selektywnego usunięcia.
Cytowanie: Annunziato, S., Quan, C., Donckele, E.J. et al. Cereblon induces G3BP2 neosubstrate degradation using molecular surface mimicry. Nat Struct Mol Biol 33, 479–487 (2026). https://doi.org/10.1038/s41594-025-01738-8
Słowa kluczowe: degradery kleju molekularnego, cereblon, ukierunkowana degradacja białek, G3BP2, oddziaływania białko–białko