Clear Sky Science · pl
Sygnalizacja TGFβ pośredniczy w odporności mikrogleju na przestrzennie i czasowo ograniczoną degenerację mieliny
Dlaczego okablowanie mózgu potrzebuje opiekunów
W miarę starzenia się „izolacja” otaczająca włókna nerwowe — nazywana mieliną — ulega naturalnemu zużyciu. Ta osłona jest kluczowa dla szybkiej i niezawodnej komunikacji między mózgiem a ciałem. Nowe badanie bada, dlaczego jeden konkretny szlak włókien nerwowych w rdzeniu kręgowym, grzbietowy słup, jest wyjątkowo podatny na takie zużycie oraz jak wbudowany hamulec układu odpornościowego — szlak sygnalizacji zwany TGFβ — zapobiega eskalacji uszkodzeń. Zrozumienie tego ukrytego zabezpieczenia jest istotne, ponieważ jego niewydolność może pomóc wyjaśnić niektóre zaburzenia rdzenia kręgowego i wpływać na leczenie chorób mózgu i nowotworów u osób starszych.
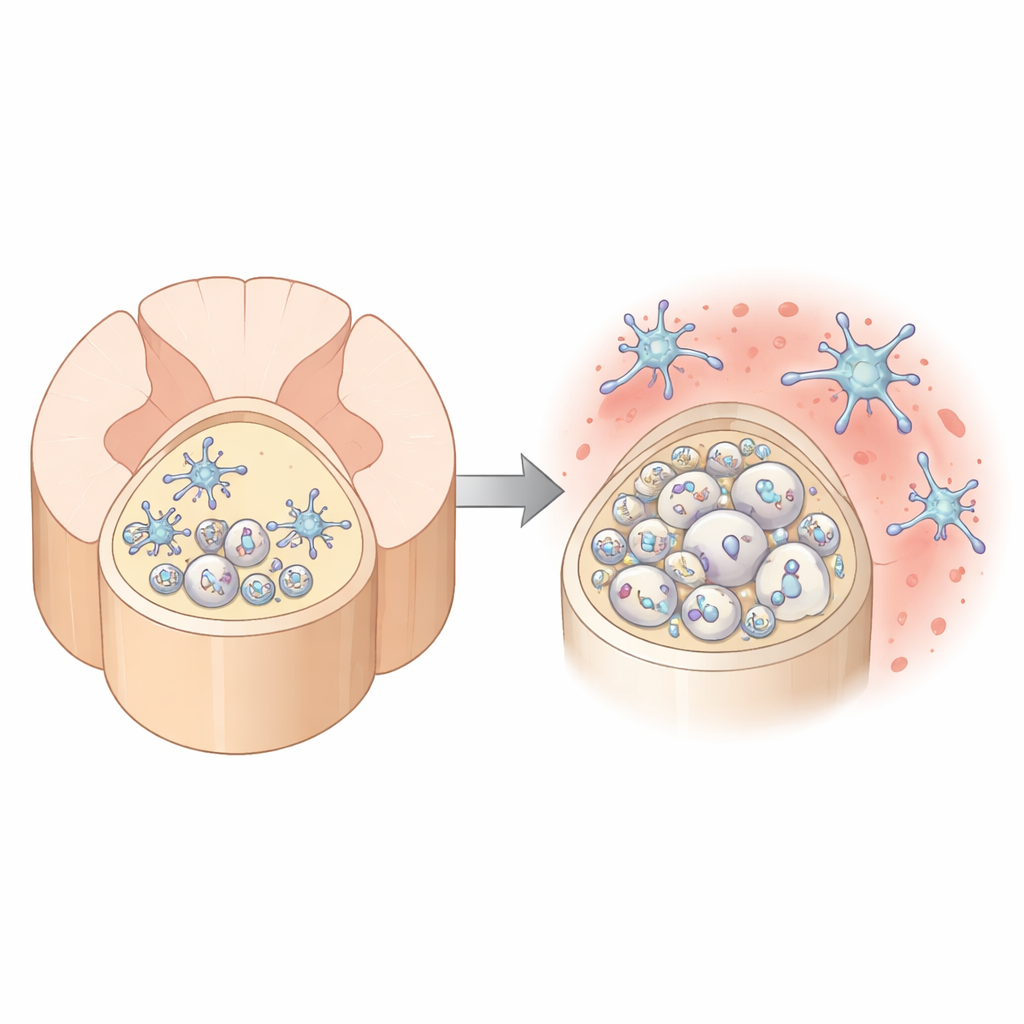
Gdzie starzenie najmocniej uderza w „autostradę” rdzenia
Autorzy najpierw porównali dwa główne pasma istoty białej w rdzeniu kręgowym myszy: grzbietowy słup z tyłu oraz brzuszny słup z przodu. Korzystając z wysokorozdzielczej mikroskopii elektronowej, stwierdzili, że wraz z wiekiem mielina w grzbietowym słupie staje się coraz bardziej zdeformowana. Normalnie ciasne owinięcia wokół włókien nerwowych poluzowują się, wypuklają lub odrywają, pozostawiając powiększone przestrzenie między nerwem a izolacją oraz wzrost jawnego rozpadu mieliny. W przeciwieństwie do tego, słup brzuszny pozostaje stosunkowo stabilny. Region grzbietowy zawiera też znacznie więcej, ale cieńszych aksonów, co sprawia, że jest to szczególnie wymagające środowisko dla komórek budujących i utrzymujących mielinę.
Nadzorcy odporności pod rosnącym obciążeniem
Otaczające te włókna mikrogleje to rezydujące komórki odpornościowe mózgu i rdzenia kręgowego. Nieustannie patrolują tkankę, usuwając szczątki i dopracowując połączenia. W miarę jak mielina grzbietowego słupa degeneruje się z wiekiem, mikrogleje zaczynają wyglądać i zachowywać się inaczej: zwiększają ekspresję genów związanych z aktywacją odporności, gromadzą wewnątrz krople lipidowe i wykazują oznaki pochłaniania większej ilości uszkodzonej mieliny. Jednocześnie środowisko tkankowe w grzbietowym słupie staje się silnie wzbogacone w TGFβ1 — cząsteczkę sygnałową znaną z utrzymywania mikrogleju w powściągliwym, ochronnym stanie homeostatycznym. Same mikrogleje są głównym źródłem tego TGFβ1, co sugeruje, że próbują się hamować nawet w obliczu narastających sygnałów stresu.
Co się dzieje, gdy zawodzi hamulec bezpieczeństwa
Aby zbadać, jak ważny jest ten hamulec, badacze genetycznie wyłączyli sygnalizację TGFβ specyficznie w mikrogleju dorosłych myszy, albo usuwając receptor służący do wykrywania TGFβ, albo uniemożliwiając produkcję TGFβ1. W obu przypadkach wynik był uderzająco podobny i silnie zlokalizowany: mikrogleje w grzbietowym słupie stały się nadmiernie liczne, wysoce aktywowane i przybrały pienistą morfologię wypełnioną strawioną mieliną. Mielina w tym rejonie została zdzierana, aksony wykazywały cechy degeneracji, a myszy rozwijały pogarszające się problemy z ruchem i koordynacją, szczególnie wraz z wiekiem. Inne regiony rdzenia były znacznie mniej dotknięte, co ujawnia zależność od tego szlaku specyficzną dla regionu.
Szczególny podtyp mikrogleju i zapracowani producenci mieliny
Analiza pojedynczych jąder metodą RNA-seq pozwoliła zespołowi skatalogować poszczególne typy komórek w miarę rozwoju choroby. Odkryto wyraźną podpopulację mikrogleju — nazwaną mikroglejem wrażliwym na TGFβ — która dramatycznie się rozszerzyła po usunięciu sygnalizacji TGFβ. Komórki te wykazywały wysoką ekspresję genów związanych z silną odpowiedzią zapalną, intensywnym „jedzeniem” mieliny i gospodarką lipidową, i koncentrowały się w grzbietowym słupie. Jednocześnie populacja dojrzałych komórek wytwarzających mielinę, oligodendrocytów, uległa przesunięciu. Zdrowe podtypy zmalały, podczas gdy w uszkodzonym grzbietowym słupie rozrosła się grupa „związanych z chorobą” oligodendrocytów, która jednak nie odbudowała funkcjonalnej mieliny, pozostawiając aksony odsłonięte pomimo pozornej próby naprawy.
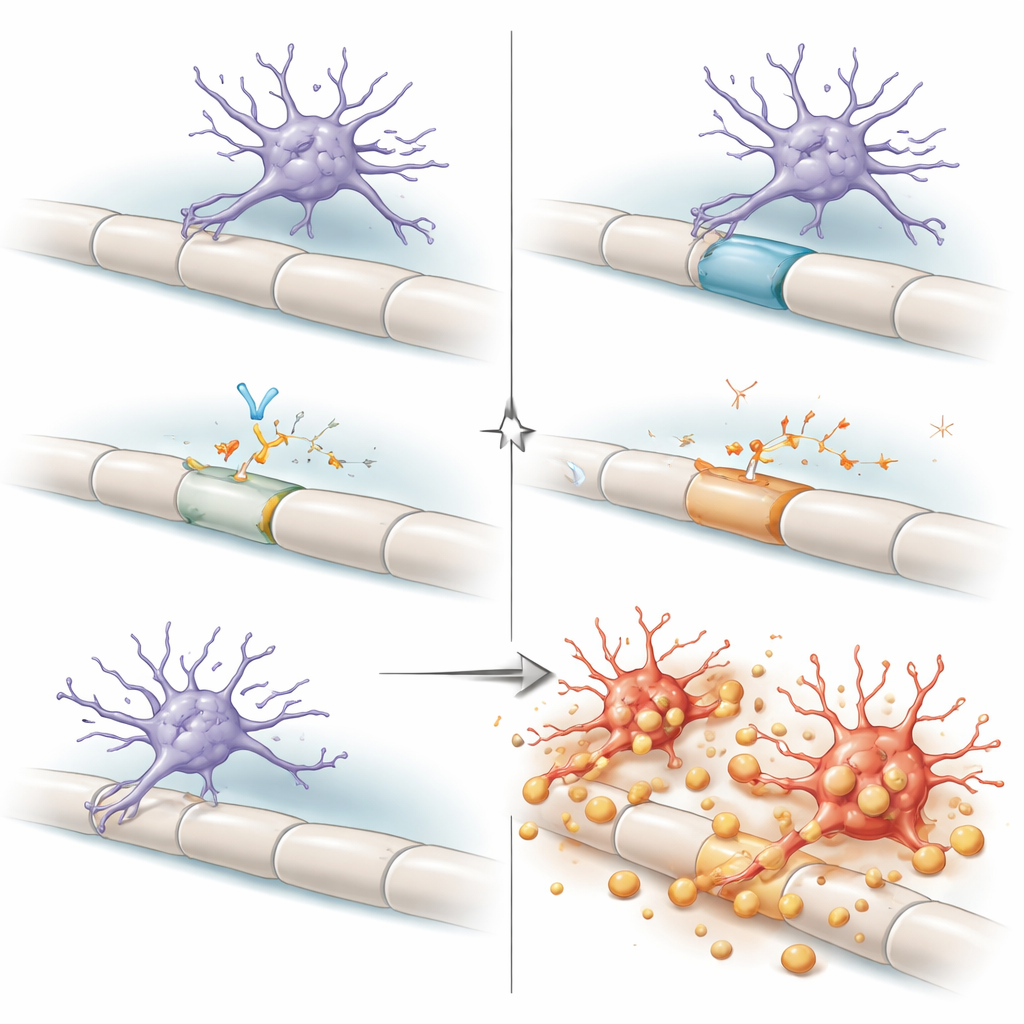
Implikacje dla starzenia i przyszłych terapii
W całości wyniki przedstawiają grzbietowy słup jako obszar o wysokim stresie, gdzie starzejąca się mielina i przeciążone komórki wspierające popychają mikroglej w kierunku punktu krytycznego. W normalnych warunkach pętla autokrynna — mikroglej produkujący i wykrywający własne TGFβ1 — utrzymuje go w stanie „wyczulonym, lecz odpornym”, zdolnym radzić sobie z narastającymi szczątkami bez atakowania stosunkowo nienaruszonej mieliny. Gdy ta pętla zostaje przerwana, mikroglej przechodzi w tryb nieadaptacyjny, agresywnie zdzierając mielinę i napędzając pogorszenie funkcji neurologicznych. Dla szerokiego odbiorcy kluczowy wniosek jest taki, że komórki odpornościowe mózgu nie są po prostu „dobre” albo „złe”; ich zachowanie w dużej mierze zależy od lokalnych wymagań okablowania i od molekularnych hamulców, takich jak TGFβ. Ponieważ leki blokujące TGFβ są opracowywane w terapii nowotworów i niektórych chorób mózgu, praca ta rodzi ważne zastrzeżenie: zakłócenie tego szlaku, zwłaszcza u osób starszych, mogłoby niezamierzenie uszkodzić wrażliwe rejony rdzenia kręgowego przez uwolnienie mikrogleju przeciwko izolacji, której nasze nerwy potrzebują do prawidłowego funkcjonowania.
Cytowanie: Zhu, K., Liu, Y., Min, JH. et al. TGFβ signaling mediates microglial resilience to spatiotemporally restricted myelin degeneration. Nat Neurosci 29, 617–631 (2026). https://doi.org/10.1038/s41593-025-02161-4
Słowa kluczowe: mikroglej, starzenie się mieliny, grzbietowy słup rdzenia kręgowego, sygnalizacja TGF beta, neurozapalność