Clear Sky Science · pl
Rusztowania o zoptymalizowanej symetrii czwartorzędowej do de novo wyznaczania struktur małych RNA metodą cryoEM
Widzenie najmniejszych kształtów RNA
W każdej komórce krótkie nici RNA składają się w drobne struktury trójwymiarowe, które włączają lub wyłączają geny, wykrywają uszkodzenia komórkowe lub świecą pod mikroskopem. Wiele z tych RNA jest tak małych, że obecne metody obrazowania mają trudności z ujawnieniem ich dokładnej architektury. Ten artykuł przedstawia sprytny sposób, by te ulotne cząsteczki uczynić widocznymi: poprzez przytwierdzenie ich do większej, samoskładającej się „ramy” z RNA, którą można wyraźnie zobaczyć metodą kriomikroskopii elektronowej, potężnej techniki obrazowania zamrożonych biomolekuł.
Budowanie pomocnej ramy z RNA
Autorzy zaczęli od fragmentu RNA pochodzącego z wirusa, który naturalnie ma skłonność do parowania w strukturę dwuelementową. Przeprojektowali ten fragment tak, by zamiast parować tylko sporadycznie, niemal zawsze składał się w bardzo regularne układy dwu‑ lub czteroczłonowe w roztworze. Te powtarzające się aranżacje tworzą de facto ramę, czyli rusztowanie z RNA, o wbudowanej symetrii. Symetria jest cenna dla kriomikroskopii, ponieważ identyczne powtarzające się jednostki można uśredniać, co wyostrza ostateczny obraz.
Przyłączanie znanych RNA jako testowych „gości”
Aby sprawdzić, czy ich rusztowanie potrafi przenieść inne RNA do pola widzenia, badacze przeszczepili dobrze poznane cząsteczki na jedno miejsce ramy. Jednym z gości był tRNA z bakterii, klasyczna cząsteczka w kształcie litery L, dostarczająca aminokwasy podczas syntezy białek. Innym było Mango‑III, niewielkie zaprojektowane RNA, które wiąże barwnik i fluorescencyjnie świeci, szeroko używane jako znacznik. W obu przypadkach połączone molekuły składały się i parowały zgodnie z zamierzeniem, a kriomikroskopia elektronowa dostarczyła szczegółowych map ogólnych kształtów. W przypadku tRNA obrazy były na tyle ostre, by zauważyć subtelne różnice między niezmodyfikowaną formą używaną tutaj a wcześniej badanymi, chemicznie modyfikowanymi wersjami. Dla Mango‑III mapy pokazały, że aptamer staje się znacznie bardziej sztywny po związaniu barwnika, co wyjaśnia mechanizm włączania fluorescencji. 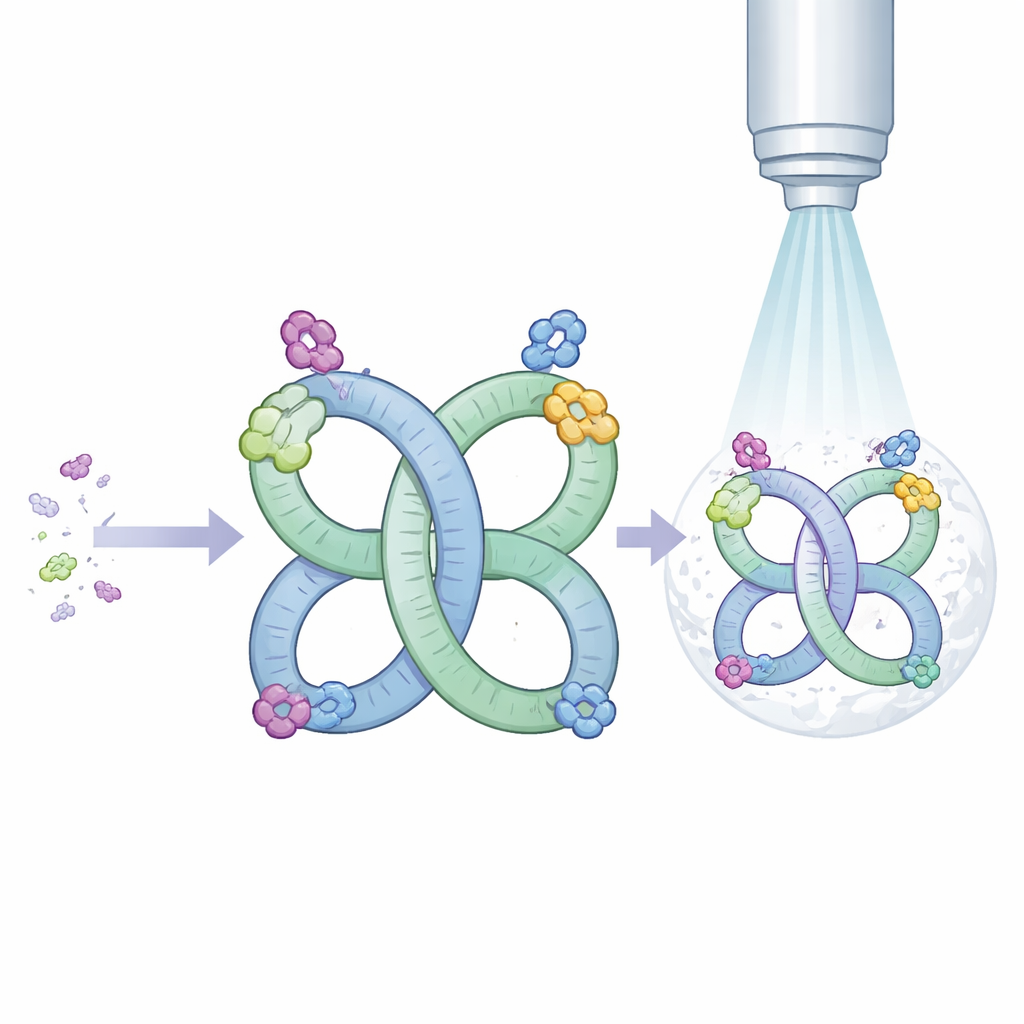
Ujawnianie, jak projektowane RNA chwytają małe cząsteczki
Zespół przeszedł następnie do RNA, których pełne struktury nie były wcześniej widziane. Przyłączyli do rusztowania dwa małe aptamery — krótkie RNA wyselekcjonowane in vitro do wiązania określonych małych ligandów. Jeden aptamer rozpoznaje lek chininę; drugi wykrywa 8‑oksyguaninę, uszkodzoną postać zasady nukleotydowej sygnalizującą stres oksydacyjny u bakterii. Dzięki rusztowaniu kriomikroskopia dostarczyła wyjątkowo wysokiej jakości map, na tyle szczegółowych, by prześledzić każdy łańcuch RNA od końca do końca i zobaczyć, gdzie leżą jony metali oraz cząsteczki wody. W aptamerze wiążącym chinę kieszonka wiążąca otula lek głównie poprzez ciasne układanie (stacking) i dopasowanie kształtu, z zaskakująco niewielką liczbą bezpośrednich wiązań wodorowych. W przeciwieństwie do tego aptamer dla 8‑oksyguaniny owija ligand w misterną sieć wiązań wodorowych, które kontaktują niemal każde chemicznie odrębne miejsce na uszkodzonej zasadzie, wyjaśniając jego wyraźną zdolność rozróżnienia 8‑oksyguaniny od zwykłej guaniny.
Elastyczna symetria dla jaśniejszych obrazów
Co ciekawe, to samo rusztowanie RNA może składać się albo w struktury dwuczłonowe, albo czteroczłonowe, w zależności od warunków i przyłączonego gościa. Gdy tworzy się układ czteroczłonowy, powtarzalna geometria dodatkowo poprawia jakość obrazu. W jednym przypadku rusztowanie przyjęło kształt czteroczłonowy mimo że jego sekwencja była identyczna z wersją dwuczłonową, co podkreśla, jak niewielkie przesunięcia w parowaniu zasad mogą przeorganizować całą strukturę. Autorzy zbadali również praktyczne aspekty zbierania danych w kriomikroskopii, takie jak to, jak odchylanie siatki (tilting) może przezwyciężyć preferowane orientacje cząstek na siatce oraz jak narzucanie symetrii podczas przetwarzania obrazów łagodnie, lecz konsekwentnie wyostrza otrzymywane struktury.
Nowe okno na maleńkie maszyny RNA
Podsumowując, praca ta pokazuje, że zwarte, symetryczne rusztowanie z RNA może przekształcić inaczej niewidoczne małe RNA w doskonałe cele dla kriomikroskopii elektronowej, umożliwiając w korzystnych przypadkach struktury wykraczające poza poziom atomowy. Poprzez przyłączenie nieznanego RNA do ramy za pomocą prostego łącznika helikalnego, badacze mogą teraz określić jego trójwymiarowe złożenie, zobaczyć dokładnie, jak chwyta mały ligand, i dostrzec uporządkowane jony metali oraz cząsteczki wody, które modulują jego zachowanie. Dla szerokiej publiczności kluczowe przesłanie jest takie: mamy teraz praktyczne narzędzie, by przyjrzeć się z bliska niektórym z najmniejszych i najbardziej wszechstronnych maszyn RNA w przyrodzie i biotechnologii, torując drogę do racjonalnego projektowania nowych sensorów RNA, leków i urządzeń molekularnych. 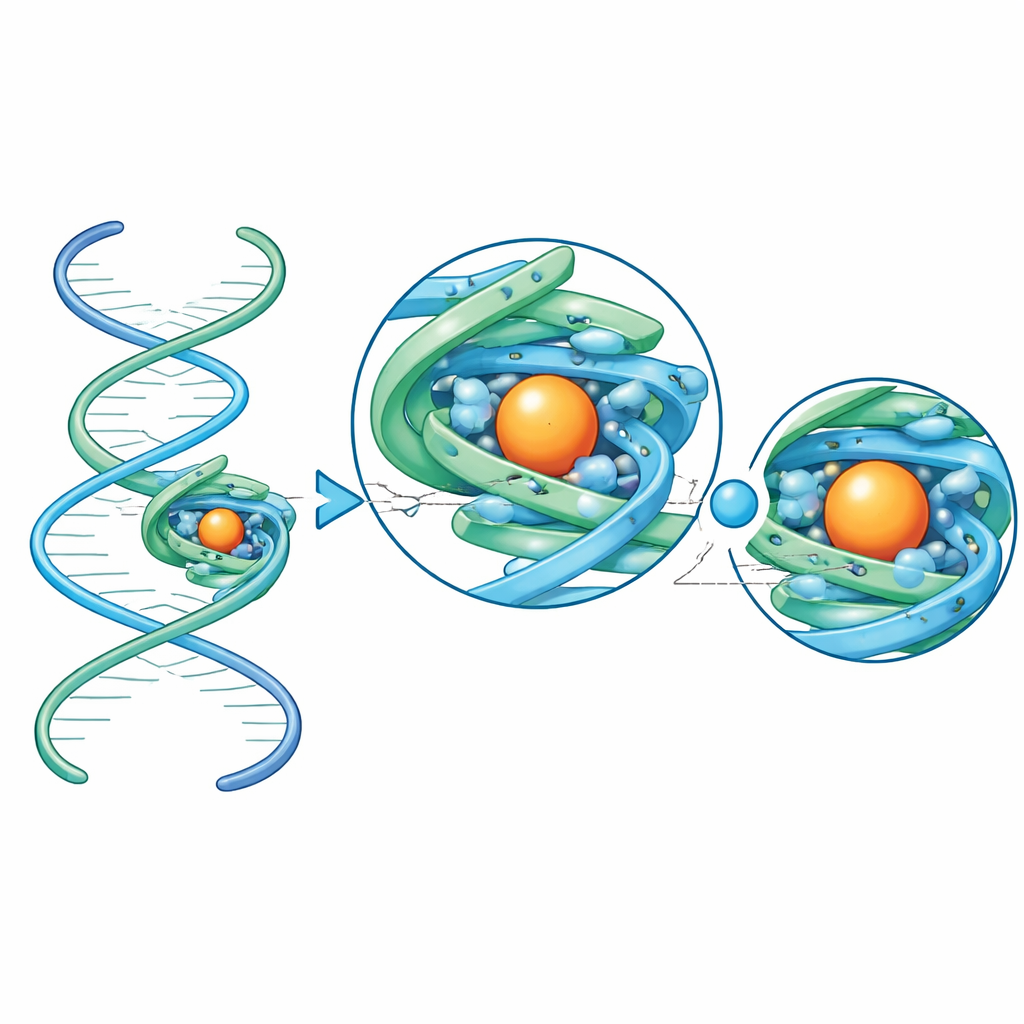
Cytowanie: Jones, C.P., Ferré-D’Amaré, A.R. Scaffolds with optimized quaternary symmetry for de novo cryoEM structure determination of small RNAs. Nat Methods 23, 609–616 (2026). https://doi.org/10.1038/s41592-026-03016-x
Słowa kluczowe: Struktura RNA, kriomikroskopia elektronowa, aptamer, ryboswitch, rusztowania molekularne