Clear Sky Science · pl
MaAsLin 3: doprecyzowanie i rozszerzenie uogólnionych wielozmiennych modeli liniowych do odkrywania skojarzeń w metoomice
Dlaczego mali sąsiedzi jelit mają znaczenie
W naszych organizmach mieszka biliony mikroorganizmów, które pomagają trawić pokarm, kształtować układ odpornościowy, a nawet mogą wpływać na nastrój. Dzięki sekwencjonowaniu DNA katalogowanie tych społeczności stało się łatwe, ale pojawiło się kluczowe pytanie: które konkretne mikroby współwystępują z chorobami, takimi jak choroba zapalna jelit, albo z codziennymi cechami, takimi jak wiek czy dieta? Odpowiedź okazuje się zaskakująco trudna. Dane są zaszumione, pełne zer i raportowane jako procenty zamiast rzeczywistych liczebności. Ten artykuł przedstawia MaAsLin 3, nowe narzędzie statystyczne zaprojektowane tak, by wydobywać wyraźniejsze sygnały z nieporządnych danych mikrobiomu, umożliwiając badaczom bardziej wiarygodne łączenie mikroorganizmów ze zdrowiem człowieka i środowiskiem.
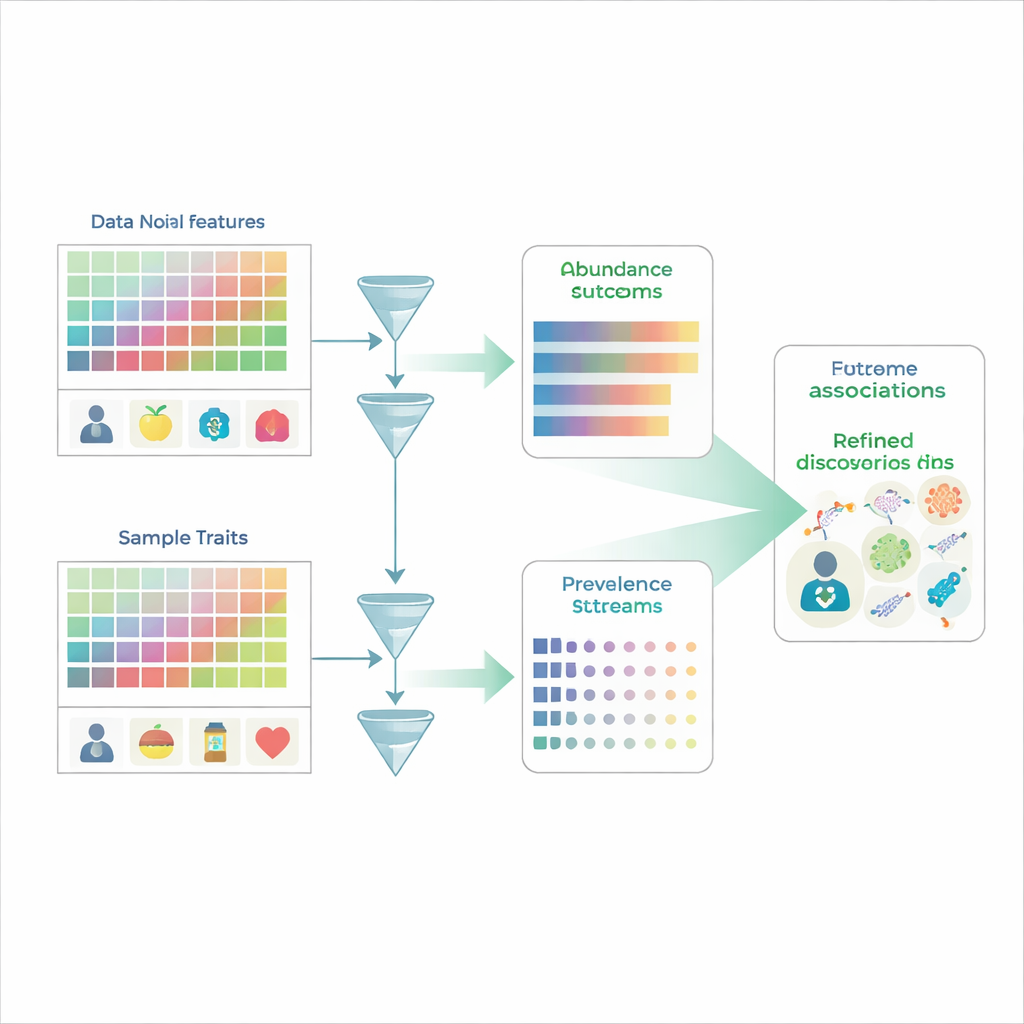
Szukając wzorców w zaszumionym tłumie
Tradycyjne badania mikrobiomu przypominają nieco liczenie twarzy w tłumie: badacze mierzą względną obfitość setek lub tysięcy gatunków mikroorganizmów u wielu osób, a następnie pytają, które gatunki różnią się między grupami, np. chorymi i zdrowymi. Jednak dane mikrobiomu są ograniczone do procentów, które muszą sumować się do 100%, więc jeśli jeden gatunek rośnie, przynajmniej jeden inny wydaje się maleć, nawet jeśli jego rzeczywista ilość się nie zmieniła. Dodatkowo wiele gatunków po prostu nie jest wykrywanych w danej próbce, co daje liczne zera, które mogą odzwierciedlać prawdziwą nieobecność lub ograniczenia wykrywalności. Powszechne metody analizy często zlewają dwa różne pytania — czy mikroorganizm w ogóle występuje oraz ile go jest, gdy występuje — co ułatwia błędną interpretację biologii leżącej u podstaw.
Oddzielanie obecności od ilości
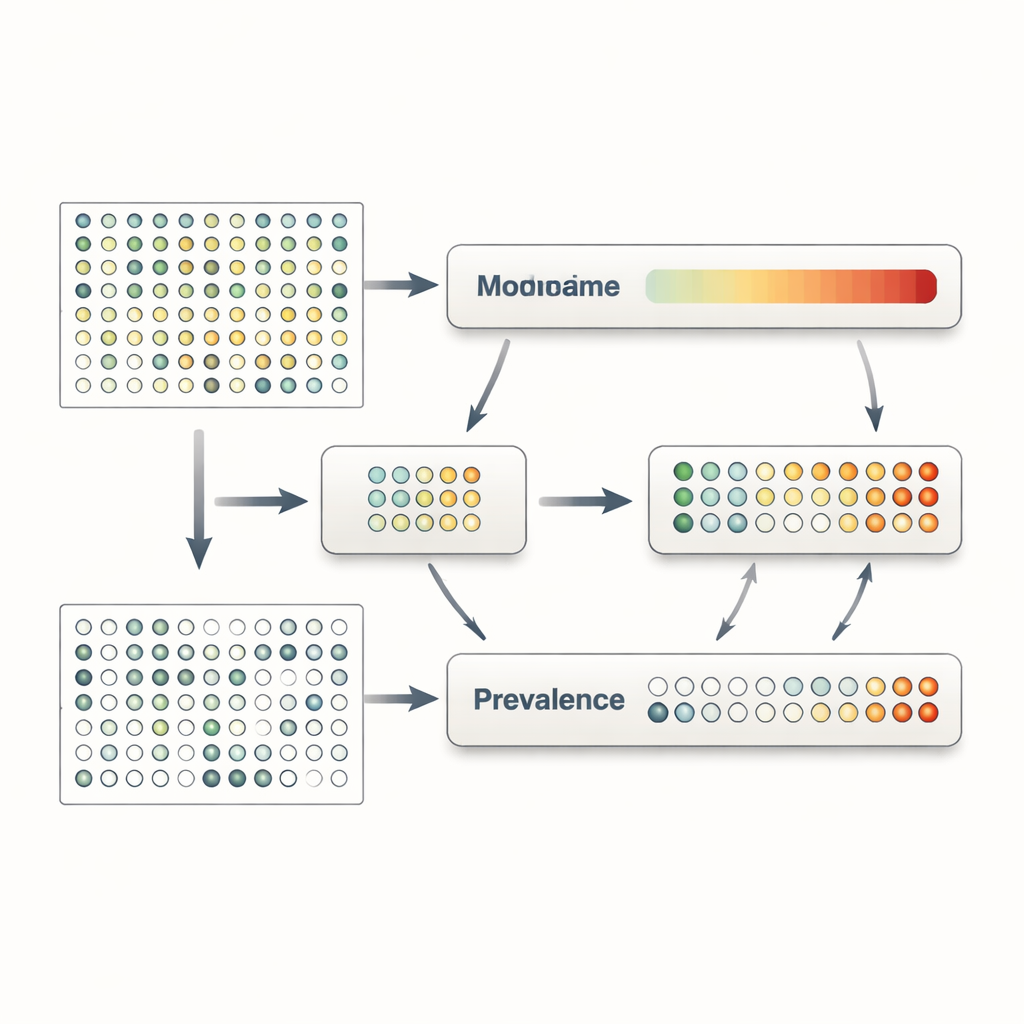
MaAsLin 3 rozwiązuje te problemy, traktując eksplicytnie obecność i ilość jako odrębne, lecz powiązane zjawiska. Dla każdej cechy mikrobiologicznej — takiej jak gatunek, gen czy szlak metaboliczny — buduje dwa modele równolegle. Jeden model bada prewalencję, pytając, jak często cecha jest wykrywana w próbkach o różnych cechach. Drugi model koncentruje się na obfitości, badając, jak poziom cechy zmienia się wśród tych próbek, w których cecha została wykryta. Dzieląc dane w ten sposób, MaAsLin 3 unika powszechnego skrótu polegającego na zastępowaniu zer arbitralnie małymi liczbami, co może zniekształcać wyniki. Następnie łączy oba efekty w całościowy obraz związku każdej cechy z poszczególnymi cechami, jednocześnie pozwalając badaczom zobaczyć, czy skojarzenie dotyczy głównie obecności, ilości czy obu.
Zbliżając się do realnych ilości
Dodatkową komplikacją w nauce o mikrobiomie jest to, że większość pomiarów ma charakter względny: mówią, jaką część całej społeczności zajmuje dany gatunek, a nie ile komórek faktycznie tam jest. Tymczasem pytania biologiczne często zależą od obfitości absolutnej — na przykład czy liczba komórek patogenu przekracza próg, który może wywołać chorobę. MaAsLin 3 oferuje dwa uzupełniające się rozwiązania. Kiedy eksperymenty zawierają dodatkowe informacje, takie jak znane ilości organizmu odniesienia lub oszacowania całkowitego ładunku mikrobiologicznego, metoda może przekształcić względne procenty w estymaty liczebności bezwzględnych i modelować je bezpośrednio. Gdy takich danych brak, MaAsLin 3 porównuje zachowanie każdej cechy do typowego wzorca wśród wszystkich cech, co przy realistycznych założeniach przybliża to, co byłoby obserwowane na skali absolutnej. Obszerne symulacje komputerowe i testy na rzeczywistych zestawach danych z eksperymentalnie zmierzonymi obfitościami absolutnymi pokazują, że ta strategia trafnie odtwarza leżące u podstaw trendy i przewyższa kilka powszechnie używanych narzędzi.
Ujawnianie ukrytych sygnałów w chorobach jelit
Aby zilustrować praktyczne znaczenie tych postępów, autorzy zastosowali MaAsLin 3 do dużej, dobrze zbadanej kohorty osób z i bez chorób zapalnych jelit, takich jak choroba Leśniowskiego–Crohna i wrzodziejące zapalenie jelita grubego. Wcześniejsze prace już identyfikowały wiele zmian mikrobiotycznych w tych schorzeniach, ale MaAsLin 3 dodał kilka warstw niuansów. Potwierdził większość znanych powiązań, jednocześnie wykazując, że około trzy czwarte skojarzeń dotyczyło zmian w tym, czy mikroby w ogóle występowały, a nie w tym, jak były obfite, gdy występowały. Innymi słowy, zapalenie jelit często wiązało się z całkowitą utratą pewnych korzystnych mikroorganizmów lub brakiem ich wykrycia, a nie tylko z łagodnym spadkiem ich poziomów. Metoda ujawniła także mikroby, których sama obecność — niezależnie od ilości — silnie korelowała z zaburzeniem społeczności jelitowej związanym z chorobą.
Co to oznacza dla przyszłych badań i opieki
Dla osób niebędących specjalistami kluczowy przekaz jest taki, że sposób analizy danych mikrobiomu może znacząco wpłynąć na to, które mikroby uznajemy za istotne dla zdrowia. Poprzez lepsze radzenie sobie z zerami, oddzielanie obecności od ilości oraz przybliżanie rzeczywistych liczebności komórek, MaAsLin 3 daje ostrzejsze narzędzie do odkrywania wiarygodnych markerów mikrobiologicznych chorób, diety i środowiska. Wyniki dotyczące chorób zapalnych jelit sugerują, że wiele klinicznie istotnych zmian dotyczy mikroorganizmów, które znikają lub pojawiają się na nowo, a nie tylko tych, które stopniowo zmieniają obfitość. To rozróżnienie jest ważne przy projektowaniu terapii: jeśli choroba wiąże się z utratą korzystnych gatunków, strategie przywracające lub chroniące te mikroby mogą być skuteczniejsze niż podejścia polegające tylko na subtelnym przesunięciu równowagi całej społeczności. MaAsLin 3 wyposaża więc badaczy w precyzyjniejszy i bardziej elastyczny zestaw narzędzi do przekształcania złożonych pomiarów mikrobiomu w praktyczną wiedzę biologiczną.
Cytowanie: Nickols, W.A., Kuntz, T., Shen, J. et al. MaAsLin 3: refining and extending generalized multivariable linear models for meta-omic association discovery. Nat Methods 23, 554–564 (2026). https://doi.org/10.1038/s41592-025-02923-9
Słowa kluczowe: mikrobiom, choroba zapalna jelit, modelowanie statystyczne, absolutna obfitość, prewalencja mikroorganizmów