Clear Sky Science · pl
Atlas pojedynczych komórek rozwijającej się kory mózgu w zespole Downa
Dlaczego to badanie ma znaczenie
Zespół Downa jest najczęstszą genetyczną przyczyną niepełnosprawności intelektualnej, a mimo to wciąż mało wiemy, jak wpływa na rozwijający się ludzki mózg przed narodzinami. To badanie przygląda się na poziomie pojedynczych komórek korze płodu — obszarowi mózgu kluczowemu dla myślenia i pamięci — aby zmapować, co idzie nie tak, kiedy to się zaczyna i które molekularne przełączniki mogłyby zostać sprofilowane terapeutycznie.
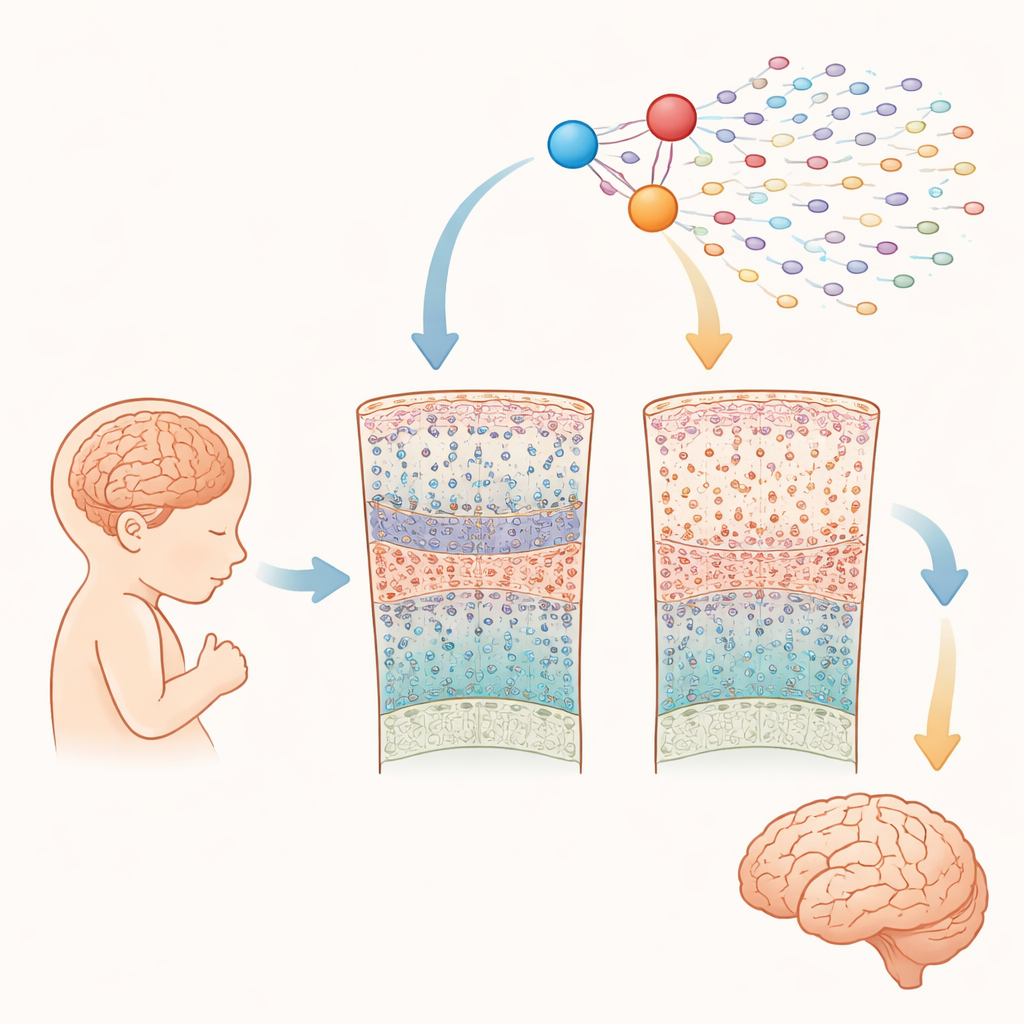
Dokładne spojrzenie na rozwijający się mózg
Naukowcy przeanalizowali niemal ćwierć miliona komórek pobranych z kory mózgowej 15 płodów z zespołem Downa i 15 bez tego zaburzenia, w okresie od 10 do 20 tygodnia po zapłodnieniu. Wykorzystując zaawansowane metody „pojedynczej komórki”, mierzyli zarówno które geny są aktywne, jak i jak dostępne jest DNA w każdej komórce. Pozwoliło to zidentyfikować wszystkie główne typy komórek obecne na tym etapie ciąży — takie jak progenitorowe komórki przypominające komórki macierzyste, różne typy neuronów pobudzających i hamujących oraz wczesne komórki glejowe — oraz porównać ich liczebność i aktywność genową między mózgami z zespołem Downa a typowymi.
Wczesne zmiany w kluczowych komórkach poznawczych
W większości szerokich klas komórkowych liczebności były podobne w obu grupach w tym wczesnym oknie. Jednak zespół zaobserwował uderzający i selektywny niedobór jednego szczególnego typu neuronu pobudzającego, który normalnie znajduje się w warstwie 4 kory i jest ważny dla przetwarzania informacji przychodzących. Te neurony definiowane są przez białka RORB i FOXP1. U płodów z zespołem Downa neurony RORB–FOXP1 były już zmniejszone w połowie ciąży, zwłaszcza między 16. a 20. tygodniem, podczas gdy inne typy neuronów wydawały się stosunkowo oszczędzone. Sugeruje to, że problemy z generowaniem lub dojrzewaniem tej podgrupy komórek zaczynają się in utero i mogą przyczyniać się bezpośrednio do późniejszych trudności poznawczych.
Zaburzone programy genetyczne i główne przełączniki
Ponadto badanie ujawniło, że setki genów były subtelnie niewłaściwie regulowane, szczególnie w neuronach pobudzających i ich progenitorach. Wiele z tych genów bierze udział w budowie przedniego mózgu, kształtowaniu rozgałęzień neuronów, tworzeniu połączeń i wspieraniu wyższych funkcji mózgu. Dane wskazują na zaburzoną sieć regulacji genów, a nie jedynie na działanie dodatkowych kopii około 200 genów na chromosomie 21 w izolacji. Korzystając z podejścia łączącego aktywność genów z dostępnością DNA, autorzy zmapowali obwody regulacyjne i wyróżnili trzy czynniki transkrypcyjne — BACH1, PKNOX1 i GABPA — kodowane na chromosomie 21 jako wrażliwe na dawkę „węzły”. Molekuły te wydają się wpływać na innych krytycznych regulatorów rozwoju kory, w tym czynników już powiązanych z niepełnosprawnością intelektualną, i pomagają wyjaśnić, jak umiarkowane 1,5-krotne zwiększenie dawki genów może rozlać się na całe programy rozwojowe.
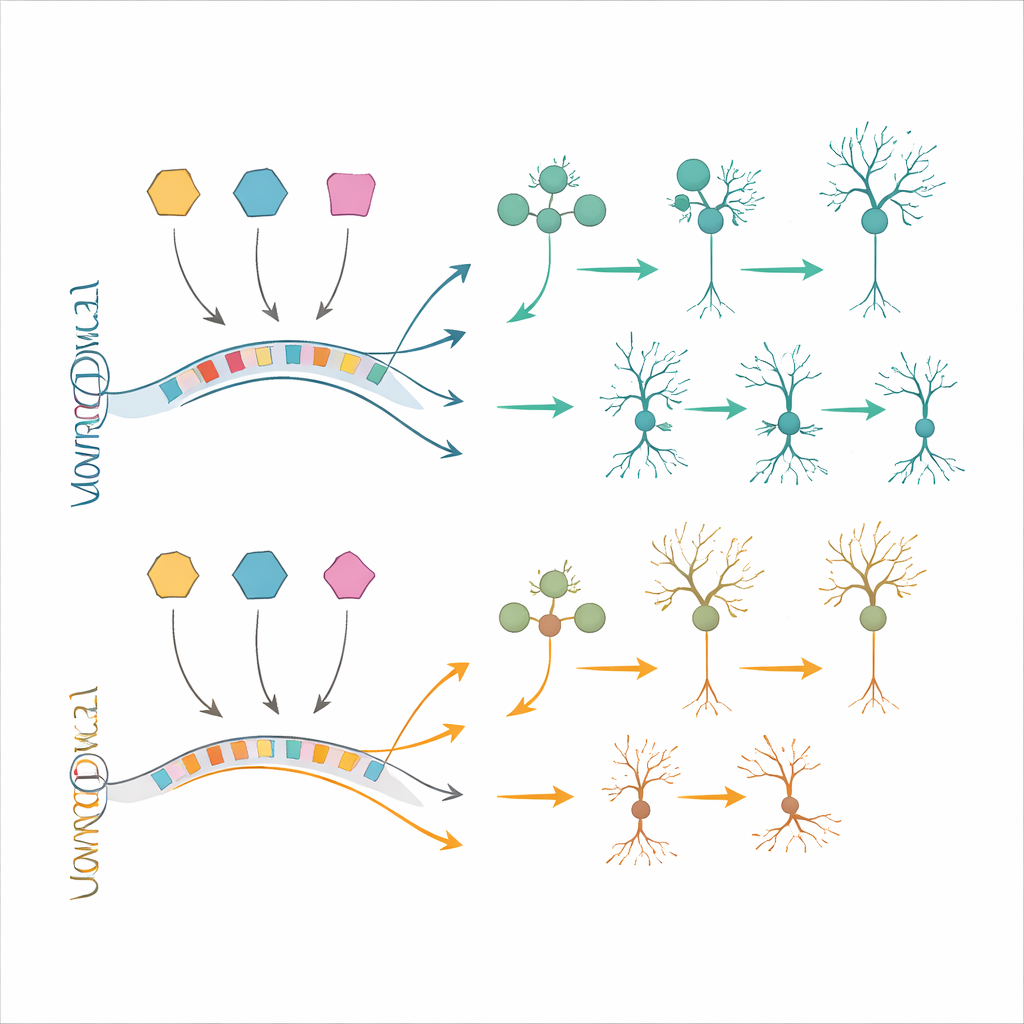
Testowanie strategii ratunkowych w komórkach i żywych mózgach
Aby sprawdzić, czy te molekularne zmiany można skorygować, zespół sięgnął po modele komórek macierzystych. Wytworzyli progenitory nerwowe i neurony z indukowanych pluripotentnych komórek macierzystych zawierających trizomię 21 oraz z dopasowanych komórek kontrolnych. Wiele zmian w ekspresji genów obserwowanych w tkance płodowej pojawiło się ponownie w tych hodowlach, potwierdzając trafność modeli. Naukowcy następnie użyli oligonukleotydów antysensownych — krótkich nici zsyntetyzowanego materiału podobnego do DNA — aby obniżyć poziomy BACH1, PKNOX1 lub GABPA w kierunku normalnego. Częściowa normalizacja nadmiernie eksprymowanych czynników transkrypcyjnych prowadziła do częściowego przywrócenia ekspresji kilku genów podrzędnych, w tym tych znanych z udziału w niepełnosprawności intelektualnej i różnicowaniu neuronalnym. W podejściu komplementarnym przeszczepili ludzkie komórki nerwowe z trizomią 21 do mózgów myszy i pozwolili im dojrzewać in vivo. Te przeszczepy odtworzyły dodatkowe cechy podobne do zespołu Downa, takie jak zmieniony stosunek neuronów do gleju i zmiany genowe, które nie były w pełni uchwycone w hodowlach, oferując potężne pole testowe dla przyszłych terapii.
Co to znaczy na przyszłość
W sumie praca dostarcza szczegółowego atlasu tego, jak zespół Downa przekształca genetyczny pejzaż rozwijającej się kory na poziomie pojedynczych komórek. Dla czytelnika ogólnego kluczowy przekaz jest taki, że dodatkowy chromosom nie dodaje po prostu kilku „błędnych” genów; przesuwa wiele wzajemnie powiązanych molekularnych przełączników, prowadząc do wczesnych i selektywnych braków niektórych neuronów związanych z myśleniem. Wskazując niewielki zestaw czynników transkrypcyjnych z chromosomu 21 jako centralnych graczy — i pokazując, że ich efekty można częściowo odwrócić w ludzkich komórkach — badanie otwiera drzwi do bardziej ukierunkowanych strategii mających na celu poprawę rozwoju i funkcji mózgu w zespole Downa.
Cytowanie: Lattke, M., Tan, W.L., Sukumaran, S.K. et al. Single-cell atlas of the developing Down syndrome brain cortex. Nat Med 32, 1061–1072 (2026). https://doi.org/10.1038/s41591-026-04211-1
Słowa kluczowe: Zespół Downa, rozwój mózgu płodowego, genomika pojedynczych komórek, neurony korowe, czynniki transkrypcyjne