Clear Sky Science · pl
Wielomodalna ucieczka antygenowa przed zaangażowującymi limfocyty T lekami ukierunkowanymi na GPRC5D w szpiczaku mnogim
Kiedy nowotwór przechytrza precyzyjną immunoterapię
Mocne, oparte na układzie odpornościowym leki zmieniają leczenie szpiczaka mnogiego, nowotworu krwi, który dla większości pacjentów pozostaje nieuleczalny. Terapie te przekierowują własne limfocyty T pacjenta, by rozpoznawały i niszczyły komórki nowotworowe oznaczone specyficznymi „flagami” na powierzchni. Obiecującą flagą jest cząsteczka zwana GPRC5D. Jednak, jak przy wielu terapiach ukierunkowanych, guzy potrafią ewoluować i wymknąć się leczeniu. To badanie rozplata ze szczególną dokładnością, w jaki sposób komórki szpiczaka zmieniają lub ukrywają flagę GPRC5D, aby uchylić się przed wysoce skutecznymi lekami angażującymi limfocyty T.
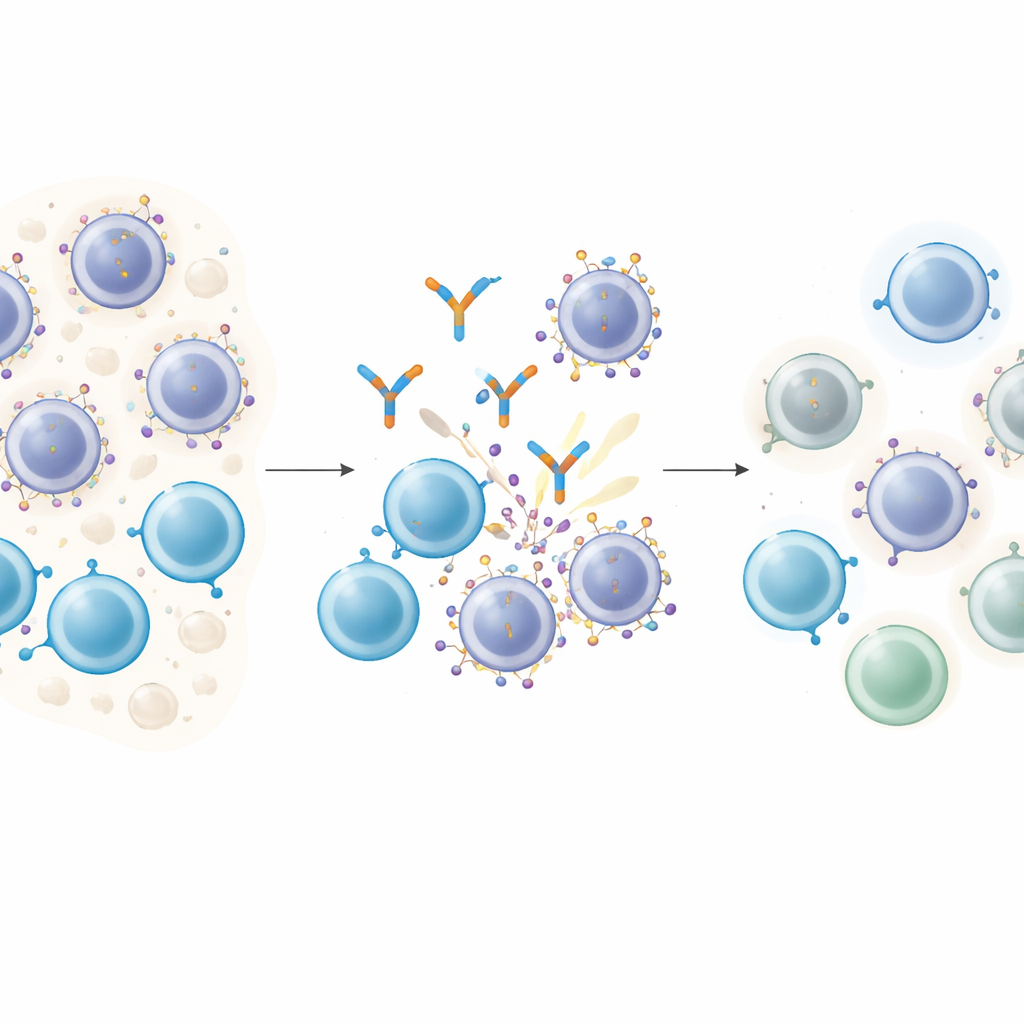
Jak „sprytne” leki przyczepiają się do komórek nowotworowych
Przeciwciała angażujące limfocyty T działają jak molekularni swatowie: jeden koniec łapie limfocyt T, drugi przyczepia się do cząsteczki na komórce nowotworowej, zbliżając je do siebie, aby limfocyt mógł zabić cel. W szpiczaku mnogim GPRC5D jest atrakcyjnym celem, bo występuje obficie na złośliwych komórkach plazmatycznych, a rzadko w większości tkanek normalnych. Pacjenci leczeni lekiem ukierunkowanym na GPRC5D o nazwie talquetamab często doświadczają głębokich remisji. Jednak niemal wszyscy ostatecznie mają nawroty, co rodzi kluczowe pytanie: czy komórki nowotworowe zmieniają sam cel, od którego zależą te leki?
Śledzenie ewolucji guza w czasie rzeczywistym
Naukowcy obserwowali 21 osób z trudnym do leczenia szpiczakiem, które otrzymały talquetamab. Pobierali próbki szpiku kostnego przed leczeniem u niektórych pacjentów oraz ponownie w momencie nawrotu, a następnie analizowali komórki nowotworowe na wielu poziomach DNA, RNA i chromatyny. Ten niezwykle szczegółowy obraz ujawnił, że u około dwóch trzecich pacjentów z nawrotem nowotwór zmienił GPRC5D w sposób, który osłabiał lub blokował działanie leku. Co uderzające, często współistniało kilka różnych opornych podklonów — genetycznie odmiennych odgałęzień guza — co pokazuje, że ewolucja prowadząca do ucieczki może iść wieloma ścieżkami jednocześnie.
Trzy główne sposoby, w jakie guzy ukrywają cel
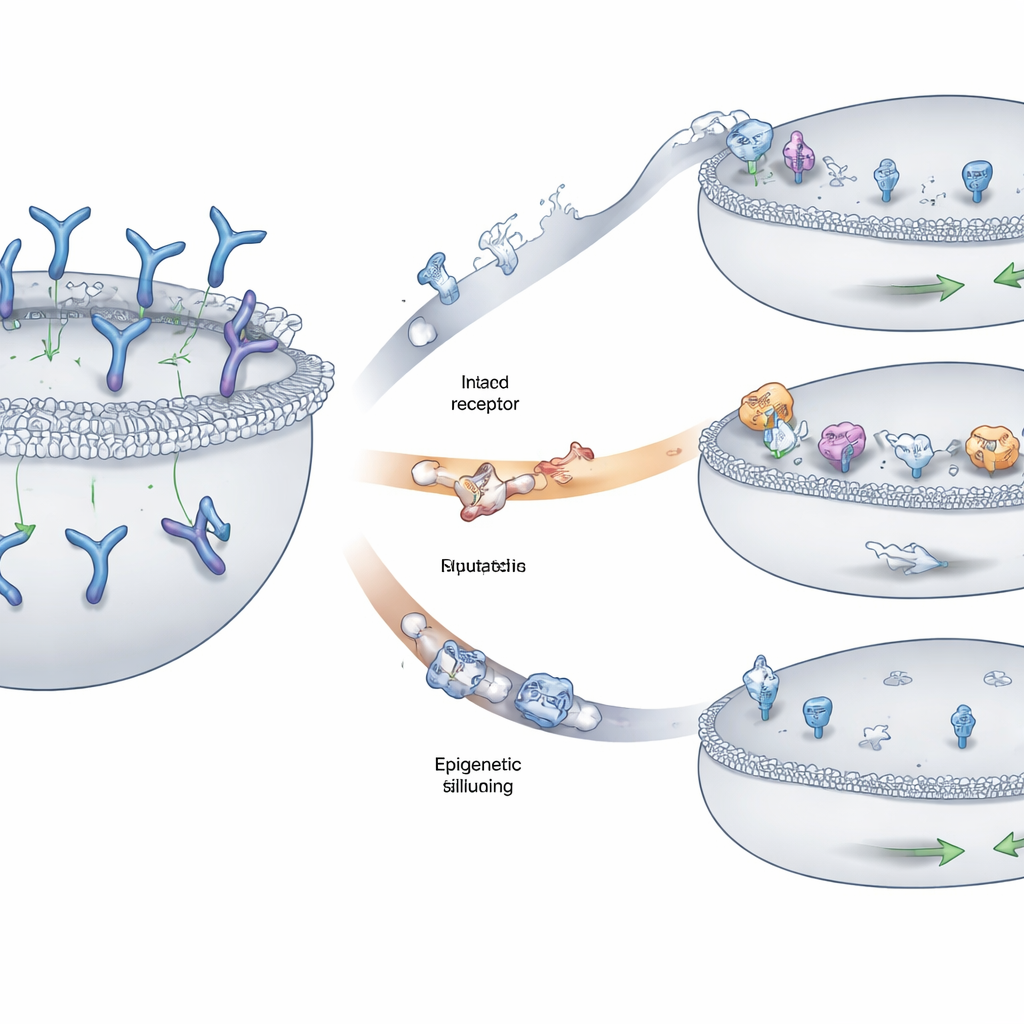
Zespół zidentyfikował trzy powtarzające się wzorce unikania rozpoznania. U niektórych pacjentów fragmenty chromosomu z genem GPRC5D zostały usunięte na obu kopiach, co całkowicie zmazywało flagę z powierzchni komórki. U innych drobniejsze zmiany — zamiany pojedynczych nukleotydów lub małe insercje i delecje — zniekształcały kluczowe regiony białka GPRC5D. Wiele z tych zmian zaburzało fragmenty białka potrzebne do prawidłowego transportu z wnętrza komórki na błonę zewnętrzną, powodując, że GPRC5D utknął w wewnętrznej kompartmentalizacji zamiast być eksponowanym tam, gdzie lek mógłby go dostrzec. Trzecia droga dotyczyła wyciszenia epigenetycznego: okolica DNA wokół GPRC5D stała się ściśle upakowana i chemicznie oznaczona, tak że gen był rzadko transkrybowany, mimo że sekwencja zasadniczo pozostała nienaruszona. Komórki guza stosujące tę strategię wytwarzały niewiele lub wcale GPRC5D.
Kiedy flaga jest obecna, ale zamek już nie pasuje
Nie wszystkie drogi ucieczki usuwały GPRC5D z powierzchni komórki. W niektórych przypadkach białko wyglądało normalnie w standardowych testach laboratoryjnych, ale przestało pasować do leku jak klucz do zamka. Zespół odtworzył konkretne mutacje pochodzące od pacjentów w liniach komórkowych i testował, jak dobrze różne przeciwciała ukierunkowane na GPRC5D potrafią się z nimi wiązać i je zabijać. Jedna mutacja subtelnie zmieniła dokładne miejsce, w którym talquetamab chwytając receptor, co wyraźnie zmniejszyło zdolność leku do wiązania i wywołania śmierci komórki, mimo że receptor wciąż był widoczny przy rutynowym barwieniu. Co ciekawe, inny lek ukierunkowany na GPRC5D, który trzyma receptor za dwa miejsca, pozostał skuteczny wobec kilku z tych mutantów, podkreślając, jak projekt leku — na przykład stosowanie wiązania wielowartościowego lub wieloepitopowego — może wpłynąć na przeżywalność opornych klonów.
Ponad cel: inne ograniczenia ataku odpornościowego
Chociaż większość nawrotów wykazywała jakąś formę utraty lub zmiany GPRC5D, u mniejszości pacjentów nastąpił nawrót bez oczywistych zmian samego celu. W tych przypadkach problem wydawał się leżeć po stronie limfocytów T: były mniej sprawne i mniej zdolne do zabijania komórek nowotworowych w testach laboratoryjnych, co sugeruje, że długotrwała, ciągła ekspozycja na terapię engagerami może wyczerpywać układ odpornościowy. Badanie ujawniło także, że pewien genetyczny podtyp szpiczaka (związany z przemieszczeniem chromosomowym t(11;14)) naturalnie utrzymuje gen GPRC5D w bardziej „zamkniętym” stanie chromatyny, z niższą ekspresją wyjściową. To sugeruje, że niektórzy pacjenci mogą być predysponowani do słabszych odpowiedzi, ponieważ ich guzy zaczynają z przytłumionym poziomem docelowej flagi.
Co to oznacza dla pacjentów i przyszłych terapii
Dla pacjentów i klinicystów ta praca wyjaśnia, dlaczego nawet bardzo silne terapie ukierunkowane na GPRC5D nie są jeszcze lekami uzdrawiającymi: komórki szpiczaka mogą usuwać, przearanżowywać, źle trasować lub wyłączać samą flagę, na której opierają się te leki, i często robią to na kilka sposobów naraz. Wyniki sugerują, że monitorowanie DNA guza, a nie tylko pomiar poziomów białka, będzie istotne dla wykrywania pojawiających się mutacji ucieczkowych, które standardowe testy mogą przeoczyć. Wskazują też na strategie następnej generacji — takie jak leki wiążące GPRC5D silniej w wielu miejscach, kombinacje atakujące więcej niż jeden cel jednocześnie, albo środki reaktywujące uciszone geny — aby wyprzedzić ewolucję guza. W istocie to badanie mapuje drogi ucieczki wykorzystywane przez szpiczaka, tak by przyszłe terapie mogły być zaprojektowane tak, by je zablokować i utrzymać skuteczność terapii opartych na limfocytach T na dłużej.
Cytowanie: Lee, H., Ahn, S., Gonzales, G.A. et al. Multimodal antigenic escape to GPRC5D-targeted T cell engagers in multiple myeloma. Nat Med 32, 964–977 (2026). https://doi.org/10.1038/s41591-025-04175-8
Słowa kluczowe: szpiczak mnogi, engagery limfocytów T, GPRC5D, ucieczka antygenowa, immunoterapia przeciwnowotworowa