Clear Sky Science · pl
Celowana na BCMA terapia komórkowa CAR mRNA w mięśniowej miastenii: randomizowane, podwójnie zaślepione, kontrolowane placebo badanie fazy 2b
Dlaczego to badanie ma znaczenie dla życia codziennego
Miastenia gravis to przewlekła choroba, która sprawia, że proste czynności — jak wchodzenie po schodach, żucie posiłku czy utrzymanie powiek otwartych — stają się niespodziewanie trudne. Wiele osób przez lata musi przyjmować silne leki hamujące układ odpornościowy, które mogą powodować poważne działania niepożądane. W tym badaniu przetestowano nowy rodzaj jednokrotnej terapii komórkowej, która ma wyciszyć chorobę przynajmniej na rok przy zaledwie sześciu cotygodniowych infuzjach, co potencjalnie zmniejsza potrzebę ciągłego leczenia.
Choroba zmęczonych mięśni
W miastenii gravis własna odporność błędnie atakuje „uścisk dłoni” między nerwami a mięśniami. Przeciwciała wytwarzane przez określone komórki odpornościowe blokują i uszkadzają miejsca dokujące, które zwykle pozwalają sygnałom nerwowym wywołać ruch mięśnia. Z czasem pojawiają się opadające powieki, bełkotliwa mowa, trudności w połykaniu oraz osłabienie ramion, nóg i mięśni oddechowych. Standardowe leczenie ogólnie tłumi układ odpornościowy, co może pomagać, ale często pozostawia uporczywe objawy i zwiększa ryzyko infekcji, przyrostu masy ciała, zmian nastroju oraz innych problemów związanych z lekami.
Nowy rodzaj spersonalizowanej terapii komórkowej
Testowana tutaj terapia, nazwana Descartes-08, stosuje bardziej ukierunkowane podejście. Lekarze najpierw pobierają z krwi własne komórki T pacjenta — komórki odpornościowe, które można wyszkolić do rozpoznawania określonych celów. W laboratorium komórkom tym tymczasowo przekazuje się instrukcje genetyczne w postaci mRNA, które uczą je rozpoznawać białko zwane BCMA na powierzchni komórek produkujących przeciwciała napędzających chorobę. W przeciwieństwie do tradycyjnych terapii komórkowych stosowanych w onkologii, które wykorzystują trwałe zmiany wirusowe i wymagają chemioterapii poprzedzającej zabieg, ta konstrukcja jest krótkotrwała i nie wymaga wstępnego niszczenia układu odpornościowego. Pacjenci otrzymują Descartes-08 w postaci sześciu krótkich cotygodniowych infuzji w trybie ambulatoryjnym. 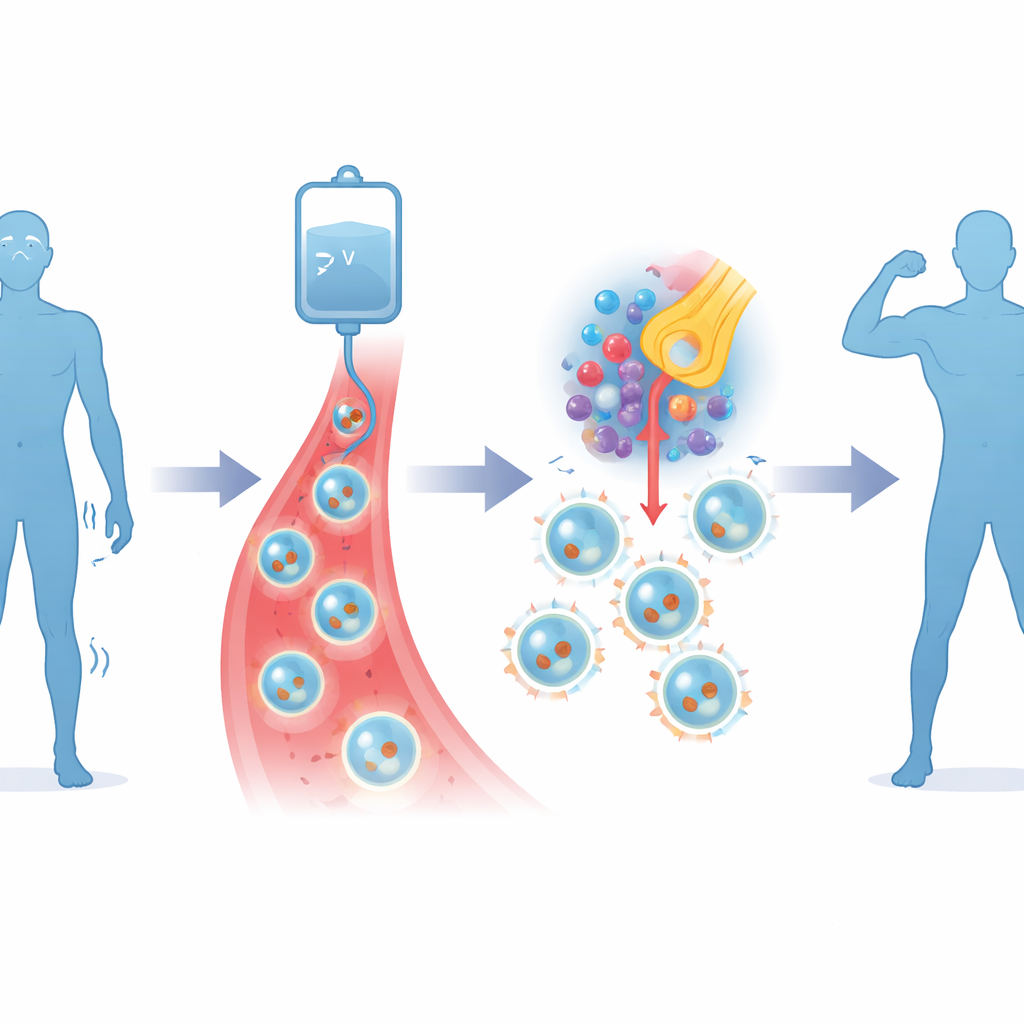
Sprawiedliwy test pomysłu
To badanie fazy 2b objęło dorosłych z uogólnioną miastenią gravis, której nie dotyczyły jedynie mięśnie oczu, i którzy byli już leczeni standardowymi środkami. Uczestnicy zostali losowo przydzieleni do otrzymania Descartes-08 lub infuzji wyglądającej identycznie — placebo, a ani oni, ani ich lekarze nie wiedzieli, którą terapię otrzymują. Głównym miernikiem był powszechnie stosowany wynik łączący raporty pacjentów dotyczące funkcjonowania w codziennym życiu z badaniem siły przeprowadzonym przez lekarza. Badacze pytali: ile osób trzy miesiące po leczeniu poprawiło się co najmniej o pięć punktów — więcej niż to, co eksperci uznają za istotną zmianę? Śledzono też, jak długo utrzymywały się poprawy, czy pacjenci mogli obniżyć dawki steroidów oraz jakie działania niepożądane wystąpiły przez cały rok.
Silniejsze mięśnie, mniej objawów
Wśród 26 uczestników uwzględnionych w głównej analizie osoby, które otrzymały Descartes-08, miały ponad dwukrotnie większe szanse na osiągnięcie założonej poprawy po trzech miesiącach niż te z grupy placebo (około dwie trzecie wobec jednej czwartej). Przeciętnie pacjenci leczeni wykazywali większe spadki w punktacji nasilenia objawów i lepsze wyniki testów siły w porównaniu z grupą placebo, a te korzyści zazwyczaj pogłębiały się przez pierwsze cztery miesiące i były nadal obecne po roku. Około jedna trzecia pacjentów osiągnęła „minimalne wyrażenie objawów”, co oznaczało, że ich codzienna punktacja objawów była bliska zeru; zjawisko to było jeszcze częstsze — u ponad połowy osób — które nigdy wcześniej nie otrzymały nowszych leków biologicznych. Wielu pacjentów leczonych Descartes-08 zdołało też zmniejszyć dawkę steroidów mniej więcej o połowę po sześciu miesiącach, podczas gdy dawki w grupie placebo pozostały mniej więcej takie same. 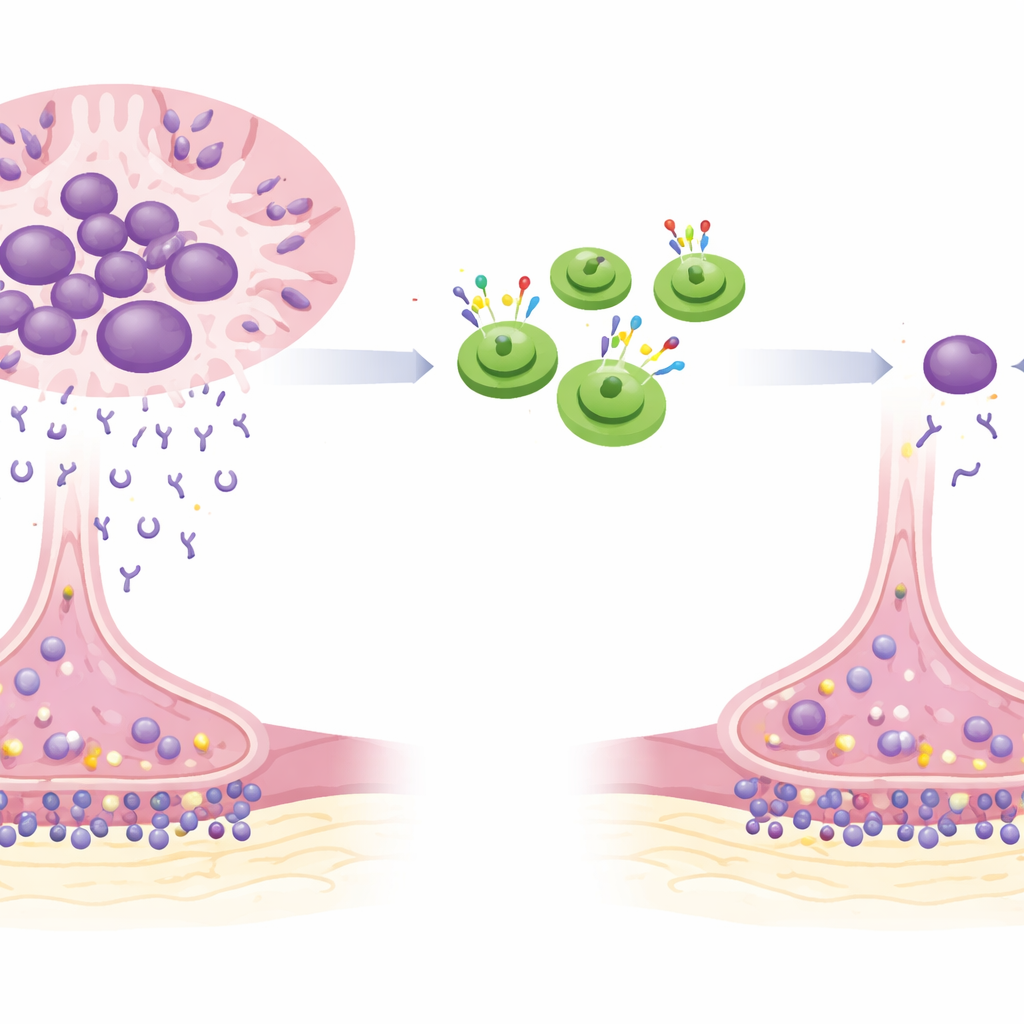
Bezpieczeństwo i co dzieje się w układzie odpornościowym
Działania niepożądane były częste, lecz przeważnie łagodne do umiarkowanych w obu grupach. Najczęściej występującymi problemami przy Descartes-08 były krótkotrwałe reakcje po infuzji — gorączka, dreszcze, ból głowy i bóle mięśni — które zwykle ustępowały w ciągu dnia bez specjalnego leczenia. Nie zaobserwowano poważnych powikłań, takich jak zagrażające życiu burze cytokinowe czy poważne zaburzenia neurologiczne, które mogą występować przy niektórych terapiach onkologicznych. Co ważne, badania krwi wykazały, że ogólny poziom przeciwciał i odpowiedzi ochronne po szczepieniach zostały zachowane, co sugeruje, że terapia głównie zredukowała komórki wywołujące chorobę, zamiast szeroko niszczyć układ odpornościowy. Pomiary eksploracyjne sugerowały, że niektóre sygnały zapalne związane z autoimmunizacją spadły po leczeniu, zgodnie z bardziej precyzyjnym „zresetowaniem” błędnie skierowanej odpowiedzi immunologicznej.
Co to może znaczyć dla pacjentów
Dla osób żyjących z miastenią gravis wyniki te sugerują, że krótki kurs spersonalizowanych infuzji komórkowych może przynieść znaczącą, długotrwałą ulgę, umożliwiając jednocześnie zmniejszenie codziennych leków immunosupresyjnych. Badanie było stosunkowo niewielkie i niektóre różnice poza głównym wynikiem wymagają potwierdzenia w większych próbach, ale spójny wzorzec poprawy i na ogół możliwe do opanowania działania niepożądane są obiecujące. Jeśli przyszłe badania potwierdzą te ustalenia, terapia komórkowa oparta na mRNA mogłaby stać się nową opcją, która kontroluje chorobę bardziej precyzyjnie i wygodnie, przybliżając wielu pacjentów do życia z minimalnymi objawami zamiast stałego zmęczenia i obciążeń medycznych.
Cytowanie: Vu, T., Durmus, H., Rivner, M. et al. BCMA-directed mRNA CAR T cell therapy for myasthenia gravis: a randomized, double-blind, placebo-controlled phase 2b trial. Nat Med 32, 1131–1141 (2026). https://doi.org/10.1038/s41591-025-04171-y
Słowa kluczowe: miastenia gravis, terapia komórkowa, komórki CAR T, choroba autoimmunologiczna, terapeutyki mRNA