Clear Sky Science · pl
Abemacyklib w oponiakach z somatycznymi zmianami NF2 lub szlaku CDK: badanie fazy 2 Alliance A071401
Dlaczego to badanie guzów mózgu ma znaczenie
Oponiaki są najczęstszymi pierwotnymi guzami mózgu. Wielu pacjentom udaje się dobrze po zabiegu chirurgicznym i radioterapii, lecz dla tych, których guzy ciągle nawracają lub rosną, dostępnych jest niewiele skutecznych leków. W badaniu sprawdzono, czy istniejący lek przeciwnowotworowy — abemacyklib — może spowolnić wzrost agresywnych oponiaków posiadających określone zmiany genetyczne, dając nadzieję tam, gdzie opcje terapeutyczne są ograniczone.
Bliższe spojrzenie na oporne guzy mózgu
Większość oponiaków rośnie wolno i często można je opanować chirurgicznie, a w razie potrzeby także radioterapią. Jednak guzy wyższych stopni (oznaczane jako stopień 2 i 3) są bardziej agresywne i częściej nawracają. Historycznie terapie lekowe dla tych nawrotowych guzów dawały ograniczone efekty. W ciągu ostatniej dekady naukowcy zmapowali zmiany DNA napędzające powstawanie oponiaków i wykryli, że niektóre guzy noszą modyfikacje w genach takich jak NF2 oraz w genach kontrolujących cykl komórkowy — mechanizmach decydujących o podziałach komórek. Odkrycia te otworzyły drogę do testowania leków, które celują w te zmienione szlaki.
Projekt badania z wyborem na podstawie genów
Naukowcy uruchomili ogólnokrajowe badanie medycyny precyzyjnej o nazwie Alliance A071401, mające na celu dopasowanie pacjentów z nawrotowymi lub postępującymi oponiakami do terapii celowanych według profilu genetycznego ich guzów. Jedna z gałęzi tego badania skupiła się na abemacyklibie — doustnym leku blokującym dwie kluczowe kinazy cyklu komórkowego: CDK4 i CDK6. Do tej części mogli przystąpić pacjenci z oponiakami stopnia 2 lub 3 mający mutacje NF2 lub zmiany w szlaku CDK. Wszyscy uczestnicy przeszli wcześniej operację, prawie wszyscy otrzymali radioterapię, a wielu próbowało innych terapii układowych. Abemacyklib podawano dwa razy dziennie w 28-dniowych cyklach i kontynuowano do wyraźnego pogorszenia guza lub wystąpienia nieakceptowalnych działań niepożądanych.
Jak skuteczna była terapia?
Głównym wskaźnikiem powodzenia była odsetek pacjentów żyjących i wolnych od progresji choroby sześć miesięcy po rozpoczęciu leczenia abemacyklibem. Wśród pierwszych 24 kwalifikujących się pacjentów poddanych analizie, 14 (58%) osiągnęło ten próg, co wyraźnie przekroczyło wcześniej ustalony próg ośmiu pacjentów, który sygnalizowałby obiecującą aktywność. Najlepszą obserwowaną odpowiedzią była „stabilizacja choroby” u dwóch trzecich tych pacjentów; żaden nie miał wyraźnej redukcji guza, ale zatrzymanie wzrostu agresywnych guzów ma znaczenie kliniczne w sytuacji, gdy zwykle pogarszają się mimo leczenia. Po uwzględnieniu wszystkich 35 ocenialnych pacjentów mediana czasu do progresji wynosiła od 7,6 do 10,1 miesiąca, w zależności od analizy, a mediana przeżycia całkowitego wynosiła około 29 miesięcy. Analizy genetyczne sugerowały, że pacjenci z mutacjami NF2 mieli tendencję do dłuższego pozostawania bez progresji niż ci z samymi zmianami w szlaku CDK, choć badanie było zbyt małe, by wyciągać pewne wnioski.
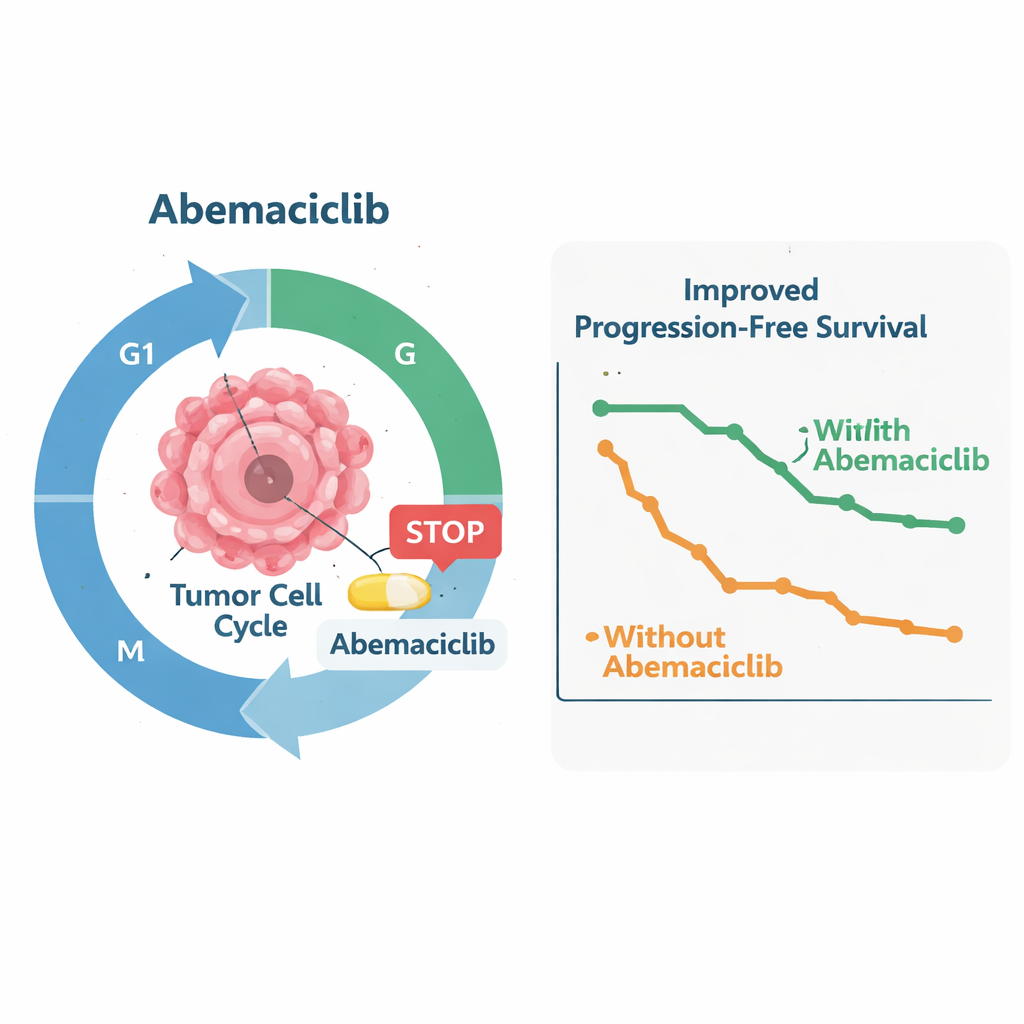
Działania niepożądane i bezpieczeństwo
Wszystkich 36 pacjentów, którzy rozpoczęli leczenie abemacyklibem, monitorowano pod kątem działań niepożądanych. Średnio otrzymali dziewięć cykli leczenia. Około jedna trzecia doświadczyła opóźnień w przynajmniej jednym cyklu, a siedem osób przerwało terapię z powodu działań niepożądanych lub powikłań. Jedenastu pacjentów miało ciężkie (stopień 3 lub 4) zdarzenia możliwe do powiązania z lekiem, w tym spadki parametrów krwi, biegunkę, zmęczenie, podwyższenie enzymów wątrobowych oraz w jednym przypadku silne wymioty. Te działania niepożądane były podobne do obserwowanych przy stosowaniu abemacyklibu w innych nowotworach, takich jak rak piersi, i generalnie uważano je za możliwe do opanowania przez regulację dawki i opiekę wspomagającą.
Co to oznacza dla pacjentów
Badanie nie obejmowało grupy porównawczej otrzymującej inny standardowy lek, częściowo dlatego, że nie ma uzgodnionego standardowego leczenia po niepowodzeniu operacji i radioterapii. Zamiast tego badacze porównali swoje wyniki z danymi historycznymi z wcześniejszych badań u podobnych pacjentów, które pokazują, że tylko około jedna trzecia pozostaje bez progresji po sześciu miesiącach. W tym badaniu 58% pacjentów wolnych od progresji po sześciu miesiącach wypada zachęcająco, zwłaszcza że wiele guzów już opierało się wielokrotnym terapiom. Chociaż abemacyklib rzadko powodował zmniejszenie guzów, jego zdolność do utrzymania ich w stabilnym stanie przez wiele miesięcy stanowi istotny postęp dla pacjentów z ograniczonymi opcjami.
Krok w kierunku precyzyjniejszej opieki nad guzami mózgu
Dla osób z agresywnymi, opornymi na leczenie oponiakami, to badanie daje ostrożny powód do optymizmu. Wykazało, że dopasowywanie pacjentów do leków na podstawie genetyki ich guzów jest możliwe na skalę krajową oraz że abemacyklib może spowolnić progresję choroby przy zarządzalnym profilu bezpieczeństwa w wielu przypadkach. Choć potrzebne są większe, kontrolowane badania, wyniki te wspierają dalsze testy abemacyklibu — możliwe w skojarzeniu z innymi terapiami — i przybliżają dziedzinę do prawdziwie spersonalizowanej opieki pacjentów z oponiakami wysokiego stopnia.
Cytowanie: Brastianos, P.K., Dooley, K., Geyer, S. et al. Abemaciclib in meningiomas with somatic NF2 or CDK pathway alterations: the phase 2 Alliance A071401 trial. Nat Med 32, 717–724 (2026). https://doi.org/10.1038/s41591-025-04141-4
Słowa kluczowe: oponiak, abemacyklib, guz mózgu, terapia celowana, badanie kliniczne