Clear Sky Science · pl
Interpretable inflammation landscape of circulating immune cells
Dlaczego zapalenie we krwi ma dla ciebie znaczenie
Zapalenie leży u podstaw wielu chorób, od zapalenia stawów i astmy po COVID-19 i nowotwory. Mimo to lekarzom wciąż trudno jest odczytać sygnały zapalne organizmu w sposób, który jasno wyjaśnia, co idzie nie tak i jakie leczenie będzie najskuteczniejsze. To badanie tworzy ogromną „mapę” komórek odpornościowych krążących we krwi i pokazuje, jak te komórki mogą działać jako żywe, łatwe do pobrania markery do klasyfikacji szerokiego spektrum chorób zapalnych.
Budowanie gigantycznej mapy komórek odpornościowych
Aby odwzorować ten krajobraz, badacze przeanalizowali ponad 6,5 miliona komórek odpornościowych pobranych z krwi 1 047 osób. Ochotnicy obejmowali 19 stanów chorobowych, w tym choroby autoimmunologiczne, takie jak toczeń i reumatoidalne zapalenie stawów, przewlekłe choroby płuc, jak astma i POChP, infekcje takie jak COVID-19 i HIV oraz kilka nowotworów, a także dawców zdrowych. Przy użyciu analizy RNA pojedynczych komórek zmierzono, które geny są aktywne w każdej komórce, a następnie zastosowano zaawansowane metody statystyczne, by skorygować techniczne różnice między badaniami i pogrupować komórki w 64 odrębne stany komórkowe układu odpornościowego. Ten „Atlas Zapalenia” obejmuje zarówno dobrze znane typy — takie jak limfocyty T, B i monocyty — jak i bardziej wyspecjalizowane podtypy, które zmieniają się wraz z przebiegiem choroby.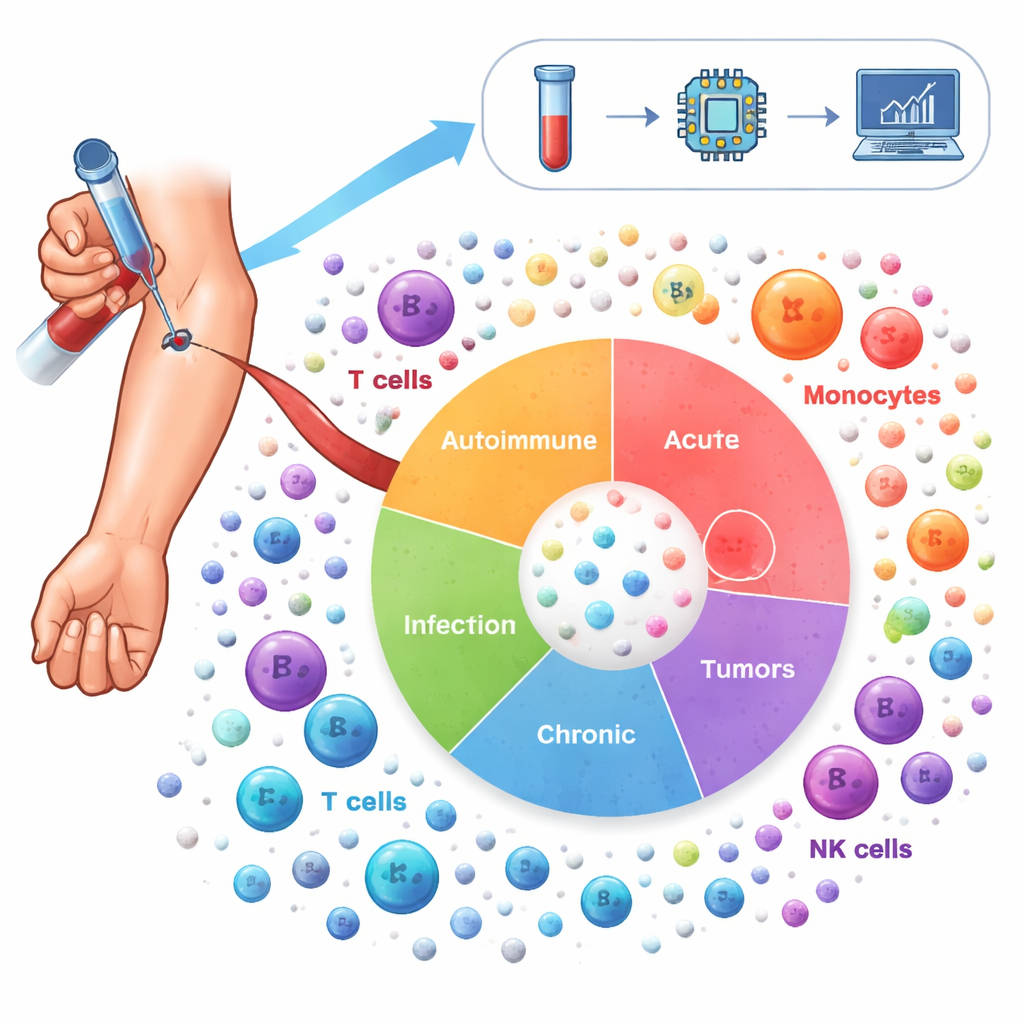
Odczytywanie zapalnych sygnatur organizmu
Zespół skupił się następnie na genach kontrolujących aktywację komórek odpornościowych, ich migrację, prezentację antygenów oraz reakcje na cząsteczki sygnałowe, takie jak interferony i czynnik martwicy nowotworów. Pogrupowali te geny w 21 biologicznych „sygnatur” i dopracowali je dla każdego głównego typu komórek. Porównując pacjentów z dawcami zdrowymi, mogli zobaczyć, które sygnatury są w różnych chorobach włączone lub wyciszone. Na przykład wiele chorób zapalnych o podłożu immunologicznym wykazywało silniejszą aktywność cząsteczek adhezyjnych i mechanizmów prezentacji antygenu, podczas gdy odpowiedzi interferonowe były osłabione w większości typów komórek, lecz nasilenie ich obserwowano w niektórych komórkach CD8 T. Infekcje wirusowe, takie jak grypa i COVID-19, wzmacniały programy indukowane przez interferony, podczas gdy przewlekłe infekcje, jak HIV i wirusowe zapalenie wątroby typu B, je osłabiały.
Skupianie się na kluczowych genach i przełącznikach kontrolnych
Ponieważ szerokie sygnatury wciąż ukrywają istotne szczegóły, badacze zagłębili się w poszczególne geny i ich regulatorów. W nie‑naiwnych komórkach CD8 T odkryli, że dwa geny, FGFBP2 i GZMB, są szczególnie aktywne w określonych podtypach pamięci efektorowej, zwłaszcza w wrzodziejącym zapaleniu jelita grubego. Geny te wiązane są z uszkodzeniem powierzchni nabłonkowych, a ich silny sygnał we krwi sugeruje, że te agresywne komórki są już „zaprzyjaźnione” przed wejściem do tkanek. Osobna analiza sieci regulacji genów wyodrębniła dwa czynniki transkrypcyjne, STAT1 i SP1, jako centralne regulatory programów indukowanych przez interferony. Ich wzorce aktywności różniły się między chorobami i typami komórek — na przykład przeciwne zachowanie w monocytach w porównaniu z komórkami CD8 T w toczniu oraz zmiany między fazami zaostrzenia a remisji — co sugeruje, jak te same szlaki mogą być ochronne w jednym kontekście, a szkodliwe w innym.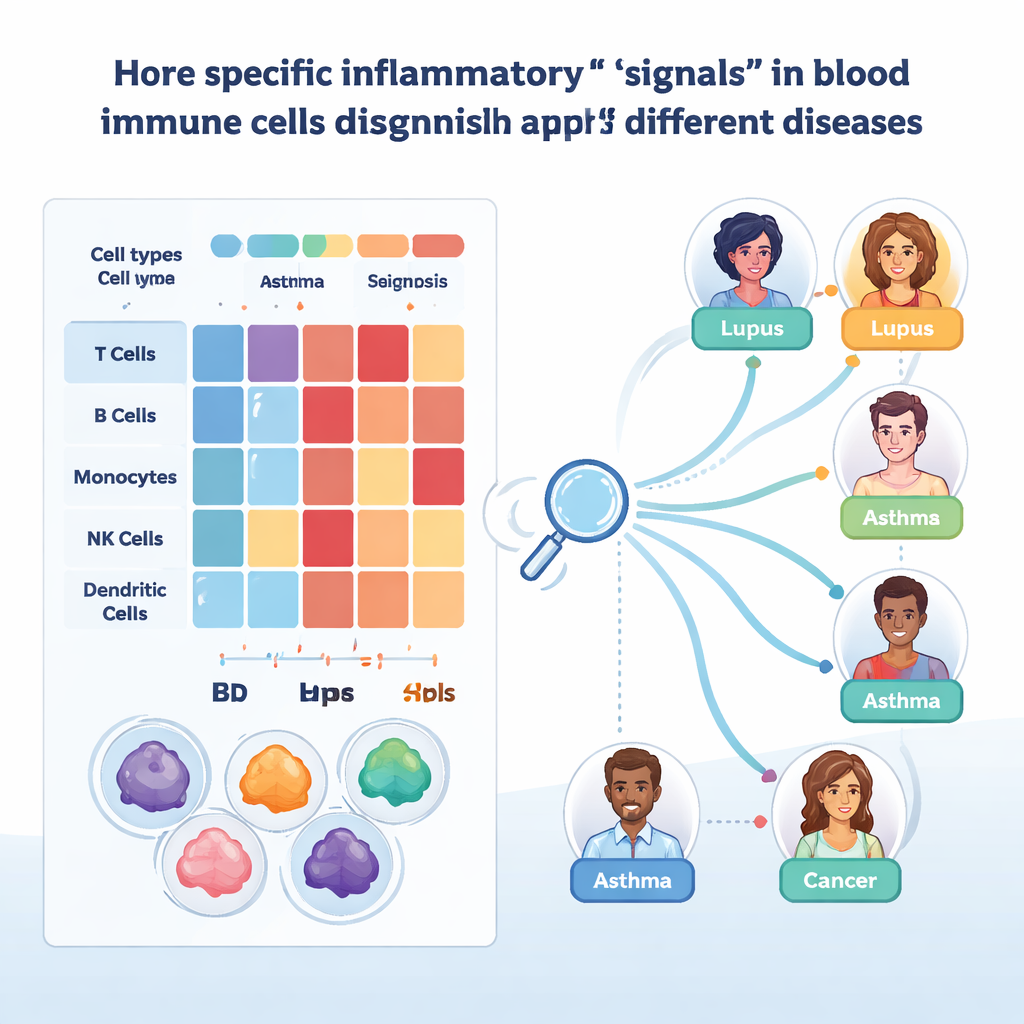
Uczenie maszynowe rozpoznające chorobę na podstawie komórek krwi
Aby przekształcić atlas w narzędzie praktyczne, zespół zastosował interpretowalne metody uczenia maszynowego. Trenowali modele typu gradient-boosted decision tree oddzielnie dla każdego głównego typu komórek, prosząc algorytmy, by oznaczały poszczególne komórki właściwą chorobą na podstawie ich ekspresji genów. Modele te osiągały wysoką dokładność w testach na wydzielonych próbkach, zwłaszcza po korekcie technicznych różnic. Dzięki metodzie SHAP, która wyjaśnia, które geny napędzają daną decyzję, badacze mogli zidentyfikować kandydatów na biomarkery. Przykładem jest CYBA w monocytach, którego poziomy pomagały odróżnić choroby skóry, takie jak łuszczyca, od zapalenia jelita w chorobie Crohna i wrzodziejącym zapaleniu jelita grubego. Innym przykładem jest IFITM1 w niektórych limfocytach T i komórkach limfoidalnych wrodzonych, rozróżniający astmę od POChP i wskazujący na różne wzorce przewlekłej obrony przeciwwirusowej.
W kierunku diagnostycznej kompasy opartej na krwi
Na koniec autorzy zapytali, czy całych pacjentów — nie tylko pojedyncze komórki — da się klasyfikować na podstawie ich krążących profili odpornościowych. Rzutowali dane każdej komórki do skompresowanej przestrzeni „osadzeń” (embedding), uśredniali te osadzenia według typu komórek dla każdego pacjenta i trenowali klasyfikatory do przewidywania choroby. Gdy nowi pacjenci przypominali tych z danych treningowych, wyniki były doskonałe. Jednak gdy próbki pochodziły z całkowicie niezależnych badań wykorzystujących różne metody laboratoryjne, dokładność spadała gwałtownie, ujawniając, jak wrażliwe są takie narzędzia na zmienność techniczną. Bardziej kontrolowany, „centralizowany” zbiór danych, wygenerowany w jednym ośrodku przy użyciu jednej chemii sekwencjonowania, przywracał dużą część wydajności, wskazując na potrzebę ujednoliconych protokołów lub bardzo dużych, zróżnicowanych zbiorów treningowych.
Co to oznacza dla przyszłej diagnostyki i leczenia
Dla laika kluczowym przekazem jest to, że twoje krążące komórki odpornościowe niosą bogaty odcisk tego, jak organizm jest zapalny. Odczytując te odciski komórka po komórce, praca ta pokazuje, że możliwe jest rozróżnienie wielu chorób, odkrywanie genów, które mogą napędzać specyficzne objawy, oraz zaczynanie budowy uniwersalnych testów krwi klasyfikujących choroby zapalne. Badanie nie jest jeszcze gotowym testem klinicznym — techniczne różnice między studiami nadal ograniczają wiarygodność — lecz tworzy podstawy dla przyszłych narzędzi „płynnej biopsji”, które mogłyby pomóc lekarzom we wcześniejszym ustaleniu właściwej diagnozy i leczenia, używając prostego pobrania krwi.
Cytowanie: Jiménez-Gracia, L., Maspero, D., Aguilar-Fernández, S. et al. Interpretable inflammation landscape of circulating immune cells. Nat Med 32, 633–644 (2026). https://doi.org/10.1038/s41591-025-04126-3
Słowa kluczowe: inflammation, immune cells, single-cell RNA sequencing, biomarkers, machine learning