Clear Sky Science · pl
CD38 zapewnia komórkom regulatorowym T swoistym dla antygenu odporność na stres, umożliwiając kontrolę miejscowego zapalenia OUN
Dlaczego mają znaczenie komórki odpornościowe strzegące mózgu
Wiele autoimmunologicznych chorób mózgu, takich jak stwardnienie rozsiane, przypomina tlące się pożary: początkowy wybuch zapalenia przygasa, ale uszkodzenia mogą nawracać po latach. Badanie stawia pozornie proste pytanie o dalekosiężnych konsekwencjach: po ataku w ośrodkowym układzie nerwowym (OUN) — co utrzymuje spokój, a co przechyla równowagę z powrotem ku chorobie? Autorzy skupiają się na niewielkiej populacji komórek odpornościowych zwanych komórkami T regulatorowymi, które osiedlają się w mózgu i rdzeniu kręgowym po zapaleniu, i pokazują, jak pojedyncza cząsteczka powierzchniowa pozwala im przetrwać w nieprzyjaznym środowisku i zapobiegać nawrotom.
Utrzymujący się lokalny oddział strażników immunologicznych
Wykorzystując model myszy odzwierciedlający wybrane cechy stwardnienia rozsianego, badacze śledzili różne typy limfocytów T w przebiegu choroby od nasilenia do fazy rekonwalescencji. Podczas gdy zwykłe pomocnicze komórki T napędzające zapalenie malały w liczbie wraz z poprawą objawów, komórki T regulatorowe — wyspecjalizowane komórki tłumiące reakcje immunologiczne — pozostawały w OUN. Ich względny udział w lokalnej puli limfocytów T faktycznie wzrósł, a komórki te skupiały się w odrębnych niszach wokół przestrzeni płynu mózgowo-rdzeniowego i ochronnych opon mózgowych. Oznaczając miejsca pochodzenia napływających komórek, zespół wykazał, że po wycofaniu się choroby do OUN dociera bardzo niewiele nowych komórek T regulatorowych z węzłów chłonnych. Zamiast tego populacja w OUN utrzymywała się głównie lokalnie, co sugeruje istnienie długotrwałej rezydentnej „siły pokojowej”. 
Odporni na stres strażnicy w nieprzyjaznej niszy
Postzapalne środowisko OUN jest dla tych strażników dalekie od komfortowego. Po głównej fali choroby spada poziom sygnału wzrostowego interleukiny-2 (IL-2) — od którego komórki T regulatorowe silnie zależą — ponieważ większość konwencjonalnych komórek T się wycofała. Równocześnie tkanka zawiera dużo metabolicznej cząsteczki NAD+, która może wywoływać śmierć komórki lub osłabiać kluczowe receptory powierzchniowe, gdy zostanie zmodyfikowana przez określony enzym. Poprzez genetyczne znakowanie i śledzenie pojedynczych komórek T regulatorowych autorzy rozróżnili „stabilne” komórki, które zachowały swoją tożsamość, od „niestabilnych”, które utraciły charakterystyczny program Foxp3. Komórki stabilne wykazywały znacznie wyraźniejszy sygnaturowy zapis sygnalizacji IL-2 i wyższe poziomy receptorów dla IL-2, co sugeruje, że zdolność do wyczuwania skąpej IL-2 jest kluczowa do przetrwania w tym zestresowanym środowisku.
Lokalna kontrola nawrotów z wnętrza mózgu
Aby sprawdzić, czy te rezydentne komórki T regulatorowe rzeczywiście mają znaczenie dla długoterminowej kontroli choroby, badacze selektywnie usunęli je z OUN, stosując toksynę podaną bezpośrednio do płynu mózgowo-rdzeniowego, pozostawiając większość systemowych komórek T regulatorowych nienaruszoną w reszcie ciała. W ciągu kilku dni myszy w trakcie rekonwalescencji doświadczyły ciężkich nawrotów z nawracającym porażeniem. Natomiast usunięcie komórek T regulatorowych jedynie w organizmie, oszczędzając te w OUN, nie wywołało zaostrzeń. Nawrót obejmował szybką reaktywację i ekspansję efektorowych komórek T, które już osiadły w OUN, nawet gdy ich rekrutacja z krwi została zablokowana. To dowodzi, że lokalne komórki T regulatorowe, a nie krążące, są niezbędne do powstrzymania pozostających po ataku agresywnych komórek.
Jak jeden enzym chroni komórki regulatorowe
Zagłębiając się mechanistycznie, autorzy szukali cząsteczek odróżniających odporne na stres komórki T regulatorowe w OUN. Wyłonił się kluczowy gracz: CD38, enzym na powierzchni komórki, który rozkłada zewnątrzkomórkowe NAD+. W zapalnym OUN komórki T regulatorowe silnie zwiększały ekspresję CD38, podczas gdy komórki konwencjonalne nie wykazywały tak wyraźnej zmiany. Gdy zespół przeszczepił do myszy regulatorowe komórki T reagujące na mielinę pozbawione CD38, te komórki dotarły do OUN, lecz nie potrafiły kontrolować choroby, w przeciwieństwie do swoich normalnych odpowiedników. W chimerycznych zwierzętach mieszanych, gdzie tylko rezydentne komórki T regulatorowe były pozbawione CD38, usunięcie frakcji z CD38 wystarczającej spowodowało nawroty, co pokazuje, że CD38 działa w sposób wewnątrzkomórkowy, umożliwiając skuteczną kontrolę.
Ochrona sygnału podtrzymującego życie
Doświadczenia mechanistyczne ujawniły, jak CD38 zapewnia tę odporność. Wysokie poziomy NAD+ w OUN mogą napędzać chemiczną modyfikację białek powierzchniowych przez enzym ARTC2.2. Jednym z wrażliwych celów jest podjednostka o wysokim powinowactwie receptora dla IL-2, którą komórki T regulatorowe wyrażają na bardzo wysokim poziomie, zwłaszcza gdy rozpoznają antygeny mózgowe. U komórek T regulatorowych pozbawionych CD38, narażonych na NAD+, większość receptorów IL-2 ulegała modyfikacji, prowadząc do słabszej aktywacji przekaźnika STAT5 i obniżonej odpowiedzi na IL-2. W przeciwieństwie do tego, komórki wyrażające CD38 lokalnie obniżały stężenie NAD+ wokół siebie, ograniczając szkodliwą modyfikację i zachowując silną sygnalizację IL-2. U żywych myszy wstrzyknięcie NAD+ do mózgu selektywnie zabiło większość komórek T regulatorowych przez tę drogę, oszczędzając komórki konwencjonalne, co podkreśla, jak kruche jest to środowisko bez ochronnego enzymu. 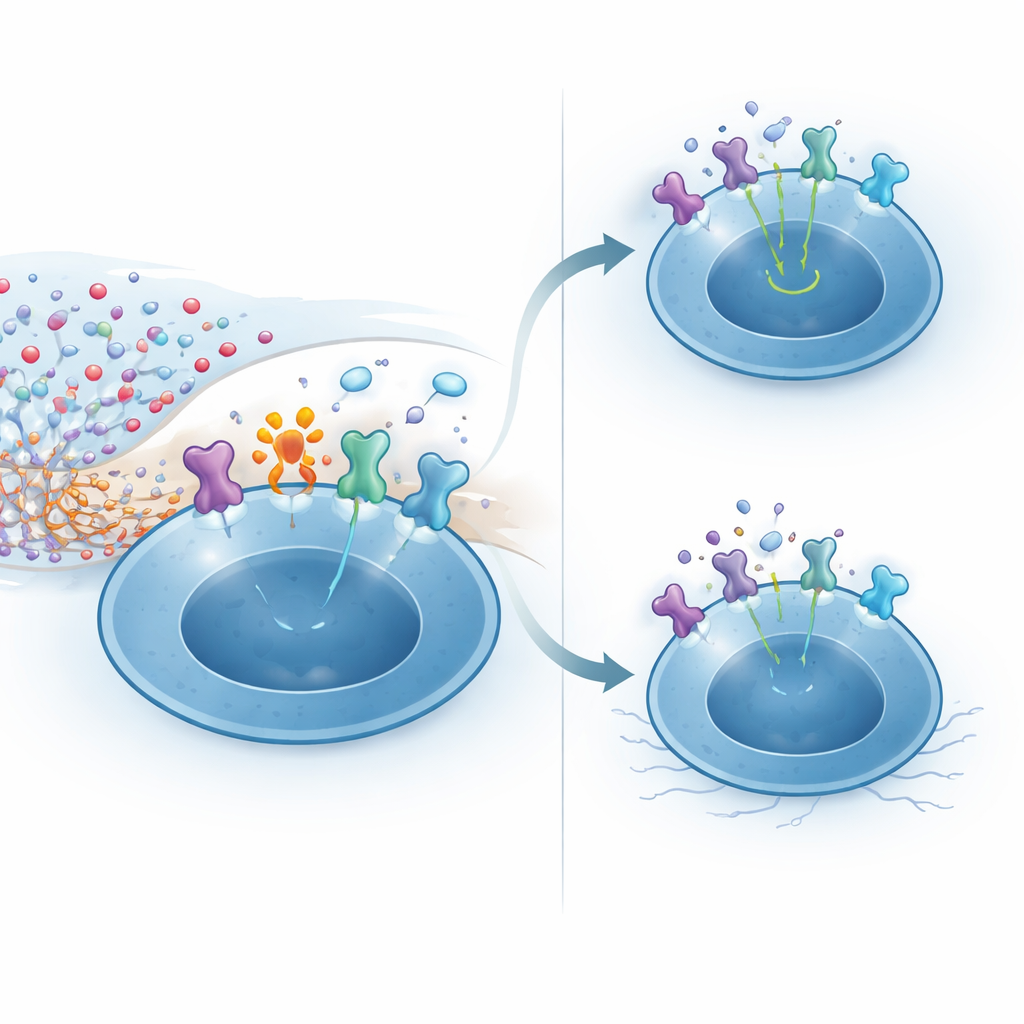
Co to oznacza dla przewlekłej autoimmunizacji mózgu
Ta praca kreśli obraz przewlekłej autoimmunizacji OUN jako skompartmentalizowanej bitwy: małe skupiska pozostających agresywnych komórek T rezydują w mózgu i rdzeniu kręgowym, powstrzymywane przez równie wyspecjalizowane lokalne komórki T regulatorowe. Ci strażnicy są „odporni na stres”, ponieważ CD38 pozwala im przetrwać wysokie poziomy NAD+ i dalej wyczuwać minimalne ilości IL-2, zachowując tożsamość i funkcję supresyjną. Dla czytelników niebędących specjalistami kluczowy wniosek jest taki, że długoterminowa kontrola chorób takich jak stwardnienie rozsiane może zależeć mniej od układu odpornościowego krążącego we krwi, a bardziej od pielęgnowania i ochrony tych rezydentnych strażników w samym mózgu — potencjalnie poprzez ukierunkowanie szlaków zwiększających funkcję CD38 lub wrażliwość na IL-2 w komórkach T regulatorowych.
Cytowanie: Chen, HH., Tyystjärvi, S., Ruiz Navarro, D. et al. CD38 endows local antigen-specific Treg cells with stress resilience for control of compartmentalized CNS inflammation. Nat Immunol 27, 516–529 (2026). https://doi.org/10.1038/s41590-025-02416-z
Słowa kluczowe: komórki T regulatorowe, stwardnienie rozsiane, zapalenie ośrodkowego układu nerwowego, enzym CD38, tolerancja immunologiczna