Clear Sky Science · pl
Specyficzność antygenowa klonalnie wzbogaconych komórek CD8+ T w stwardnieniu rozsianym
Dlaczego te badania są ważne dla ludzi
Stwardnienie rozsiane (SR) to choroba, w której własny układ odpornościowy atakuje mózg i rdzeń kręgowy, ale dokładne czynniki wywołujące ten atak pozostają niejasne. Jednym z długo podejrzewanych sprawców jest wirus Epsteina–Barra (EBV) — bardzo powszechny wirus zakażający większość ludzi w ciągu życia. W tym badaniu badacze zajrzeli bezpośrednio do płynu otaczającego mózg, aby sprawdzić, jakie komórki odpornościowe się tam znajdują, co robią i, co istotne, na co reagują. Zrozumienie tego związku mogłoby zmienić sposób, w jaki diagnozujemy, monitorujemy i ostatecznie leczymy SR.
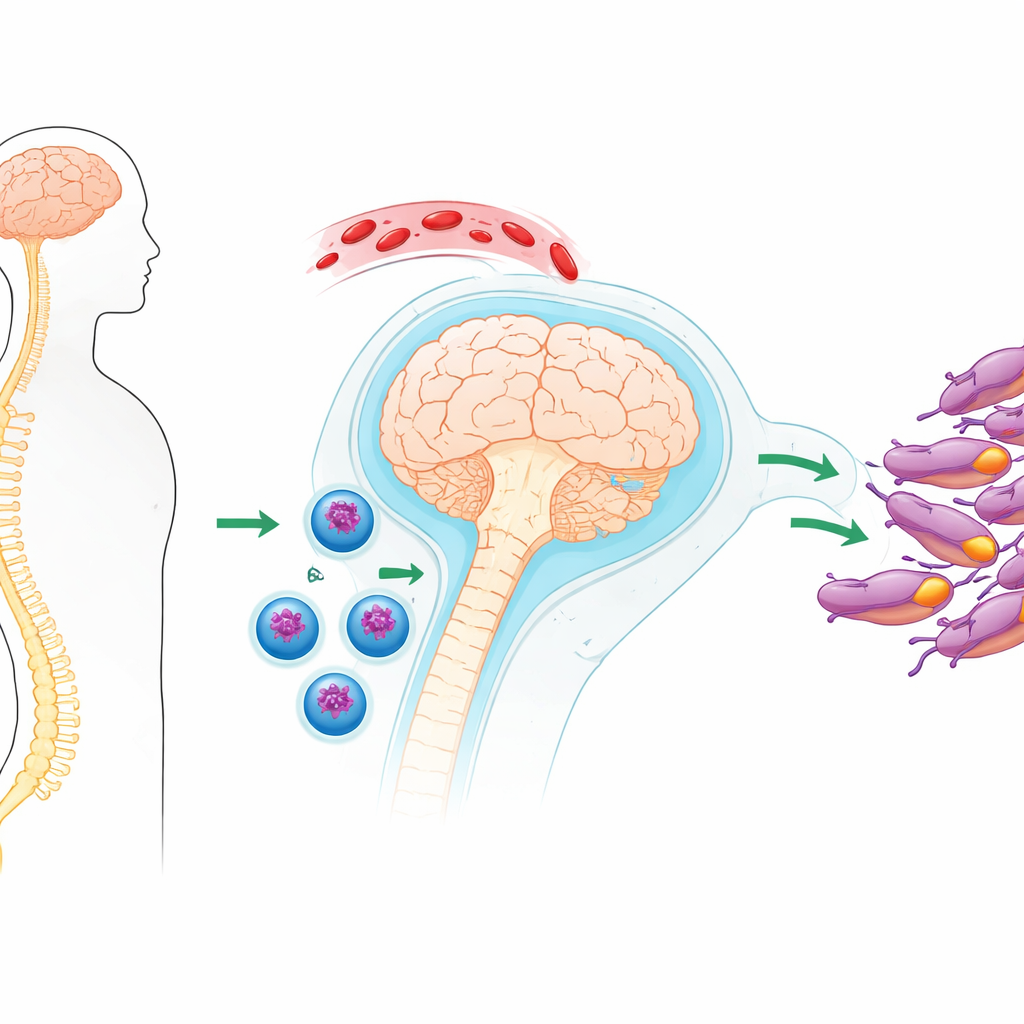
Komórki odpornościowe na miejscu
Badacze przeanalizowali próbki krwi i płynu mózgowo‑rdzeniowego od 18 osób: pacjentów z wczesnym SR lub pokrewnym pierwszym atakiem, osób z innymi zapalnymi schorzeniami mózgu oraz zdrowych ochotników. Przy użyciu wysokorozdzielczego sekwencjonowania pojedynczych komórek skatalogowali dziesiątki tysięcy pojedynczych komórek T — typu białych krwinek, które potrafią rozpoznawać i zabijać zakażone lub nieprawidłowe komórki. Stwierdzili, że w płynie otaczającym mózg komórki T u pacjentów z SR wyglądały na bardziej aktywowane i lepiej przygotowane do wnikania w tkanki oraz wykonywania funkcji niszczących niż komórki T uczestników kontrolnych.
Mała, ale potężna grupa nawracających sprawców
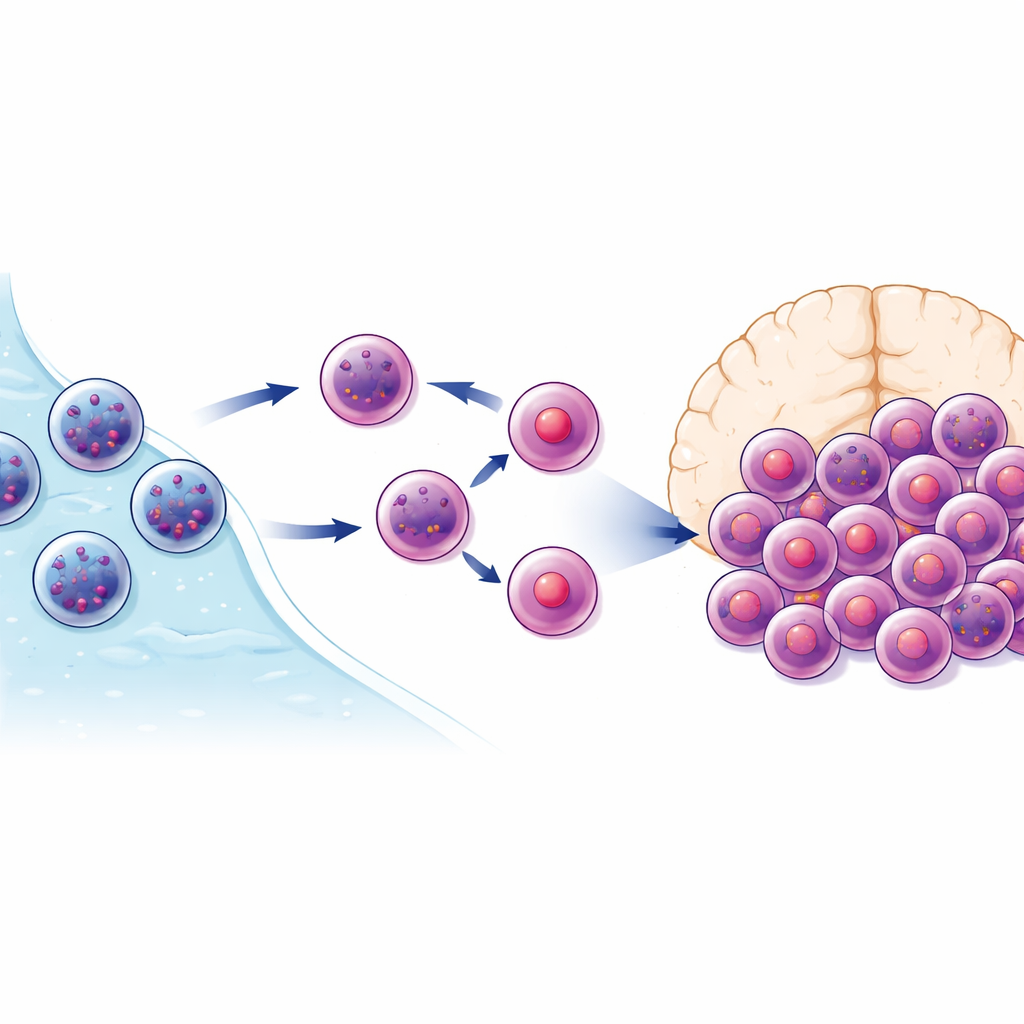
Komórki T, które wielokrotnie spotykają swój cel, rozrastają się w klony — duże rodziny niemal identycznych komórek. Gdy zespół analizował sekwencje receptorów komórek T, które służą jako znaczniki ID dla każdego klonu, odkrył niewielki podzbiór klonów komórek CD8 T, które były silnie rozrośnięte i niezwykle wzbogacone w płynie mózgowo‑rdzeniowym w porównaniu z krwią. Ponad 70% tych wzbogaconych klonów stanowiły komórki CD8, podtyp wyspecjalizowany w zabijaniu. Komórki te nosiły genetyczne sygnatury doświadczonych wojowników: wyrażały molekuły związane z wnikaniem w tkanki, osiedlaniem się w ośrodkowym układzie nerwowym oraz potężnym aparatem zabijającym komórki. U niektórych pacjentów z SR garstka takich klonów stanowiła znaczący ułamek wszystkich komórek T w płynie mózgowo‑rdzeniowym.
Śledząc ślad do powszechnego wirusa
Kluczowe pytanie brzmiało, co te dominujące klony komórek T rozpoznają. Autorzy sklonowali receptory z 23 najbardziej wzbogaconych klonów CD8 T i przetestowali je przeciwko ogromnym bibliotekom kandydackich fragmentów wirusów i białek ludzkich. Kilka sztucznych peptydów „mimików” wiązało się z niektórymi receptorami, ale nie wywoływało ich niezawodnej aktywacji, co sugerowało, że nie są to ich prawdziwe cele. Jednak trzy niezależne klony CD8 T od trzech różnych pacjentów z SR reagowały silnie i specyficznie na znane białka EBV. Te ukierunkowane na wirusa klony były nie tylko liczne w płynie mózgowo‑rdzeniowym; ich profile genetyczne sugerowały, że aktywnie uczestniczą w kontrolowaniu zakażenia, a nie pozostają w stanie spoczynku.
Objawy aktywności wirusa w płynie mózgowym
Aby sprawdzić, czy sam EBV jest obecny, badacze zmierzyli DNA i RNA EBV w płynie mózgowo‑rdzeniowym. Wykryli materiał genetyczny EBV u większości uczestników, co odzwierciedla powszechność tego wirusa w populacji ogólnej. Jednak pewne transkrypty EBV związane z reaktywacją wirusa były wyższe u osób z SR lub z pierwszym zdarzeniem demielinizacyjnym niż u kontrolnych. Co istotne, pacjenci, którzy mieli silnie rozrośnięte EBV‑specyficzne komórki CD8 w płynie mózgowo‑rdzeniowym, także mieli tendencję do obecności sygnatur EBV w tym płynie. Ten wzorzec wskazuje na scenariusz, w którym EBV staje się aktywny w lub w pobliżu ośrodkowego układu nerwowego, przyciągając i rozszerzając wyspecjalizowane komórki T walczące z wirusem.
Co to znaczy dla zrozumienia SR
W sumie badanie pokazuje, że we wczesnym, nieleczonym SR, płyn otaczający mózg zawiera niewielką, ale wyraźną populację komórek CD8 T, które są silnie rozrośnięte, uzbrojone do uszkodzeń tkanek i w kilku przypadkach specyficznie nastawione na rozpoznawanie EBV. Równocześnie ślady genetyczne EBV są obficiej obecne w płynie mózgowo‑rdzeniowym tych pacjentów. Chociaż praca ta nie dowodzi, że EBV bezpośrednio powoduje SR ani że te komórki T atakują osłonki mielinowe, dostarcza mocnych przesłanek, że EBV odgrywa istotną rolę w środowisku chorobowym. To powiązanie może w przyszłości umożliwić lekarzom śledzenie istotnych dla choroby komórek odpornościowych w płynie rdzeniowym oraz zainspirować terapie celujące albo w sam EBV, albo modulujące wirus‑specyficzne komórki T gromadzące się w mózgach osób z SR.
Cytowanie: Hayashi, F., Mittl, K., Dandekar, R. et al. Antigen specificity of clonally enriched CD8+ T cells in multiple sclerosis. Nat Immunol 27, 490–502 (2026). https://doi.org/10.1038/s41590-025-02412-3
Słowa kluczowe: stwardnienie rozsiane, wirus Epsteina–Barra, komórki T CD8, płyn mózgowo‑rdzeniowy, autoimmunologiczne zapalenie układu nerwowego