Clear Sky Science · pl
Rozwikłanie decyzji linii CD8 ujawnia, że funkcjonalnie różne komórki CD8+ są selekcjonowane przez odmienne grasico‑pochodne peptydy MHC‑I
Jak komórki cytotoksyczne wybierają swoje role
Nasz układ odpornościowy polega na limfocytach CD8, często nazywanych komórkami zabójcami, które eliminują komórki zainfekowane wirusem lub nowotworowe. Jednak nie wszystkie komórki CD8 zachowują się tak samo: jedne są bezwzględnymi zabójcami, inne pełnią bardziej pomocniczą rolę, a jeszcze inne rodzą się przygotowane jako komórki „pamięci” gotowe do szybkiej reakcji. Badanie to ujawnia, jak w trakcie krótkiego okresu dojrzewania w grasicy komórki CD8 są kierowane na te różne ścieżki przez precyzyjne sygnały, które otrzymują z otaczających tkanek.
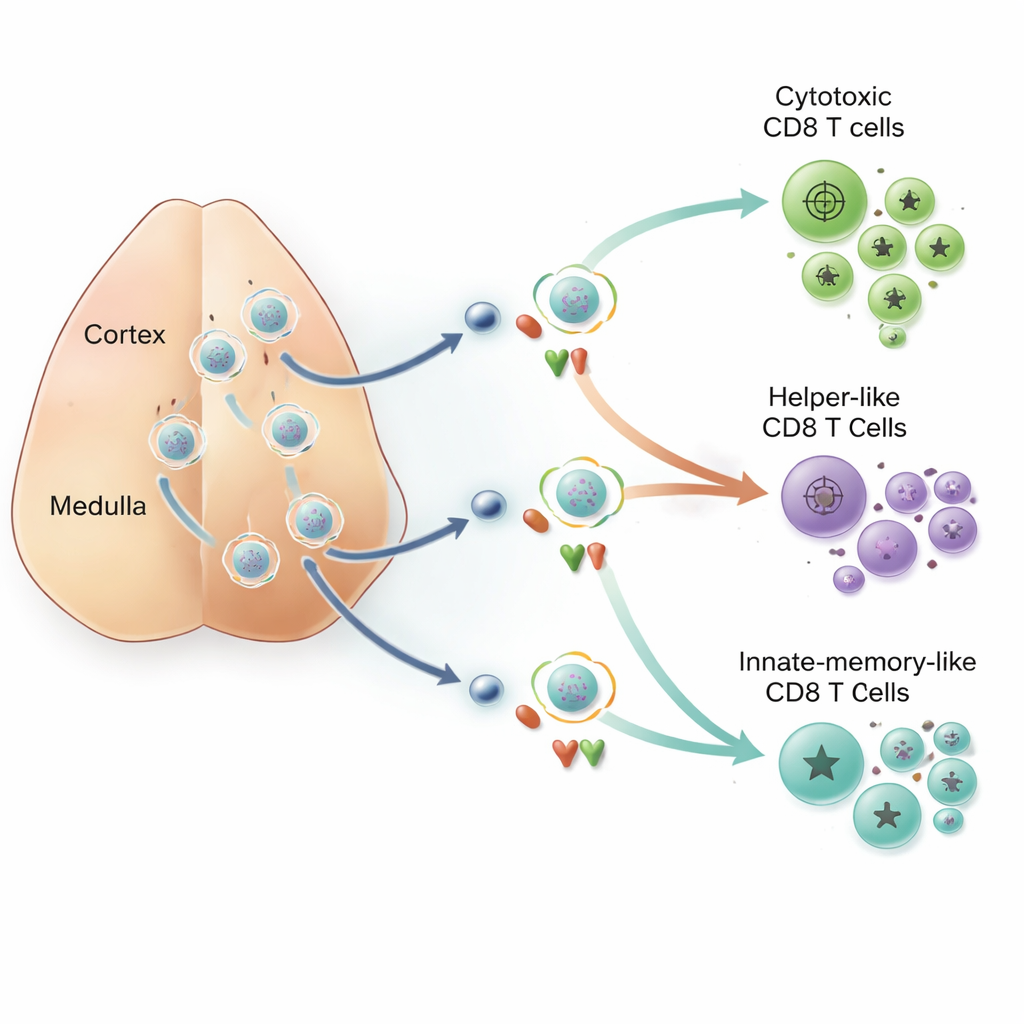
Szkoła doskonalenia wewnątrz klatki piersiowej
Głęboko w klatce piersiowej grasica pełni rolę szkoły doskonalenia dla niedojrzałych limfocytów T. Tam rozwijające się komórki nieustannie sprawdzają swoje receptory względem małych fragmentów białek, czyli peptydów, prezentowanych na innych komórkach. Tylko te, które rozpoznają własne molekuły organizmu z odpowiednią siłą, mogą dojrzewać. Autorzy skupili się na limfocytach CD8, które są selekcjonowane przez peptydy prezentowane na cząsteczkach MHC klasy I. Wcześniejsze modele sugerowały, że to, czy limfocyt stanie się typem pomocniczym czy zabójczym, zależało głównie od tego, który powierzchniowy „współreceptor” był wyrażany i jak długo receptor sygnalizował podczas selekcji. Dokładny sposób, w jaki te elementy współdziałają, oraz rola samych peptydów pozostawały jednak niejasne.
Przeprogramowanie limfocytów ujawnia ukryte wybory
Aby zbadać te zagadnienia, badacze stworzyli myszy nazwane CD8Dual, w których oba zwykłe miejsca genowe współreceptorów zostały przeprogramowane tak, aby produkować współreceptory typu CD8. Ten sprytny zabieg sprawił, że wszystkie rozwijające się limfocyty w tych zwierzętach były nastawione na rozpoznawanie MHC klasy I, co pozwoliło zespołowi wyizolować wpływ samych wzorców sygnalizacji na losy komórek. Ku zaskoczeniu, mimo że komórki używały tego samego rodzaju współreceptora i rozpoznawały tę samą klasę MHC, wyłoniły się dwie odrębne populacje limfocytów CD8. Jedna grupa, oznaczona aktywnością czynnika nazwanego ThPOK, zachowywała się jak klasyczne komórki pomocnicze: wyrażała molekuły komunikujące się z innymi komórkami układu odpornościowego i mogła przekształcać się w komórki regulatorowe lub przypominające natural killer T. Druga grupa, oznaczona czynnikiem Runx3, miała molekularne i funkcjonalne cechy cytotoksycznych zabójców.
Czas trwania sygnału i podróż przez grasicę
Dlaczego genetycznie podobne komórki rozdzieliły się tak wyraźnie? Śledząc markery powierzchniowe raportujące niedawną aktywność receptorów, autorzy pokazali, że komórki korzystające z jednego loci genowego doświadczały ciągłej sygnalizacji podczas migracji z kory grasicy do głębszych jej obszarów; komórki te przyjęły los pomocniczy. W przeciwieństwie do nich, komórki polegające na drugim locus doświadczyły przerwy w sygnalizacji, po której lokalne cytokiny skierowały je ku tożsamości cytotoksycznej. To wspierało ideę, że to czas trwania sygnału, bardziej niż jego sama obecność, decyduje o roli limfocytu CD8. Pojawiła się jednak dodatkowa zagadka: nawet gdy wszystkie komórki miały dokładnie ten sam receptor dla tego samego peptydu — używając specjalnych myszy z monoklonalnym receptorem T‑komórkowym — niektóre nadal stawały się komórkami pomocniczymi, a inne zabójczymi. To wskazywało na kolejny poziom kontroli: naturę i lokalizację peptydów dokonujących selekcji.
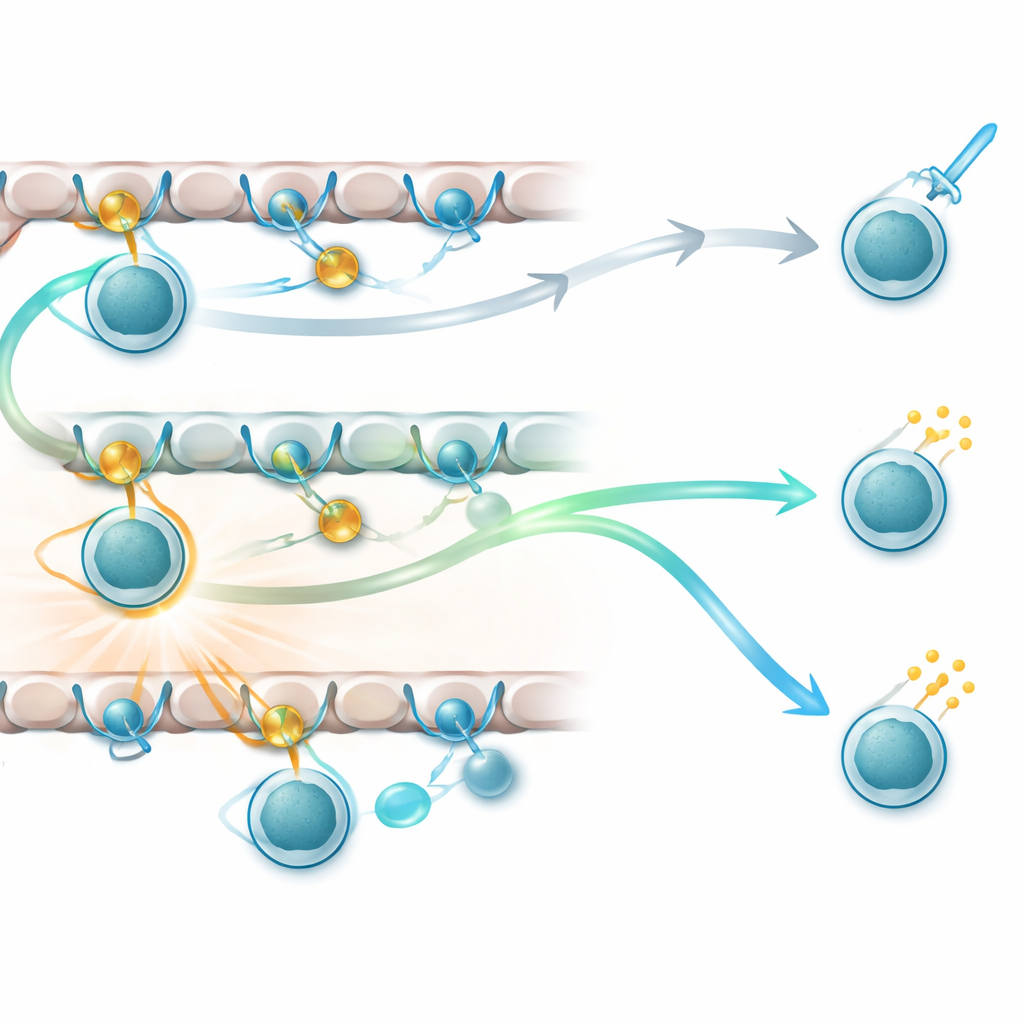
Różne peptydy, różne przyszłości
W grasicy fragmenty peptydów powstają dzięki molekularnym „szatkownicom” zwanym proteasomami. Specjalizowana wersja, zwana tymoproteasomem, wytwarza zestaw peptydów znanych jako peptydy β5t, które pojawiają się tylko na komórkach w zewnętrznej korze. Inne, szerzej występujące peptydy, określane jako nie‑β5t, są obecne zarówno w korze, jak i w głębszych obszarach narządu. Porównując myszy normalne z tymi pozbawionymi β5t, zespół stwierdził, że peptydy β5t niemal wyłącznie generują konwencjonalne cytotoksyczne komórki CD8. Natomiast komórki CD8 o cechach pomocniczych oraz odrębna grupa „pamięci wrodzonej” CD8 — komórek opuszczających grasicę już przygotowanych do szybkiej reakcji — były selekcjonowane jedynie przez szeroko rozpowszechnione peptydy nie‑β5t. Te komórki pamięci wrodzonej powstawały, gdy rozwijające się komórki typu cytotoksycznego ponownie napotykały peptydy nie‑β5t później w swojej wędrówce, otrzymując drugą falę sygnałów w środowisku bogatym w cytokinę IL‑4.
Znaczenie dla odporności
Mówiąc wprost, praca ta pokazuje, że nie wszystkie własne peptydy w grasicy są równoważne. Peptydy występujące jedynie w korze dają limfocytom krótki impuls instrukcji, który następnie zanika, produkując klasyczne komórki zabójcze CD8. Peptydy napotykane wielokrotnie, w miarę jak komórki migrują w głąb grasicy, mogą wydłużyć lub na nowo wzbudzić sygnalizację. Gdy sygnał jest mocny i ciągły, komórki CD8 przyjmują cechy pomocnicze; gdy pojawia się później i łączy się ze specyficznymi lokalnymi cytokinami, stają się komórkami pamięci wrodzonej. Łącząc typ peptydu, miejsce jego ekspozycji w grasicy oraz czas trwania zaangażowania receptorów T, badanie wyjaśnia, jak pojedynczy narząd szkoleniowy może wygenerować zróżnicowaną armię limfocytów CD8 przeznaczonych do natychmiastowego zabijania, koordynacji odpowiedzi immunologicznej lub szybkich reakcji pamięciowych.
Cytowanie: Shinzawa, M., Ramos, N., Bui, K. et al. Unraveling CD8 lineage decisions reveals that functionally distinct CD8+ T cells are selected by different MHC-I thymic peptides. Nat Immunol 27, 786–798 (2026). https://doi.org/10.1038/s41590-025-02411-4
Słowa kluczowe: rozwój limfocytów CD8, selekcja grasicy, peptydy MHC klasy I, limfocyty pamięci wrodzonej, losy linii limfocytów T