Clear Sky Science · pl
Przestrzenne wzorce sygnalizacji TGFβ w fibroblastach leżą u podstaw oporności na leczenie w reumatoidalnym zapaleniu stawów
Dlaczego uporczywy ból stawów ma znaczenie
Wiele osób z reumatoidalnym zapaleniem stawów przyjmuje nowoczesne leki tłumiące układ odpornościowy, a mimo to ich stawy pozostają bolesne i sztywne. Badanie stawia pytanie, dlaczego niektórzy pacjenci nie poprawiają się, nawet gdy zapalenie w stawie wydaje się ustępować. Poprzez dokładne zbadanie, gdzie i w jaki sposób określone komórki podporowe w stawie uruchamiają programy bliznowacenia, badacze odkrywają ukrytą formę uszkodzenia, która może wyjaśniać utrzymujący się ból i wskazywać nowe strategie terapeutyczne.
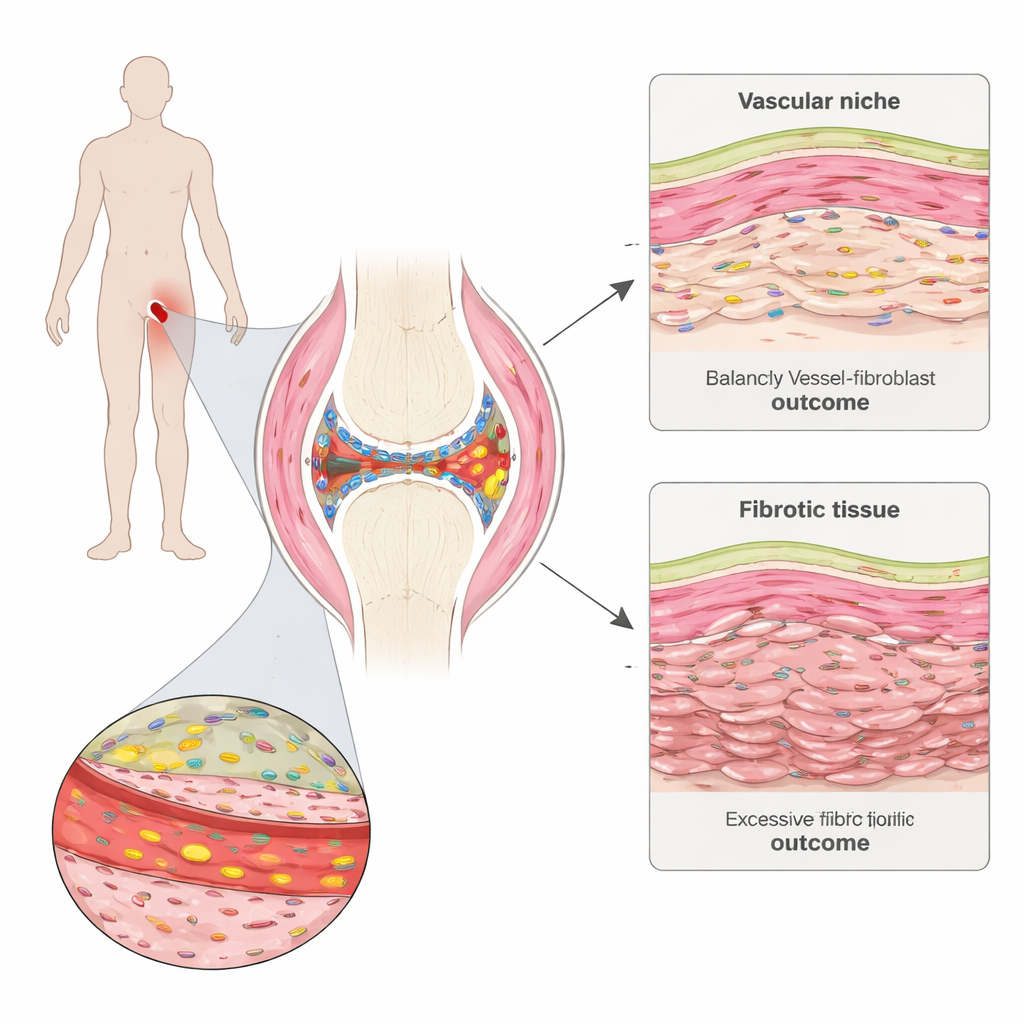
Bliższe spojrzenie do bolącego stawu
Reumatoidalne zapalenie stawów atakuje błonę maziową (synowium), cienką tkankę wyściełającą i nawilżającą stawy. Zespół pobrał drobne biopsje synowium od osób z wczesną chorobą przed rozpoczęciem terapii i ponownie po sześciu miesiącach. Dzięki zaawansowanemu mapowaniu ekspresji genów w przestrzeni mogli zobaczyć, które geny były aktywne w tysiącach pojedynczych komórek, zachowując jednocześnie informacje o ich położeniu w tkance. Zidentyfikowali wyraźne „sąsiedztwa” w synowium, w tym skupiska komórek odpornościowych, obszary bogate w tłuszcz, cienką wewnętrzną wyściółkę oraz rejony pełne naczyń krwionośnych i komórek strukturalnych zwanych fibroblastami.
Komórki tworzące blizny a oporność na leczenie
Porównując pacjentów, którzy później osiągnęli remisję, z tymi, którzy tego nie zrobili, badacze zauważyli uderzający wzorzec: przed leczeniem pacjenci nieuzyskujący remisji już mieli silniejsze sygnały włóknienia tkanki. Pewien program fibroblastów, charakteryzowany wysoką produkcją białka macierzy zewnątrzkomórkowej o nazwie COMP, był u tych pacjentów rozrośnięty. Te bogate w COMP fibroblasty dzieliły cechy z komórkami tworzącymi blizny obserwowanymi w włóknieniu płuc i skóry i były najsilniej powiązane ze słabą odpowiedzią na leczenie. Z upływem czasu rejony zdominowane przez te komórki miały tendencję do gęstego zapełniania tkanką łączną przy relatywnie niskiej liczbie komórek, co sugeruje, że odkładają sztywną macierz, która może utrzymywać się nawet po ustąpieniu zapalenia.
Naczynia krwionośne jako ukryci dyrygenci
Fibrogenne fibroblasty nie były rozproszone losowo. Grupowały się wokół naczyń krwionośnych, tworząc warstwowe strefy około-naczyniowe. Najwewnętrzniejsza warstwa, przylegająca do ściany naczynia, wyrażała inne geny niż warstwa zewnętrzna. Zespół wykazał, że komórki wyściełające naczynia krwionośne wysyłają sygnały Notch do pobliskich fibroblastów, które z kolei kształtują odpowiedź tych fibroblastów na rodzinę pro-bliznowatych bodźców znanych jako TGF‑beta. Blisko naczynia sygnalizacja Notch pobudza fibroblasty do wytwarzania TGF‑beta, ale jednocześnie obniża liczbę receptorów TGF‑beta na ich powierzchni, ograniczając ich wrażliwość. Dalej od naczynia, gdzie wpływ Notch słabnie, fibroblasty mają więcej receptorów i stają się wysoce responsywne, przekształcając się w komórki bogate w COMP, które napędzają włóknienie.
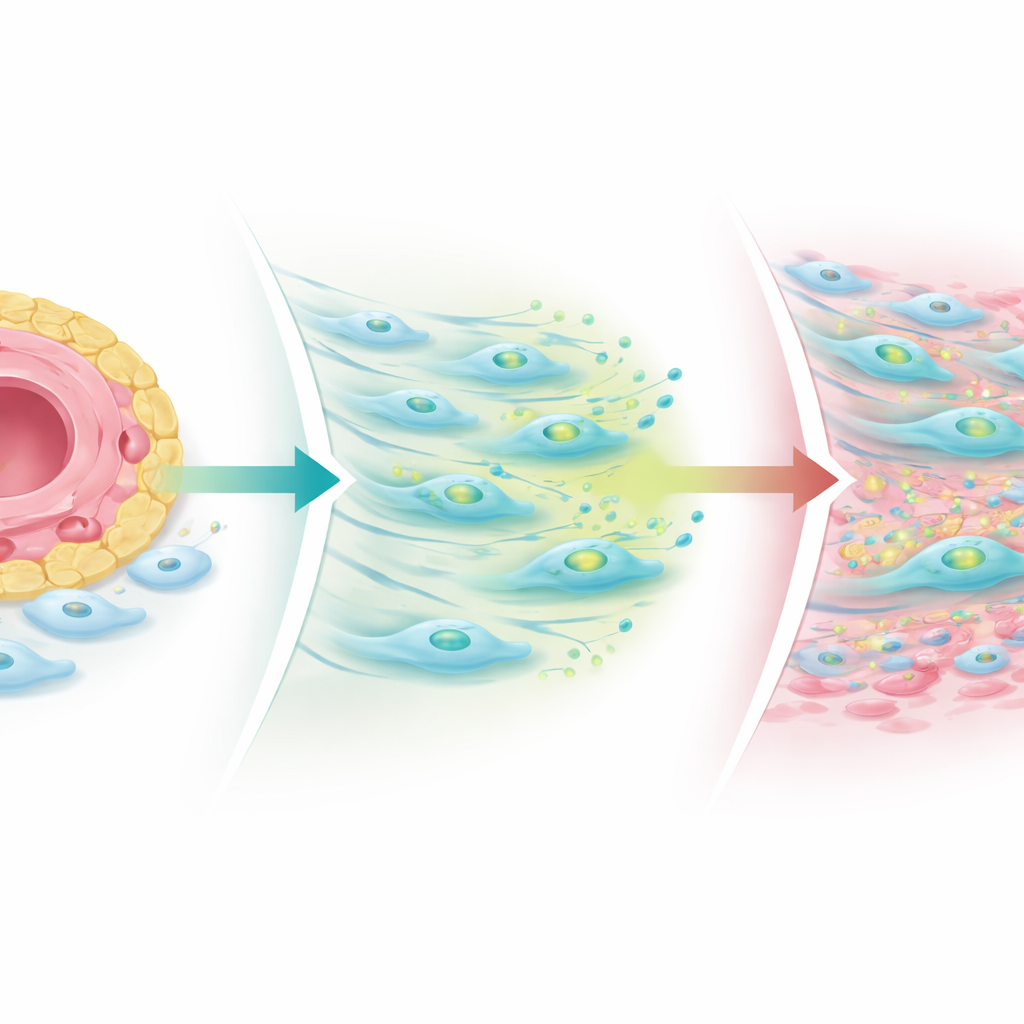
Co się dzieje, gdy równowaga zostaje zaburzona
Badacze zbudowali uproszczone modele stawu w naczyniach laboratoryjnych oraz trójwymiarowe organoidy pochodzące z tkanek pacjentów, aby zbadać ten mechanizm. Gdy wzmocnili sygnały Notch pochodzące od komórek śródbłonka, fibroblasty zwiększały produkcję TGF‑beta, ale redukowały poziom receptorów, ograniczając bliznowacenie. Gdy zablokowali Notch lub zaburzyli jego stały wzorzec, fibroblasty odzyskiwały receptory TGF‑beta — zwłaszcza koreceptor zwany receptorem III TGF‑beta — a komórki fibrogenne pozytywne dla COMP rozrastały się z dala od naczyń. W biopsjach pacjentów pobranych po leczeniu skupiska komórek odpornościowych zmniejszyły się u niemal wszystkich, ale nisze fibrogenne, szczególnie obszary bogate w COMP, często się powiększały, zwłaszcza u tych, u których ból stawów się utrzymywał. Sugeruje to, że standardowe leki przeciwzapalne mogą ugasić „ogień” układu odpornościowego, jednocześnie pozostawiając lub nawet odsłaniając proces bliznowacenia, który utrzymuje stawy sztywne i bolesne.
Nowe sposoby na uspokojenie uporczywych stawów
Na koniec zespół sprawdził, czy zakłócenie tego obwodu fibrogennego może mieć zastosowanie terapeutyczne. W organoidach pochodzących od pacjentów leki hamujące Notch lub blokujące sygnalizację TGF‑beta zmniejszały produkcję COMP, innych białek związanych ze bliznami oraz kluczowych kolagenów, a także przebudowywały aktywność genową w strefach około-naczyniowych. Dla nieprofesjonalnego obserwatora przekaz jest taki, że nie całe uszkodzenie w reumatoidalnym zapaleniu stawów wynika z widocznego zapalenia: część z niego jest „wbudowana” w komórki podporowe stawu i naczynia krwionośne. Celując w rozmowę Notch–TGF‑beta, która kontroluje, jak fibroblasty odkładają tkankę bliznowatą, przyszłe terapie mogą zapobiec lub odwrócić uporczywą, włóknistą postać choroby oporną na obecne leki ukierunkowane na układ odpornościowy.
Cytowanie: Bhamidipati, K., McIntyre, A.B.R., Kazerounian, S. et al. Spatial patterning of fibroblast TGFβ signaling underlies treatment resistance in rheumatoid arthritis. Nat Immunol 27, 556–571 (2026). https://doi.org/10.1038/s41590-025-02386-2
Słowa kluczowe: reumatoidalne zapalenie stawów, włóknienie, fibroblasty, sygnalizacja TGF‑beta, szlak Notch