Clear Sky Science · pl
Inżynieria ksylotransferaz do manipulowania proteoglikanami w komórkach ssaków
Dlaczego powłoki komórkowe mają znaczenie
Każda komórka w naszym organizmie nosi molekularną „powłokę”, która pomaga jej komunikować się z sąsiadami i odbierać sygnały ze środowiska. Ważną część tej powłoki stanowią proteoglikany — białka ozdobione długimi łańcuchami cukrowymi, które działają jak maleńkie anteny dla czynników wzrostu, sygnałów immunologicznych i wskazówek strukturalnych. Gdy to cukrowe upiększenie zawodzi, rozwój może zostać zaburzony, a tkanki takie jak kość i mięsień mogą być poważnie dotknięte. Naukowcy jednak mieli trudności z dokładnym zmapowaniem, które białka przenoszą te łańcuchy i jak poszczególne elementy powłoki wpływają na zachowanie komórek. W tym badaniu przedstawiono precyzyjną strategię chemiczną do znakowania i odbudowy tych łańcuchów cukrowych na żywych komórkach ssaków, otwierając drogę do odczytywania i przepisania informacji zapisanej na ich powierzchniach. 
Przeprojektowanie pierwszego kroku przyłączania cukru
Budowa proteoglikanów zaczyna się, gdy specjalna rodzina enzymów — ksylotransferazy XT1 i XT2 — dodaje pierwszy cukier do białka, oznaczając miejsce, w którym rozrośnie się długi łańcuch. Ponieważ oba enzymy mogą wykonać ten sam początkowy krok, trudno było rozróżnić, na których białkach działa każdy z nich wewnątrz komórek. Autorzy zastosowali strategię „bump‑and‑hole” — powszechną we współczesnej biologii chemicznej — aby to rozwiązać. Lekkо zmienili kształt miejsca aktywnego XT1, tworząc dodatkową przestrzeń („dziurę”), i wprowadzili dopasowany, nieco bardziej masywny składnik cukrowy, 6AzGlc („guzek”). Zmutowana XT1 może teraz używać tego zmodyfikowanego cukru, podczas gdy naturalny enzym nie potrafi, co pozwala badaczom oznaczać tylko te białka, które zostały dotknięte przez przeprojektowany enzym.
Przemycanie projektowanego cukru do komórek
Aby podejście zadziałało w żywych komórkach, zespół musiał dostarczyć „guzkowy” cukier w formie rozpoznawalnej przez metabolizm komórkowy. Zamiast polegać na normalnych szlakach wychwytu cukrów — które słabo obsługują analogi ksylozy — skonstruowali „zamkniętą” wersję 6AzGlc z ukrytą grupą fosforanową. Po wejściu do cytosolu enzymy komórkowe odsłaniają tę grupę i przekształcają cząsteczkę w UDP‑6AzGlc, aktywowaną formę wymaganą przez przeprojektowane ksylotransferazy. Dokładna chromatografia potwierdziła, że komórki traktowane prawidłowo skonfigurowanym, zamkniętym związkiem wytwarzały znaczne ilości aktywowanego, projektowanego cukru, podczas gdy kontrola będąca lustrzanym odbiciem wytwarzała niemal nic. 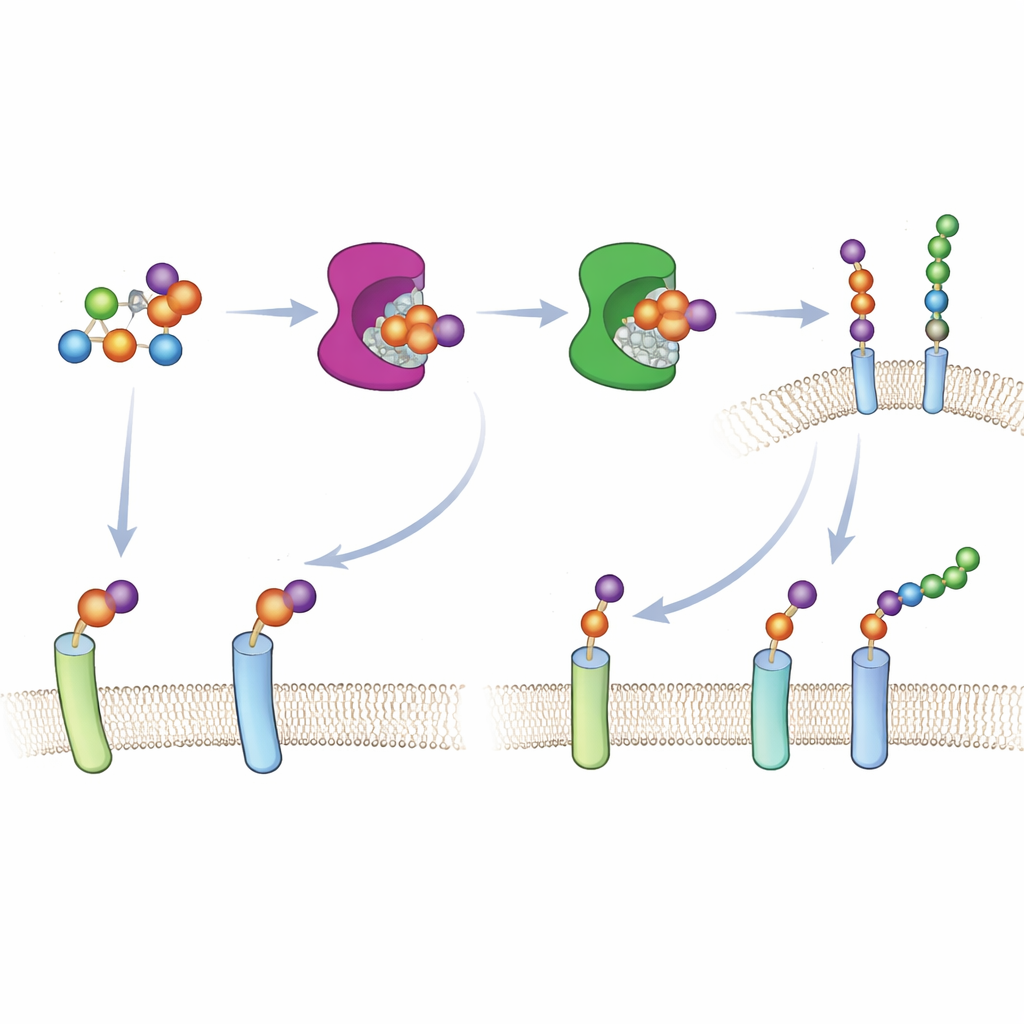
Oznaczanie i identyfikacja ukrytych graczy
Gdy zarówno zmodyfikowany enzym, jak i aktywowany cukier były dostępne, badacze pokazali, że tylko komórki ekspresjonujące zmienione XT1 lub XT2 włączały znacznik 6AzGlc do swoich proteoglikanów powierzchniowych. Grupa azotowa (azydowa) obecna w 6AzGlc służy jako mały chemiczny uchwyt, który można „kliknąć” z barwnikami fluorescencyjnymi lub biotyną, umożliwiając wizualizację i wzbogacenie znakowanych białek. Spektrometria mas z analiz wzbogaconych próbek ujawniła bogaty zestaw znanych proteoglikanów — w tym decorin, wiele glipikanów, syndekan‑4, CD44 i wersikan — potwierdzając, że system oznacza autentyczne białka niosące cukry. Co ważne, przeprojektowane enzymy zachowały te same preferencje sekwencyjne co ich naturalne odpowiedniki, co oznacza, że chemiczny znacznik jest instalowany na autentycznych miejscach przyłączenia, a nie w nowych, sztucznych pozycjach.
Budowanie projektowanych proteoglikanów
Niespodziewaną korzyścią znacznika 6AzGlc jest to, że w przeciwieństwie do naturalnego cukru startowego nie może on być przedłużony do pełnej długości łańcucha przez enzymy następujące dalej w szlaku. Skutecznie zamyka to łańcuch i upraszcza strukturę molekularną, którą trzeba analizować za pomocą spektrometrii mas. Autorzy wykorzystali tę cechę jako narzędzie: po tym jak XT1 wstawia 6AzGlc w naturalne miejsce przyłączenia, używają chemii kliknięcia, by dokręcić syntetyczne fragmenty heparyny, tworząc „projektowane proteoglikany” z precyzyjnie zdefiniowanymi łańcuchami cukrowymi. W komórkach raka piersi pozbawionych własnego syndekanu‑1, dodanie takich projektowanych wersji przywróciło normalne rozprzestrzenianie się na powierzchni pokrytej białkiem, dowodząc, że chemicznie odbudowany proteoglikan może funkcjonalnie zastąpić naturalny.
Co to oznacza dla biologii i medycyny
To badanie dostarcza potężnego zestawu narzędzi do selektywnego znakowania i manipulowania łańcuchami cukrowymi, które kontrolują sposób, w jaki komórki komunikują się. Dzięki rozdzieleniu ról XT1 i XT2 oraz znakowaniu wyłącznie ich bezpośrednich celów, badacze mogą teraz mapować, które proteoglikany działają w określonych tkankach i stanach chorobowych. Możliwość zatrzymania naturalnego wzrostu łańcucha i zastąpienia go niestandardowymi cukrami pozwala również naukowcom rozdzielić, ile funkcji proteoglikanu wynika z jego ramienia białkowego, a ile z cukrowej powłoki. W dłuższej perspektywie taka precyzyjna inżynieria może pomóc odszyfrować złożone sygnałowanie na powierzchni komórki i zainspirować terapie naprawiające lub przeprogramowujące wadliwe powłoki komórkowe w zaburzeniach rozwojowych, raku i innych chorobach.
Cytowanie: Li, Z., Chawla, H., Di Vagno, L. et al. Xylosyltransferase engineering to manipulate proteoglycans in mammalian cells. Nat Chem Biol 22, 612–621 (2026). https://doi.org/10.1038/s41589-025-02113-w
Słowa kluczowe: proteoglikany, glikozoaminoglikany, ksylotransferaza, biologia chemiczna, sygnałowanie na powierzchni komórki