Clear Sky Science · pl
Pojedyncze miejsce allosteryczne łączy aktywację, modulację i inhibicję w TRPM5
Jak jeden mały strażnik kształtuje smak i metabolizm
To, jakie potrawy nam smakują i jak nasze ciało radzi sobie z cukrem, zależy od mikroskopijnych „strażników” białkowych w komórkach. Jednym z takich strażników jest kanał TRPM5, który pomaga nam wyczuwać smaki słodkie, gorzkie i umami oraz wspiera wydzielanie insuliny przez trzustkę. Badanie ujawnia, jak jedna niewielka kieszonka w TRPM5 może działać jak główny pokrętło sterujące — włączać kanał, regulować jego czułość, a nawet go wyłączać — co może naprowadzić na przyszłe terapie cukrzycy, otyłości i zaburzeń jelitowych.
Kanał na styku smaku i poziomu cukru we krwi
TRPM5 znajduje się w błonach komórek smakowych na języku, komórek wydzielających hormony w jelicie oraz komórek wydzielających insulinę w trzustce. Gdy wzrasta stężenie wapnia wewnątrz tych komórek, TRPM5 się otwiera i pozwala na przepływ jonów dodatnich, co chwilowo zmienia potencjał elektryczny komórki. W kubkach smakowych ten sygnał elektryczny informuje mózg, że na języku znajduje się coś słodkiego, gorzkiego lub umami. W trzustce pomaga precyzować wyrzuty insuliny po posiłku. Osoby i zwierzęta z upośledzoną funkcją TRPM5 wykazują problemy z uwalnianiem insuliny i kontrolą poziomu glukozy, co sugeruje, że leki ukierunkowane na TRPM5 mogłyby w przyszłości pomóc w leczeniu chorób metabolicznych. Do niedawna jednak naukowcom brakowało precyzyjnych narzędzi do włączania lub wyłączania tego kanału.
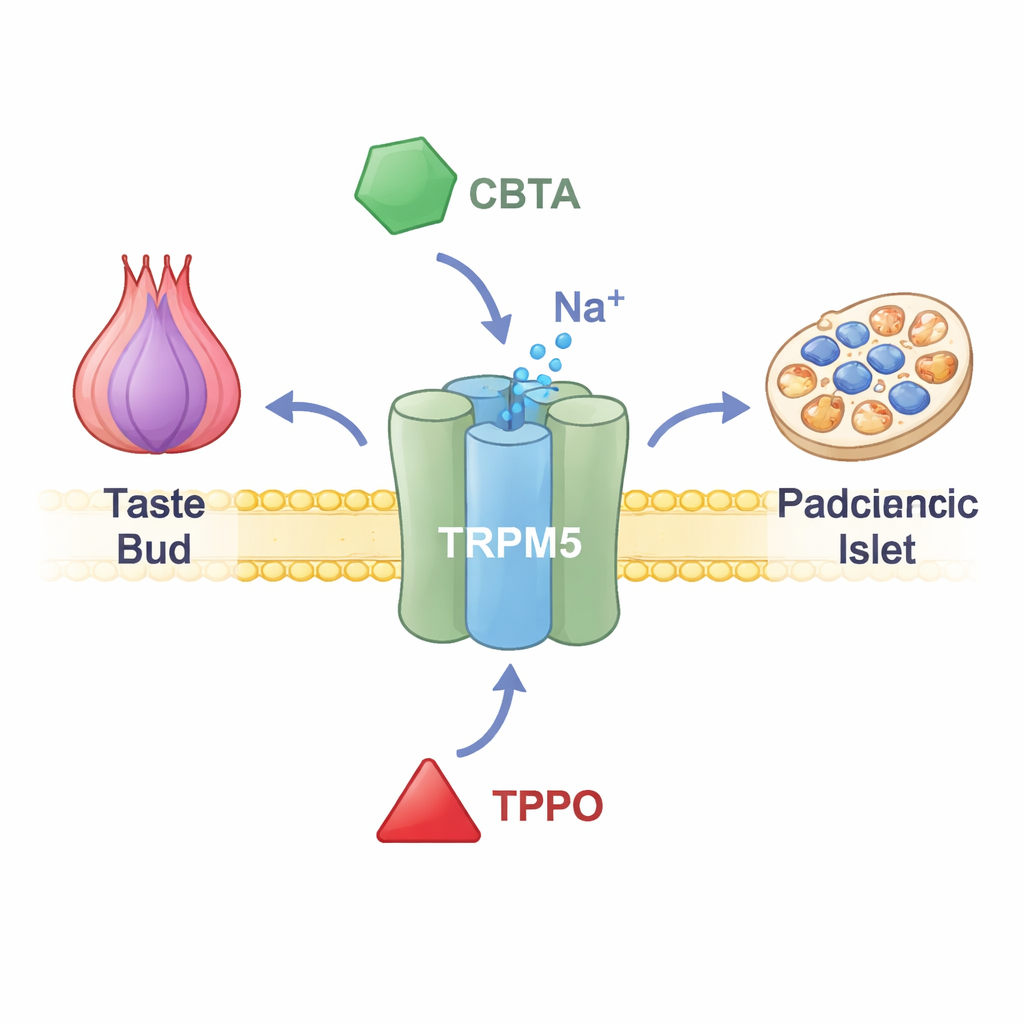
Nowy chemiczny przełącznik, który wzmacnia kanał
Naukowcy skupili się na syntetycznym związku o nazwie CBTA, znanym wcześniej jako stymulator TRPM5, ale słabo zrozumianym. Na podstawie zapisów elektrycznych z komórek zaprojektowanych do produkcji TRPM5 wykazali, że CBTA może otworzyć kanał nawet przy niemal zerowym stężeniu wapnia, co dowodzi, że działa jako prawdziwy aktywator, a nie tylko wzmacnia efekt wapnia. Gdy obecne są śladowe ilości wapnia — poziomy, które normalnie pozostawiają TRPM5 w stanie spoczynkowym — CBTA i wapń działają razem, generując znacznie większe prądy niż każde z nich osobno. Oznacza to, że CBTA czyni TRPM5 niezwykle czułym, tak że niemal spoczynkowe stężenia wapnia nagle stają się wystarczające, by szeroko otworzyć kanał.
Ukryta kieszonka kontroli ujawniona przez cryo-EM
Aby zobaczyć, jak to działa na poziomie atomowym, zespół użył krioelektronowej mikroskopii (cryo-EM) do uchwycenia trójwymiarowych migawkowych obrazów TRPM5 w różnych warunkach. Odkryli, że CBTA zagnieżdża się w wcześniej niezauważonej wnęce w górnej części regionu czującego napięcie kanału, tuż nad miejscem, gdzie zwykle wiąże się wapń. Ta wnęka, utworzona przez skupisko aminokwasów, działa jako precyzyjne miejsce dokujące. Gdy naukowcy zmienili kluczowe elementy wyściełające tę kieszonkę, CBTA nie mogło już aktywować TRPM5, chociaż wapń nadal działał, co potwierdza, że ta drobna nisza jest niezbędna dla działania związku. Co ważne, związanie CBTA subtelnie przestawia pobliskie fragmenty białka w sposób, który ułatwia wapniowi zajęcie jego zwykłego miejsca, wyjaśniając dramatyczną synergiię obserwowaną w pomiarach elektrycznych.
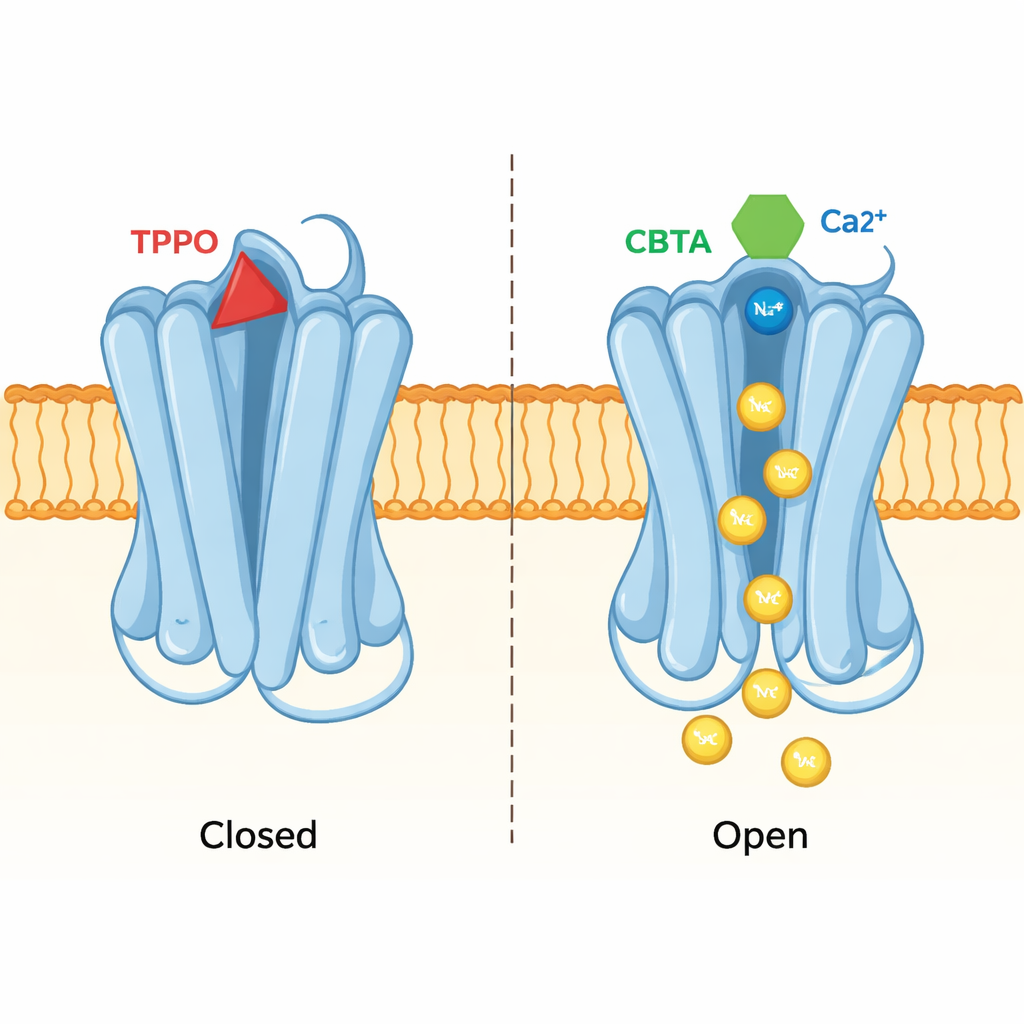
Jedna kieszonka, dwa przeciwne efekty
To samo podejście strukturalne ujawniło, jak inhibitor TPPO wykorzystuje dokładnie tę samą kieszonkę, by wywołać efekt przeciwny. Gdy TPPO się wiąże, oba miejsca wiążące wapń w TRPM5 pozostają napełnione, ale centralny por kanału pozostaje ściśnięty i jony nie przepływają. Porównanie struktur związanych z TPPO i CBTA pokazało, że ich różne kształty naciskają pobliskie segmenty białka w przeciwnych kierunkach. CBTA sprzyja ruchom rozchodzącym się w kierunku poru i jego otwarciu; TPPO natomiast zakłóca komunikację między kieszonką a porem, utrzymując bramkę zamkniętą. W istocie ta jedna kieszonka może działać albo jak przyspieszacz, albo jak hamulec, w zależności od tego, która cząsteczka się w niej znajdzie.
Przekierowanie wewnętrznego okablowania kanału
Badanie pokazuje również, że ta kieszonka kontrolna może przejąć zadania zwykle wykonywane przez oddzielny, wewnętrzny region wiążący wapń. W mutantach kanału, w których zwykłe wewnętrzne miejsce wiążące wapń jest nieaktywne, sam wapń nie był w stanie otworzyć TRPM5. Tymczasem CBTA wciąż włączał te mutanty i przekształcał kluczowy element strukturalny łączący wewnętrzne i zewnętrzne części kanału. W innych mutantach, które przerywają połączenie między wiązaniem wapnia a otwarciem poru, dodanie CBTA przywracało normalne zachowanie. Wyniki te pokazują, że nowo zidentyfikowane miejsce może przekierowywać lub naprawiać komunikację między różnymi domenami kanału, działając jako elastyczne centrum dla sygnalizacji na daleki dystans w obrębie białka.
Dlaczego to ma znaczenie dla przyszłych leków
Dla czytelników nietechnicznych główny przekaz jest taki, że naukowcy znaleźli pojedynczą, wrażliwą na leki kieszonkę w TRPM5, która może integrować aktywację, precyzyjną regulację i wyłączanie. Mały aktywator jak CBTA może jednocześnie naśladować wapń i znacznie zwiększać czułość kanału, podczas gdy inny związek, TPPO, może zatrzasnąć ten sam kanał, wszystkie te efekty są osiągane dzięki dokowaniu w tym samym miejscu. Ten jednolity obraz kontroli TRPM5 otwiera drogę do projektowania wyspecjalizowanych cząsteczek, które albo zwiększą, albo osłabią jego aktywność w konkretnych tkankach, z potencjalnymi zastosowaniami od terapii opartych na wrażeniach smakowych i leków regulujących motorykę jelit po nowe strategie zarządzania poziomem cukru i chorobami metabolicznymi.
Cytowanie: Ruan, Z., Lee, J., Li, Y. et al. A single allosteric site merges activation, modulation and inhibition in TRPM5. Nat Chem Biol 22, 402–410 (2026). https://doi.org/10.1038/s41589-025-02097-7
Słowa kluczowe: kanał TRPM5, percepcja smaku, wydzielanie insuliny, otwieranie kanałów jonowych, modulacja allosteryczna